fuel cell
「fuel cell」の意味・「fuel cell」とは
「fuel cell」は、化学反応により電力を生成する装置を指す。具体的には、燃料と酸化剤を反応させて電気を直接生成する電池の一種である。燃料電池は、化石燃料や水素などの燃料を使用し、その化学エネルギーを電気エネルギーに変換する。この過程は、燃料の酸化と酸化剤の還元という二つの半反応から成り立つ。「fuel cell」の発音・読み方
「fuel cell」の発音は、IPA表記では /ˈfjuːəl sɛl/ となる。IPAのカタカナ読みでは、「フューエル セル」となる。日本人が発音するカタカナ英語の読み方では、「フューエル セル」となる。「fuel cell」の定義を英語で解説
A fuel cell is a device that converts the chemical energy from a fuel into electricity through a chemical reaction with oxygen or another oxidizing agent. Fuel cells are different from batteries in that they require a continuous source of fuel and oxygen to run, but they can produce electricity continually for as long as these inputs are supplied.「fuel cell」の類語
「fuel cell」の類語としては、「energy converter」や「power generator」が挙げられる。これらはいずれもエネルギーを他の形態に変換する装置を指す言葉である。「fuel cell」に関連する用語・表現
「fuel cell」に関連する用語として、「hydrogen fuel cell」、「proton exchange membrane fuel cell」、「solid oxide fuel cell」などがある。これらはそれぞれ、水素を燃料とする燃料電池、プロトン交換膜を使用する燃料電池、固体酸化物を使用する燃料電池を指す。「fuel cell」の例文
1. The fuel cell converts the chemical energy from the fuel into electricity.(燃料電池は燃料からの化学エネルギーを電気に変換する。)2. Fuel cells have the potential to replace the internal combustion engine in vehicles.(燃料電池は車両の内燃機関を置き換える可能性を持っている。)
3. The hydrogen fuel cell is a type of fuel cell that uses hydrogen as its fuel.(水素燃料電池は、水素を燃料とする燃料電池の一種である。)
4. The proton exchange membrane fuel cell is known for its high power density.(プロトン交換膜燃料電池は、その高い出力密度で知られている。)
5. The solid oxide fuel cell operates at very high temperatures.(固体酸化物燃料電池は非常に高い温度で動作する。)
6. Fuel cells are more efficient than traditional combustion technologies.(燃料電池は、伝統的な燃焼技術よりも効率的である。)
7. Fuel cells can be used in a wide range of applications, from portable electronics to large power plants.(燃料電池は、携帯電子機器から大型発電所まで、幅広い用途で使用することができる。)
8. The main challenge for fuel cells is the cost of the catalysts.(燃料電池の主な課題は、触媒のコストである。)
9. The fuel cell system includes a fuel cell stack and a fuel processing system.(燃料電池システムは、燃料電池スタックと燃料処理システムを含む。)
10. Fuel cells are considered a key technology for a sustainable energy future.(燃料電池は、持続可能なエネルギー未来のための重要な技術と考えられている。)
燃料電池
【燃料電池】(ねんりょうでんち)
Fuel Cell.
水素と酸素を反応させて水を生成し、その過程で生じた電気を取り出す電池。
純粋な水素は危険で保存が難しいため、水素保有量の多いメタノールを用いる事が多い。
工業規格としては電解質の違いによって種類分けされている。
電解質によって作動温度が大きく異なるため、用途や出力によって個別の設計が必要とされる。
工業用途
燃料電池は比較的新しく登場した未発展の技術であり、今後の発展が待たれている。
反応による生成物が水以外に何もないため、内燃機関・外燃機関に比べて環境負荷が低い。
また、故障を誘発するような可動部分が無いため信頼性が高い。
このため、将来的にエンジンの代替として普及させる事を目標に研究開発が進められている。
また、構造を維持するために必要な最小単位が小さく、小型化が容易である。
このため、化学的な電池の代替として利用する事も視野に入れて研究開発が行われている。
実際の用途としては発電所、家庭用電源、自動車、携帯電子機器などが想定されている。
また、宇宙船・惑星探査機用の電源として利用する事も想定されている。
発電効率が高く、水しか排出せず、かつ静粛であるため、潜水艦の動力源としても研究されている。
フューエルセル
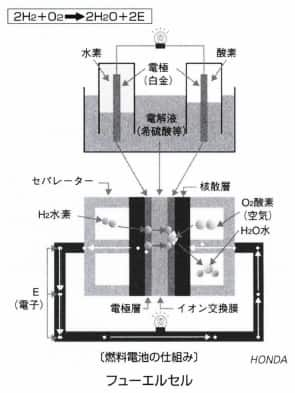
外部から、燃料としての水素と酸化剤(空気中に含まれる酸素など)を連続的に供給して、その電気化学反応によって電気エネルギーを取り出せる電池のことで、一種の発電装置ともいえる。したがって、電気自動車用の電池と異なり充電を必要とせず、エンジン車と同じように燃料を補給すればいつでも、しかも二酸化炭素などの排気ガスを出さないか、または少ない排出で走行できることで、これが次世代の動力源として注目されている理由である。構造的には、電解質とその両側に2つの電極、すなわち燃料極(アノード)と空気極(カソード)があり、さらにその外側を、セパレーターと称する燃料および空気供給用の通路を設けた板状の材料ではさんでいる。アノード側に燃料の水素を加えると触媒が作用して水素イオンと電子が発生し、この水素イオンは電界質を透過して空気極に達する。ここでアノードとカソードをモーターなどの外部負荷を介して結合すると、アノードからカソードに電子が流れ込んで電流が発生し、同時に水素イオンが酸素と反応して水が発生する。この反応は、水に入れた2つの電極に電気を加えると両極に酸素と水素が発生する、水の電気分解の、ちょうど逆の反応と考えればわかりやすい。
燃料電池
【英】: fuel cell
| 陰極に水素を陽極に酸素(空気)を供給し、水の電気分解と反対の電気化学作用を起こさせ、両極間に生ずる電気エネルギーを継続的に取り出す装置である。燃料電池は従来の火力発電のように燃焼の排ガスを発生しないため汚染物質を発生することがなく、また設置に場所を取らないので消費地点の近くに設置することが可能である。さらに発生する熱を利用すると約80%という高いエネルギー利用率が得られる。液体水素を燃料とする燃料電池は米国のアポロ衛星、スペースシャトルなどの宇宙船で実用されているが、大規模経済的な発電用の電池としては天然ガスやメタノールを改質して得られる水素を燃料とし、電極表面の触媒や両極間の電解質の種類に工夫をこらして反応速度、電流密度を上げるため、米国を中心に研究開発が進められている。わが国では通商産業省工業技術院の大型省エネルギー技術開発(ムーンライト計画)の一環としてその研究開発が進められている。 |
燃料電池
(Fuelcell から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/11/09 15:04 UTC 版)

燃料電池(ねんりょうでんち、英: fuel cell)は、燃料(多くは水素[1])と酸化剤(多くは酸素)の化学エネルギーを、一対の酸化還元反応によって電気に変換する電気化学電池である[2]。燃料電池が多くの電池と異なる点は、化学反応を維持するために燃料と(通常は空気からの)酸素を継続的に供給する必要がある点である。一方、電池では化学エネルギーは通常、電池内に既に存在する物質から得られる[3]。燃料電池は、燃料と酸素が供給される限り、継続的に電気を作り出すことができる。
最初の燃料電池は、1838年にウィリアム・グローブにより発明された。その後、1932年にフランシス・ベーコンが水素-酸素燃料電池を発明して以来、1世紀近くにわたって商業利用されてきた。アルカリ型燃料電池は、発明者の名前をとってベーコン型燃料電池とも呼ばれ、1960年代半ばからNASAの宇宙計画で人工衛星や宇宙カプセルの発電に使用されてきた。それ以来、燃料電池は他の多くのアプリケーションにも使用されている。燃料電池は、商業施設、産業施設、住宅、遠隔地やアクセスが困難な場所での一次電源やバックアップ電源として使用されている。また、フォークリフト、自動車、バス、鉄道車両、ボート、オートバイ、潜水艦などの輸送機器の動力源としても使用されている。
燃料電池にはさまざまな種類があるが、いずれも陽極と陰極、そしてイオン(多くは正電荷の水素イオン(プロトン))を行き来させる電解質で構成され、その電解質は燃料電池の両側面に存在する。陽極では、触媒によって燃料が酸化反応を起こし、イオン(多くの場合、正電荷の水素イオン)と電子が生成される。イオンは電解質を通って陽極から陰極に移動する。同時に、電子は外部回路を通って陽極から陰極に流れ、直流電気を発生させる。陰極では、別の触媒によってイオン、電子、酸素が反応し、水やその他の物質が生成される。燃料電池は電解質の種類によって分類され、起動時間が1秒の固体高分子形燃料電池(PEM燃料電池、PEMFC)から10分の固体酸化物型燃料電池(SOFC)までの差がある。関連技術として、充電することで燃料が再生されるフロー電池がある。個々の燃料電池の電位は0.7ボルト程度と比較的小さいため、用途に応じて十分な電圧を発生させるために、電池を「積み重ねる」、つまり直列に配置する[4]。燃料電池は電気だけでなく、水蒸気や熱も発生し、燃料によってはごく微量の二酸化窒素などの排出物もある。一般的に普及している燃料電池自動車やエネファームでの発電効率は30~40%であり、PEFC燃料電池の発電効率はそこまで高くない。ただしエネファームでは効率の悪さからくる廃熱を給湯に回す事でエネルギー効率の向上が可能である。また高温域で運転するSOFCによるコジェネレーション方式で廃熱を回収すれば、最大85%の効率を得ることができる[5]。
方式

使用する電解質の種類によって主に4種類の燃料電池の方式が研究されている。アルカリ電解質形燃料電池(AFC)は、従来方式であり今後の利用は限定的だと考えられている。バイオ燃料電池は、他方式と全く異なっており不明な点が多い。
固体高分子形燃料電池 (PEFC)
固体高分子(膜)形燃料電池(PE(M)FC, Polymer Electrolyte (Membrane) Fuel Cell)は、イオン交換膜を挟んで、正極に酸化材を、負極に還元材(燃料)を供給することにより発電する。イオン交換膜としてナフィオンなどのプロトン交換膜を用いた場合は、プロトン交換膜燃料電池(PEMFC, Proton Exchange Membrane Fuel Cell)とも呼ばれる。起動が早く、運転温度も80-100℃と低い。水素を燃料に用いる場合では、触媒に高価な白金を使用しており、燃料中に一酸化炭素が存在すると触媒の白金が劣化する。発電効率は30-40%程と燃料電池の中では比較的低い。
リン酸型に次いで実用化が進んでおり、主に小型用途での発電使用が想定されている。触媒として使用される白金の使用量を減らすことによるコスト低減、電解質として使用されるフッ素系イオン交換樹脂の耐久性向上などが今後の普及における課題である。
室温動作と小型軽量化が可能であるため、携帯機器、家庭用コージェネレーション、燃料電池自動車などでの利活用が進められている。
リン酸形燃料電池 (PAFC)
リン酸形燃料電池(PAFC, Phosphoric Acid Fuel Cell)は、電解質としてリン酸(H3PO4)水溶液をセパレーターに含浸させて用いる。動作温度は200℃程度で、発電効率は、約40%LHV。固体高分子形燃料電池と同様に白金を触媒としているため、燃料中に一酸化炭素が存在すると触媒の白金が劣化する。従って、天然ガスなどを燃料とする場合は、あらかじめ水蒸気改質・一酸化炭素変成反応により一酸化炭素濃度が1%程度の水素をつくり、電池本体に供給する必要がある。
工場、ビルなどの需要設備に設置するオンサイト型コジェネレーションシステムとして100/200kW級パッケージの市場投入がなされ、すでに商用機にて4万時間以上の運転寿命(スタック・改質器無交換)を達成している[注 1]。
溶融炭酸塩形燃料電池 (MCFC)
溶融炭酸塩形燃料電池(MCFC, Molten Carbonate Fuel Cell)は、水素イオン(H+)の代わりに炭酸イオン(CO32-)を用い、溶融した炭酸塩(炭酸リチウム、炭酸カリウムなど)を電解質として、セパレーターに含浸させて用いる。そのため、水素に限らず天然ガスや石炭ガスを燃料とすることが可能である。動作温度は600℃-700℃程度。常温では固体の炭酸塩も動作温度近傍では溶融するため、電解質として用いることができる。PAFCに競合する選択肢として、250kW級パッケージが市場に投入されつつある。発電効率は約45%LHV。白金触媒を用いないためPEFCやPAFCと異なり一酸化炭素による被毒の心配がなく、排熱の利用にも有利である。内部改質方式とされるが、プレリフォーミング用の改質器をシステム内に設置するのが一般的のようである。火力発電所の代替などの用途が期待されている[注 2]。
なお、通常の燃焼反応では、空気中の窒素の存在により排ガス中の二酸化炭素濃度は約20%が上限であり、更に二酸化炭素濃度を高めるには空気の代わりに酸素を用いなければならない。しかし、MCFCは炭酸イオンが電池反応に介在し、空気極側の二酸化炭素と酸素が選択的に燃料極側に移動・蓄積するため燃料極側排ガスの二酸化炭素濃度は80%程度にも達する。この性質を利用し、MCFCで二酸化炭素の回収を行うことが試みられている。日本国内では経産省補助事業として中国電力・中部電力が共同実施している[6]。
固体酸化物形燃料電池 (SOFC)
固体酸化物形燃料電池(SOFC, Solid Oxide Fuel Cell)は、固体電解質形燃料電池とも呼ばれ、動作温度は700-1,000℃を必要とするので高耐熱性の材料が必要となる。また、起動・停止時間も長い。電解質として酸化物イオンの透過性が高い安定化ジルコニアやランタン、ガリウムのペロブスカイト酸化物などのイオン伝導性セラミックスを用いており、空気極で生成した酸化物イオン(O2-)が電解質を透過し、燃料極で水素あるいは一酸化炭素と反応することにより電気エネルギーを発生させている。そのため、水素だけではなく天然ガスや石炭ガスなども、脱硫処理は必要であるが、簡単な水蒸気改質処理(一酸化炭素の除去が不要で、燃料中に若干の未改質ガスを含む改質)により燃料として用いることが可能である。活性化電圧降下が少ないので発電効率は高く、すでに56.1%LHVを達成している例もある。家庭用・業務用の1kW-10kW級としても開発されている[注 3]。 原理的には発電部分における改質(ニッケルを含む燃料極における直接内部改質)が可能であるが、吸熱反応による発電部分の極端な温度変化を防ぐために、プレリフォーマー(発電反応による熱や反応後の燃料を燃焼した熱を利用した間接内部改質)を採用するのが一般的である。固体高分子形燃料電池等の他の燃料電池で使用される白金やパラジウム等の貴金属系の触媒が不要で燃料極としては、ニッケルと電解質セラミックスによるサーメット、空気極としては導電性セラミックスを用いる。大型SOFCは、燃焼排ガスをガスタービン発電や蒸気発電に利用すれば、極めて高い総合発電効率を得ることが出来ると予測されるため、火力発電所の代替などの用途が期待されている。[注 4][注 5]
日本ガイシ株式会社は2009年6月11日に独自構造のSOFCを開発し、世界最高レベルの63%の発電効率(LHV)と90%の高い燃料利用率を達成したと発表した。[7]
JX日鉱日石エネルギーは2011年10月、市販機としては世界初となるSOFC型「エネファーム」を発売した[8]。
アルカリ電解質形燃料電池 (AFC)
アルカリ電解質形燃料電池(AFC, Alkaline Fuel Cell)は、水酸化物イオンをイオン伝導体とし、アルカリ電解液を電極間のセパレータに含侵させてセルを構成している。PEFCと同様、高分子膜を用いるタイプも報告されている。最も構造が簡単であり、アルカリ雰囲気での使用であることから、ニッケル酸化物等の安価な電極触媒を利用することができること、常温にて液体電解質を用いることからセル構成も単純にできるため、信頼性が高く、宇宙用途などに実用化されている燃料電池である。一方、改質した炭化水素系燃料から水素を取り出す場合、炭化水素が混入しているとアルカリ性電解液が炭酸塩を生じて劣化する。同様に空気を酸化剤として用いると電解液が二酸化炭素を吸収して劣化するため、純度の高い酸素を酸化剤として用いる必要がある。水素の純度を高めるためには、パラジウムの膜を透過させることにより純度を高める。電解質が水溶液であるため、作動温度域は電解液が凍結・蒸発しない温度に制限される。また、温度によりイオンの移動度(拡散係数)が変わり、発電力に影響するため、温度条件が厳しい。ニッケル系触媒は配位性のある一酸化炭素、炭化水素、酸素および水蒸気等により活性が下がるので水素燃料の純度は重要である。これらを不純物として含む改質水素の使用は望ましくない。
21世紀現在の燃料電池の研究開発上ではほとんど目を向けられることはないが、年少向けの教材から、アポロ計画やスペースシャトルまで広く「実用化」されている。アポロ13号における事故はこの燃料電池に供給する液体酸素供給系統の不具合に起因したものであり、燃料電池そのものの問題ではない。
ダイハツ工業は産業技術総合研究所と共同で水加ヒドラジン(N2H4・H2O)を燃料として0.50W/cm2の出力密度を達成したと発表している[9]。この場合、燃料電池への炭化水素の混入はなく、排出物は水と窒素のみとなる。
直接形燃料電池 (DFC)
直接形燃料電池(DFC, Direct Fuel Cell)は、改質器を介さずに燃料を直接セルスタックに供給する形式で、メタノール、エタノール、ジメチルエーテル、ヒドラジン、ホルムアルデヒド、ギ酸、アンモニア等を使用するものが試みられてきた[注 6]。つまり、DFCは燃料電池それ自身の方式を指す言葉ではない。固体酸化物形燃料電池は全てDFCに属する。燃料として用いる物質に炭素が含まれている場合、反応(発電)によって二酸化炭素が生成して排出される。そのため、アルカリ性水溶液の電解質は炭酸塩を生成するので使用できない。ヒドラジンのような還元性の燃料を使用する場合には貴金属の触媒が不要になるため、貴金属フリー液体燃料燃料電池として注目される。燃料供給ポンプや放熱ファンを使うか否かで、パッシブ型とアクティブ型に区分される。燃料極の白金に反応中間体である一酸化炭素が強吸着(被毒)してしまい反応速度が遅く、水溶性の高い燃料を用いた場合では燃料のクロスオーバーが起こるため、電力・発電効率とも低いが小型軽量のものが作れる。直接形メタノール燃料電池(DMFC)では、数十mW-10W程度の小規模小電力発電に適している。これらは小型携帯電子機器の電源としての用途が考えられている。一方で設置型には1kw級の発電能力を有する物もある[10]。
バイオ燃料電池 (BFC)
食物からエネルギーを取りだす生体システムを応用した燃料電池である[注 7]。燃料を酸化する触媒として酵素や微生物などが用いられる。酵素を用いた燃料電池においては、環境の変化に対しても安定して働く強力な酵素が不可欠であり、研究開発では、酵素の寿命を伸ばすことなどが課題となっている。血液中のグルコースを利用する体内埋め込み型ペースメーカーの開発が行われている[11]。微生物を用いた燃料電池(微生物燃料電池)においては、廃水中の有機物の利用などといった観点から研究されることが多い。
類似の研究には、光合成による植物の生体システムを応用した「太陽光バイオ燃料電池」もある。
主要4方式の比較
21世紀初頭現在、研究開発が進められている主要な4つの方式について比較を示す。
| PEFC 固体高分子形 |
PAFC リン酸形 |
MCFC 溶融炭酸塩形 |
SOFC 固体酸化物形 |
||
|---|---|---|---|---|---|
| 電解質 | 電解質材料 | イオン交換膜 | リン酸 | 炭酸リチウム、炭酸ナトリウム | 安定化ジルコニアなど |
| 移動イオン | 
燃料電池の原型として知られる 燃料電池の原理は1801年にイギリスのハンフリー・デービーによって考案された。現在の燃料電池に通じる燃料電池の原型は1839年にイギリスのウィリアム・グローブによって作製された。この燃料電池は、電極に白金を、電解質に希硫酸を用いて、水素と酸素から電力を取り出し、この電力を用いて水の電気分解をすることができた。 その後、燃料電池は、熱機関により動かされる発電機の登場によって発電システムとしてはしばらく忘れられたが、1955年、米ゼネラル・エレクトリック社(GE社)に勤務していた化学者であるW. Thomas Grubbはスルホ基で修飾されたスチレンによるイオン交換膜を電解質として用いた改良型燃料電池を開発した。3年後、GE社の別の化学者であるLeonard Niedrachは、触媒である白金の使用量を減らすことに成功し、Grubb-Niedrach 燃料電池として知られる事となった。GE社はこの技術の開発と利用を、当時進行中だったアメリカ航空宇宙局のジェミニ宇宙計画に働きかけて採用され、これが燃料電池の最初の実用となった。 1965年にアメリカ合衆国の有人宇宙飛行計画であるジェミニ5号で炭化水素系樹脂を使用した固体高分子形燃料電池が採用され、再び燃料電池が注目されるようになった。1959年、フランシス・トーマス・ベーコンは5kWの定置式燃料電池の開発に成功した。1959年、Harry Ihrigが率いるチームによって15kW出力の燃料電池トラクターが米国ウイスコンシン州のアリスシャルマーズ社の米国横断フェアーで公開された。このシステムは水酸化カリウムを電解質として使用して、圧縮水素と酸素を反応させていた。1959年、ベーコンと協力者は5kWの装置で溶接機の電源として使用できることを示した。1960年代、プラット&ホイットニー社は米国の宇宙計画に於いて宇宙船の電力と水を供給するために、ベーコンの米国での特許の使用許諾を得た。アポロ計画からスペースシャトルに至るまで燃料電池は電源、飲料水源として使用された。その際は材料の信頼性による検討の結果、アルカリ電解質形燃料電池が採用された。 民生用燃料電池として、住宅用のコジェネレーションシステムや発電施設向けに研究開発が続けられた。日本においては、通商産業省の省エネルギー政策「ムーンライト計画」に基づき、リン酸形、溶融炭酸塩形燃料電池、固体電解質形燃料電池の開発が始められた。1982年、東芝が50kWリン酸形燃料電池実験プラントを浜川崎工場に建設し、加圧形として日本初めての発電に成功。1985年には米国UTCとIFC社(米国コネチカット州)を設立し、世界最大の11MW級プラントの共同開発を開始し、1991年には、11MW実験プラントを東京電力五井火力発電所に完成させ、出力1万1000kWのリン酸形燃料電池の実証運転が行われた。 1987年、カナダのバラード パワーシステム社がフッ素系樹脂(Nafion)を電解質膜に用いた固体高分子形燃料電池を開発した。この電解質膜の耐久性に優れていたことから、燃料電池が再び注目されるようになり、研究開発が盛んになった。 米国防総省と国防総省高等研究事業局(DARPA)のローレンス・H・デュボワは、様々な液体炭化水素(メタノール、エタノールなど)で動く燃料電池に着目して、南カリフォルニア大学(USC)のローカー炭化水素研究所に所属していた酸の専門家スルヤ・プラカッシュと、ノーベル賞受賞者のジョージ・A・オラーに声をかけた。USCはジェット推進研究所、カリフォルニア工科大学の協力の下、液体炭化水素が直接酸化するシステムを発明し、のちにダイレクトメタノール燃料電池(DMFC)と名付けられた。 1994年、ダイムラーベンツ(当時)が燃料電池自動車の試作車を発表した。また、トヨタは、1997年の東京モーターショーに燃料電池自動車の試作車を発表し、2005年までに量産化することを宣言した[注 8]。 2000年代2001年には、ソニー・日立製作所・日本電気が、相次いで「携帯機器向けの燃料電池」の開発を発表している。 2002年12月には、トヨタ・FCHVおよびホンダ・FCXの燃料電池自動車の市販第一号が日本国政府に納入され、小泉純一郎首相が試乗を行った。これらは総理大臣官邸と経済産業省で使用され、24時間のフルメンテナンス体制付きのリース契約となった。 2003年には、東京都交通局にトヨタ・日野自動車製の燃料電池バスが納入、2004年末までお台場周辺で運行された。2005年には愛知万博で日野製FCHV-BUSが納入された。また、2004年には日産も横浜市などへ納入した。2006年からは、愛知万博で使用された水素ステーションが移設された中部国際空港でも運行されている。これらの公共バスは、一般人が乗る事が出来る燃料電池車であるといえる。 主に1980-1990年代に、燃料電池の開発段階に応じて、リン酸形燃料電池を「第1世代型燃料電池」、溶融炭酸塩形燃料電池を「第2世代型燃料電池」、固体酸化物形(固体電解質形)燃料電池を「第3世代型燃料電池」と呼んでいた時期もあるが、固体高分子形燃料電池が開発の主役となってから、21世紀現在、この呼び方が用いられることは殆どない。 2014年末には、トヨタが水素燃料電池により長距離走行を可能とする「MIRAI」を発売した。 2024年4月、商船三井は電気推進の旅客船「HANARIA」の営業を関門海峡エリアで開始した[13]。水素燃料電池、バイオディーゼル発電機、リチウムイオン電池を搭載したハイブリッドシステムを採用し、化石燃料に比べ0~47%の温室効果ガス排出で運航できる[14]。水素タンクはポータブル式で船尾甲板上に設置。燃料電池セル・水素タンクはトヨタ自動車、FCシステムはヤンマーパワーテクノロジーによる[15]。238総トン、全長33m、速力10.2ノット。国内初の水素燃料旅客船であり、シップ・オブ・ザ・イヤー2024を受賞[16]。
規制燃料電池の実用化には、消防法、高圧ガス保安法、電気事業法及び建築基準法(メタノールを燃料とするものは、さらに毒物劇物取扱法)などの法的規制緩和が必要であるとされ、電気設備技術基準などの見直しが行われた。2002年10月には米国運輸省が燃料電池の飛行機内持ち込みを許可するなど、燃料電池普及に向けた規制緩和の方針をいち早く打ち出している。また、安全基準や性能評価について国際的な基準制定の動きもある。 国際標準化1998年に、国際電気標準会議(IEC)内の105番目の専門委員会であるTC105が発足し、燃料電池に関する電気分野での標準化が話し合われ、すでに8つの規格が規定されている。また、電気分野以外での標準化は国際標準化機構(ISO)で行なわれている[12]。 普及への課題燃料電池を普及させるための最も大きな課題は、コストや効率の低さである。購入時の初期コストと使用期間にかかるランニング・コストが共に高いため、普及を妨げている。さらに耐久性・発電効率の向上・電解質の長寿命化やインフラ整備等の課題が指摘されてきた[12][17]。 また水素が非常に扱い難い性質である為、コストが非常に高くなってしまう事や、そもそも地球上に存在しない水素を化石燃料から製造しており、環境負荷への影響が懸念されている。[18] 触媒に白金のような貴金属を使用する方式の場合、貴金属が不足する可能性が指摘されている[19]。 燃料電池のシステム全体としての効率の低さは無視できないレベルであり、水素の製造・輸送・圧縮・発電において未だに発展途上である。
→「燃料電池自動車 § エネルギー効率」も参照
実用化2007年現在、欧州のキャンピングカーにおいて、メタノールを使用したものが開発され、2009年春、日本仕様として、エタノール濃度を調整した製品の販売が開始された。また、液化石油ガス (LPG) を使用するものが、数年の間に採用される[20]。また、リン酸形燃料電池であるUTC Power製の400kWPAFCが、ニューヨークのフリーダム・タワーに12台設置される。 なお、2009年6月4日に放送されたテレビ東京「ニュースモーニングサテライト」で、京都のベンチャー企業が携帯電話やデジタルオーディオプレーヤーの充電用として、水から水素を分離して燃料とする小型の燃料電池を2010年春にコンビニエンスストアで「高校生の小遣いで買える」価格で発売を開始すると報じられたが、詳細については不明である[21]。 2009年10月22日、東芝がモバイル機器の充電用としてメタノールを燃料とする小型のモデルの販売を、台数限定で開始した[22]。IEC (国際電気標準会議) の安全性規格 (暫定版) に準拠、としている。 米国ニュージャージー州において太陽光発電パネルと水素燃料による住宅設備のフル稼働がおこなわれている[23]。 用語燃料電池の説明では、いくつか特有の用語を使用する。一般的な用語もあるが、燃料電池だけの独自の意味を持つものもある。
燃料極=アノード=(陽極)=負極である。つまり通常の電池でいうマイナス極である。
空気極=カソード=(陰極)=正極である。つまり通常の電池でいうプラス極である。
電子伝導性があり、イオン伝導性がなく、剛直であり、ガス・液体を通さないことが必要である。 リチウムイオン電池などにおいては「セパレータ」はイオンの通過する部分の正負極を、静電的に絶縁する層を指し、燃料電池においては電解質層に当たるものであり、注意が必要である。 脚注注釈
出典
参考文献
関連項目外部リンク
|
||||
「Fuel cell」の例文・使い方・用例・文例
- Fuelcellのページへのリンク









