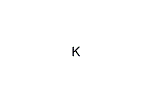人体に必要なミネラルの一種で、成人の体内には約120gから200gが含まれています。遊離イオンやリン酸塩、たんぱく質との結合体としてそのほとんどが細胞内にありますが、ごく一部は血液やリンパなどの体液(細胞外液)や骨にも含まれています。
カリウムは、細胞内液の浸透圧を調節して一定に保つ働きがあります。また、神経の興奮性や筋肉の収縮に関わっており、体液のpHバランスを保つ役割も果たしています。ナトリウムを身体の外に出しやすくする作用があるため、塩分の摂り過ぎを調節するのに役立ちます。「日本人の食事摂取基準(2005年版)」では、高血圧の予防を目的としたカリウム摂取の目標量を成人男女とも1日当たり3,500mgとしています。不足するとこれらの働きに影響することはもちろん、脱力感、食欲不振、筋無力症、精神障害、不整脈などの症状がみられることがあります。なお、大量に摂取した場合でも体内の調節機構が働くので、通常、カリウムが過剰になることはまれであると言われています。
カリウム【(ドイツ)Kalium】
カリウム
カリウム
カリウム(K)
カリウム
【英】:K
カリウム
カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/02/12 02:54 UTC 版)
カリウム(ドイツ語: Kalium [ˈkaːliʊm]、新ラテン語: kalium)は原子番号19番の元素である。ポタシウム(剥荅叟母、Potassium [poʊˈtæsiəm]) 、加里(カリ)ともいう。元素記号はK。原子量は39.10。アルカリ金属、典型元素のひとつ。生物にとって必須元素である。
- ^ Haynes, William M., ed (2011). 化学と物理のCRCハンドブック (92nd ed.). CRC Press. p. 4.122. ISBN 1439855110
- ^ Davy, Humphry (1808). “On some new phenomena of chemical changes produced by electricity, in particular the decomposition of the fixed alkalies, and the exhibition of the new substances that constitute their bases; and on the general nature of alkaline bodies”. Philosophical Transactions of the Royal Society 98: 32. doi:10.1098/rstl.1808.0001.
- ^ a b c 村上雅人『元素を知る事典: 先端材料への入門』海鳴社、2004年、100頁。ISBN 9784875252207。
- ^ Klaproth, M. (1797) "Nouvelles données relatives à l'histoire naturelle de l'alcali végétal" (New data regarding the natural history of the vegetable alkali), Mémoires de l'Académie royale des sciences et belles-lettres (Berlin), pp. 9–13 ; see p. 13. From p. 13: "Cet alcali ne pouvant donc plus être envisagé comme un produit de la végétation dans les plantes, occupe une place propre dans la série des substances primitivement simples du règne minéral, &I il devient nécessaire de lui assigner un nom, qui convienne mieux à sa nature.
La dénomination de Potasche (potasse) que la nouvelle nomenclature françoise a consacrée comme nom de tout le genre, ne sauroit faire fortune auprès des chimistes allemands, qui sentent à quel point la dérivation étymologique en est vicieuse. Elle est prise en effet de ce qu'anciennement on se servoit pour la calcination des lessives concentrées des cendres, de pots de fer (pott en dialecte de la Basse-Saxe) auxquels on a substitué depuis des fours à calciner.
Je propose donc ici, de substituer aux mots usités jusqu'ici d'alcali des plantes, alcali végétal, potasse, &c. celui de kali, & de revenir à l'ancienne dénomination de natron, au lieu de dire alcali minéral, soude &c."
(This alkali [i.e., potash] — [which] therefore can no longer be viewed as a product of growth in plants — occupies a proper place in the originally simple series of the mineral realm, and it becomes necessary to assign it a name that is better suited to its nature.
The name of "potash" (potasse), which the new French nomenclature has bestowed as the name of the entire species [i.e., substance], would not find acceptance among German chemists, who feel to some extent [that] the etymological derivation of it is faulty. Indeed, it is taken from [the vessels] that one formerly used for the roasting of washing powder concentrated from cinders: iron pots (pott in the dialect of Lower Saxony), for which roasting ovens have been substituted since then.
Thus I now propose to substitute for the until now common words of "plant alkali", "vegetable alkali", "potash", etc., that of kali ; and to return to the old name of natron instead of saying "mineral alkali", "soda", etc.) - ^ Davy, Humphry (1809). “Ueber einige neue Erscheinungen chemischer Veränderungen, welche durch die Electricität bewirkt werden; insbesondere über die Zersetzung der feuerbeständigen Alkalien, die Darstellung der neuen Körper, welche ihre Basen ausmachen, und die Natur der Alkalien überhaupt [On some new phenomena of chemical changes that are achieved by electricity; particularly the decomposition of flame-resistant alkalis [i.e., alkalies that cannot be reduced to their base metals by flames, the preparation of new substances that constitute their [metallic] bases, and the nature of alkalies generally]”]. Annalen der Physik 31 (2): 113–175. Bibcode: 1809AnP....31..113D. doi:10.1002/andp.18090310202. "p. 157: In unserer deutschen Nomenclatur würde ich die Namen Kalium und Natronium vorschlagen, wenn man nicht lieber bei den von Herrn Erman gebrauchten und von mehreren angenommenen Benennungen Kali-Metalloid and Natron-Metalloid, bis zur völligen Aufklärung der chemischen Natur dieser räthzelhaften Körper bleiben will. Oder vielleicht findet man es noch zweckmässiger fürs Erste zwei Klassen zu machen, Metalle und Metalloide, und in die letztere Kalium und Natronium zu setzen. — Gilbert. (In our German nomenclature, I would suggest the names Kalium and Natronium, if one would not rather continue with the appellations Kali-metalloid and Natron-metalloid which are used by Mr. Erman [i.e., German physics professor Paul Erman (1764–1851)] and accepted by several [people], until the complete clarification of the chemical nature of these puzzling substances. Or perhaps one finds it yet more advisable for the present to create two classes, metals and metalloids, and to place Kalium and Natronium in the latter — Gilbert.)"
- ^ Berzelius, J. Jacob (1814) Försök, att, genom användandet af den electrokemiska theorien och de kemiska proportionerna, grundlägga ett rent vettenskapligt system för mineralogien [Attempt, by the use of electrochemical theory and chemical proportions, to found a pure scientific system for mineralogy]. Stockholm, Sweden: A. Gadelius., p. 87.
- ^ 19. Kalium (Potassium) – Elementymology & Elements Multidict. vanderkrogt.net
- ^ McNaught, A. D. and Wilkinson,A. eds. (1997). Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). IUPAC. Blackwell Scientific Publications, Oxford.
- ^ a b 櫻井、鈴木、中尾 (2003) 24頁。
- ^ James, Arthur M.; Lord, Mary P. (1992). Macmillan's Chemical and Physical Data. London: Macmillan. ISBN 0-333-51167-0
- ^ a b Dye, J. L. (1979). “Compounds of Alkali Metal Anions”. Angewandte Chemie International Edition 18 (8): 587–598. doi:10.1002/anie.197905871.
- ^ 千谷 (1959) 83頁。
- ^ Helmenstine, Anne Marie. “Qualitative Analysis – Flame Tests”. About.com. 2011年5月9日閲覧。
- ^ コットン、ウィルキンソン (1987) 249-250頁。
- ^ a b c Winter, Mark. “Potassium: Key Information”. Webelements. 2011年5月8日閲覧。
- ^ Davy (1808) p. 25.
- ^ a b ショアー、ボルハルト (2004) 361頁。
- ^ a b c d Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). “Potassium” (German). Lehrbuch der Anorganischen Chemie (91-100 ed.). Berlin: Walter de Gruyter. ISBN 3-11-007511-3
- ^ Burkhardt (2006) p. 35.
- ^ 化学大辞典編集委員会 (編)『化学大辞典』共立出版、1993年。
- ^ コットン、ウィルキンソン (1987) 253頁。
- ^ Burkhardt (2006) p. 32.
- ^ 日本工業規格、JIS K0102 工場排水試験方法。
- ^ 日本工業規格、JIS K0400-49-20 水質―ナトリウム及びカリウムの定量―第2部:原子吸光法によるカリウムの定量。
- ^ 日本分析化学学会 (2008) 97頁。
- ^ 榊徹 (2003年). “イオン選択電極”. エーアンドティー. p. 5. 2011年9月28日閲覧。
- ^ 日本分析化学学会 (2008) 106頁。
- ^ レイナーキャム無機化学(原著第4版). 株式会社 東京化学同人. (2016年10月20日)
- ^ Cameron, A. G. W. (June 1957). Stellar Evolution, Nuclear Astrophysics, and Nucleogenesis. Chalk River Laboratory report CRL-41
- ^ a b c Georges, Audi (2003). “The NUBASE Evaluation of Nuclear and Decay Properties”. Nuclear Physics A (Atomic Mass Data Center) 729: 3-128. Bibcode: 2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ President and Fellows Harvard College. “Radioactive Human Body”. Harvard Natural Sciences Lecture Demonstrations. 2011年10月1日閲覧。
- ^ Winteringham, F. P. W. (1989). Radioactive fallout in soils, crops and food. FAO Soils Bulletin 61. Rome: Food and Agriculture Organization of the United Nations. p. 32. ISBN 9789251028773 2011年5月15日閲覧。
- ^ Monroe, James Stewart; Wicander, Reed; Hazlett, Richard W. (2007). Physical Geology: Exploring the Earth (6th ed. ed.). Belmont, CA: Thomson Brooks/Cole. p. 80. ISBN 9780495011484
- ^ a b c “自然起源放射性物質データベース(窒素肥料・リン酸肥料・カリ肥料)” (pdf). 独立行政法人 放射線医学総合研究所. pp. 10-11. 2011年5月8日閲覧。
- ^ “SIDS 初期評価プロファイル 塩化カリウム” (pdf). 一般社団法人 日本化学物質安全・情報センター. p. 2. 2011年5月8日閲覧。
- ^ a b c Prud'homme, Michel; Krukowski, Stanley T. (2006). “Potash”. In Kogel, Jessica Elzea; Trivedi, Nikhil C.; Barker, James M.; Krukowsk, Stanley T.. Industrial Minerals & Rocks. Littleton, CO: Society for Mining, Metallurgy, and Exploration. pp. 723–740. ISBN 9780873352338
- ^ Burkhardt, Elizabeth R. (2003). “Potassium and Potassium Alloys”. In Ullmann, Fritz; Bohnet, Matthias. Ullmann's encyclopedia of industrial chemistry. 29. Weinheim: Wiley-VCH. p. 83
- ^ Garrett, Donald E. (1996). Potash: deposits, processing, properties and uses. London: Chapman & Hall. ISBN 9780412990717
- ^ Wishart, David J. (2004). Encyclopedia of the Great Plains. University of Nebraska Press. p. 433. ISBN 9780803247871
- ^ Ober, Joyce A. (2008年). “Mineral Commodity Summaries 2008: Potash”. United States Geological Survey. 2008年11月20日閲覧。
- ^ Micale, Giorgio; Cipollina, Andrea; Rizzuti, Lucio (2009). Cipollina, Andrea; Micale, Giorgio; Rizzuti, Lucio. ed. Seawater Desalination: Conventional and Renewable Energy Processes. Berlin: Springer. p. 3. ISBN 9783642011498
- ^ a b Ober, Joyce A. (2007年). “Mineral Yearbook 2006: Potash”. United States Geological Survey. 2008年11月20日閲覧。
- ^ 荻野博『典型元素の化合物』岩波講座 現代科学への入門 11、岩波書店、2004年、150頁。ISBN 4-00-011041-1。
- ^ “Potassium Metal 98.50% Purity”. Galliumsource.com. 2010年10月16日閲覧。
- ^ “004 – Potassium Metal”. Mcssl.com. 2010年10月16日閲覧。
- ^ Abdelwahab, M.; Youssef, S.; Aly, A.; Elfiki, S.; Elenany, N.; Abbas, M. (1992). “A simple calibration of a whole-body counter for the measurement of total body potassium in humans”. International Journal of Radiation Applications and Instrumentation. Part A. Applied Radiation and Isotopes 43 (10): 1285-1289. doi:10.1016/0883-2889(92)90208-V.
- ^ Chang, Raymond (2007). Chemistry. Boston: McGraw-Hill Higher Education. p. 52. ISBN 9780071105958 2011年5月29日閲覧。
- ^ Campbell, Neil (1987). Biology. Menlo Park: Benjamin/Cummings. p. 795. ISBN 0-8053-1840-2
- ^ Lockless, S. W.; Zhou, M.; MacKinnon, R. (2007). “Structural and thermodynamic properties of selective ion binding in a K+ channel”. PLoS Biol 5 (5): e121. PMID 17472437.
- ^ Schonwald, Seth (2004). “Potassium Chloride and Potassium Permanganate”. Medical toxicology. Philadelphia: Lippincott Williams & Wilkins. pp. pp. 903-905. ISBN 9780781728454
- ^ Marfy, Claire; Cardello, A. V.; Brand, Joseph G. (1981). “Tastes of Fifteen Halide Salts Following Water and NaCl: Anion and Cation Effects”. Physiology & Behavior 26: 1083-1095.
- ^ 橋本壽夫 (2008年10月25日). “塩・話・解・題 43 ハロゲン化合物の味と安全性”. たばこ塩産業新聞 塩事業版 (JTクリエイティブサービス) 2011年8月25日閲覧。
- ^ a b c d 「日本人の食事摂取基準」策定検討会: “日本人の食事摂取基準”. 厚生労働省. pp. 252-255 (2016年). 2018年5月1日閲覧。
- ^ “Potassium Food Charts”. Asia Pacific Journal of Clinical Nutrition. 2011年5月18日閲覧。
- ^ Grim, C. E.; Luft, F. C.; Miller, J. Z.; Meneely, G. R.; Battarbee, H. D.; Hames, C. G.; Dahl, L. K. (1980). “Racial differences in blood pressure in Evans County, Georgia: relationship to sodium and potassium intake and plasma renin activity”. Journal of Chronicle Diseases 33 (2): 87-94. doi:10.1016/0021-9681(80)90032-6. PMID 6986391.
- ^ Karger, S. (2004). “Energy and nutrient intake in the European Union” (PDF). Annals of Nutrition and Metabolism 48 (2 (suppl)): 1-16. doi:10.1159/000083041.
- ^ D'Elia, L.; Barba, G.; Cappuccio, F.; Strazzullo, P. (2011). “Potassium Intake, Stroke, and Cardiovascular Disease: A Meta-Analysis of Prospective Studies”. The Journal of the American College of Cardiology 57 (10): 1210-1219. doi:10.1016/j.jacc.2010.09.070.
- ^ Folis, R. H. (1942). “Myocardial Necrosis in Rats on a Potassium Low Diet Prevented by Thiamine Deficiency”. Bulletin of the Johns-Hopkins Hospital 71: 235.
- ^ Committee on Optimization of Nutrient Composition of Military Rations for Short-Term, High-Stress Situations; Committee on Military Nutrition Research (2006). Nutrient composition of rations for short-term, high-intensity combat operations. Washington, D.C.: National Academies Press. pp. pp. 287 ff. ISBN 9780309096416 2011年5月29日閲覧。
- ^ Shallenberger, R. S. (1993). Taste chemistry. London: Blackie Academic & Professional. pp. pp. 120 ff. ISBN 9780751401509 2011年5月29日閲覧。
- ^ 中屋豊『よくわかる栄養学の基本としくみ』秀和システム、2009年、167頁頁。ISBN 9784798022871。
- ^ 嶋津孝、下田妙子『臨床栄養学 疾病編』(第2版)化学同人〈エキスパート管理栄養士養成シリーズ〉、2010年、159頁。ISBN 4759812296。
- ^ Slonim, Anthony D.; Pollack, Murray M. (2006). “Potassium”. Pediatric critical care medicine. Philadelphia, PA: Lippincott Williams & Wilkins. p. 812. ISBN 9780781794695
- ^ Visveswaran, Kasi (2009). “hypokalemia”. Essentials of Nephrology (2nd ed. ed.). New Delhi: BI Publications. p. 257. ISBN 9788172253233
- ^ a b c 岐阜県街路樹等整備・管理の手引き 岐阜県建設研究センター、岐阜県造園緑化協会、2022年4月23日閲覧。
- ^ “年報 平成20年”. 経済産業省生産動態統計. 2011年6月10日閲覧。
- ^ a b c d Greenwood (1997) p.73
- ^ 千谷 (1959) 108頁。
- ^ 足立、岩倉、馬場 (2004) 52頁。
- ^ Roy, Amit H. (2007). “Fertilizers and Food Production”. In Kent, James A.. Kent and Riegel's handbook of industrial chemistry and biotechnology. 1. New York: Springer. pp. pp. 1111-1157. ISBN 9780387278438
- ^ “施肥量決定の考え方、方法等”. 三重県中央農業改良普及センター. p. 78. 2011年6月29日閲覧。
- ^ “Potassium Content of Selected Foods per Common Measure, sorted by nutrient content”. USDA National Nutrient Database for Standard Reference, Release 20
- ^ Figoni, Paula I. (2010). “Bleaching and Maturing Agents”. How Baking Works: Exploring the Fundamentals of Baking Science. Hoboken: John Wiley & Sons. p. 86. ISBN 9780470392676
- ^ Chichester, C. O. (1986). “Uses and Exposure to Sulfites in Food”. Advances in Food Research. 30. Orlando: Academic Press. pp. pp. 4-6. ISBN 9780120164301
- ^ Kearey, Philip; Brooks, M.; Hill, Ian (2002). “Optical Pumped Magnetometer”. An introduction to geophysical exploration. Oxford: Blackwell Science. p. 164. ISBN 9780632049295
- ^ Werner, R. C.; Jackson, C. B. (1957). “Chapter 18. The Manufacture of Potassium and NaK”. Advances in Chemistry. 19. pp. pp. 169-173. doi:10.1021/ba-1957-0019.ch018. ISBN 9780841200203 ISBN 9780841221666.
- ^ Greenwood (1997) p. 76.
- ^ Siegel, Richard S. (1940). “Ignition of the safety match”. Journal of Chemical Education 17 (11): 515. doi:10.1021/ed017p515.
- ^ Toedt, John; Koza, Darrell; Cleef-Toedt, Kathleen Van (2005). “Personal Cleansing Products: Bar Soap”. Chemical Composition of Everyday Products. Westport: Greenwood Press. ISBN 9780313325793
- ^ 千谷 (1959) 114頁。
- ^ 職業能力開発総合大学校能力開発研究センター 編『めっき科電気めっき作業法-2級技能士コース』職業訓練教材研究会、2005年、223頁。ISBN 4786330043。
- ^ 加藤俊二『身の回りを化学の目で見れば』化学同人、1986年、162頁。ISBN 4759801553。
- ^ Greenwood (1997) p.74
- ^ Marx, Robert F. (1990). The History of Underwater Exploration. New York: Dover Publications. ISBN 9780486264875
- ^ Gettens, Rutherford John; Stout, George Leslie (1966). Painting Materials: A Short Encyclopaedia. New York: Dover Publications. pp. pp. 109-110. ISBN 9780486215976
- ^ 櫻井、鈴木、中尾 (2003) 128頁。
- ^ コットン、ウィルキンソン (1987) 264頁。
- ^ ショアー、ボルハルト (2004) 359-361頁。
- ^ ショアー、ボルハルト (2004) 360頁。
- ^ 薬事日報社 編『医薬部外品原料規格-2006追補』薬事日報社、2009年、16頁。ISBN 4840811016。
- ^ 厚生労働省 編『食品衛生検査指針 理化学編 2005』日本食品衛生協会、2005年、76-77頁。ISBN 4889250034。
- ^ 萩中淳『分析科学』化学同人、2007年、294頁。ISBN 4759812520。
- ^ 本浄高治『基礎分析化学』化学同人、1998年、80-82頁。ISBN 4759808205。
- ^ Bowen, Robert (1988). “Theory and Assumptions in Potassium-Argon Dating”. Isotopes in the Earth Sciences. London: Chapman & Hall. pp. pp. 203-208. ISBN 9780412537103
- ^ A temperature below absolute zero Max Plank Gesellscaft
- ^ Purefoy, Christian (2010年11月26日). “Nigeria's 500-year-old dye tradition under threat”. CNN 2011年10月1日閲覧。
- ^ Marggraf, Andreas Siegmund (1761). Chymischer Schriften. Berlin: Bey Arnold Wever. p. 167
- ^ du Monceau, H. L. D. (1736). “Sur la Base de Sel Marine” (French). Memoires de l'Academie royale des Sciences: 65-68.
- ^ Enghag, P. (2004). “11. Sodium and Potassium”. Encyclopedia of the Elements. Weinheim: Wiley-VCH. ISBN 3527306668
- ^ Davy (1808) pp. 1–44.
- ^ a b Shaposhnik, V. A. (2007). “History of the discovery of potassium and sodium (on the 200th anniversary of the discovery of potassium and sodium)”. Journal of Analytical Chemistry 62 (11): 1100-1102. doi:10.1134/S1061934807110160.
- ^ Weeks, Mary Elvira (1932). “The discovery of the elements. XI. Some elements isolated with the aid of potassium and sodium: Zirconium, titanium, cerium, and thorium”. Journal of Chemical Education 9 (7): 1231. doi:10.1021/ed009p1231.
- ^ Siegfried, R. (1963). “The Discovery of Potassium and Sodium, and the Problem of the Chemical Elements”. Isis 54 (2): 247-258. doi:10.1086/349704. JSTOR 228541.
- ^ Browne, C. A. (1926). “Historical notes upon the domestic potash industry in early colonial and later times”. Journal of Chemical Education 3 (7): 749. doi:10.1021/ed003p749.
- ^ “石鹸の歴史”. 石鹸百科. 生活と科学社 (2009年). 2011年9月29日閲覧。
- ^ Liebig, Justus von (1840). Die organische Chemie in ihrer Anwendung auf Agricultur und Physiologie. Braunschweig: Vieweg
- ^ Cordel, Oskar (1868). Die Staßfurter Kalisalze in der Landwirthschaft. Aschersleben, Germany: L. Schnock
- ^ Birnbaum, Karl (1869). Die Kalidüngung in ihren Vortheilen und Gefahren. Berlin: Wiegandt & Hempe
- ^ United Nations Industrial Development Organization; Int'l Fertilizer Development Center (1998). Fertilizer Manual. Dordrecht, The Netherlands: Kluwer Academic Publishers. pp. pp. 46 ff, 417 ff. ISBN 9780792350323
- ^ Miller, H. (1980). “Potash from Wood Ashes: Frontier Technology in Canada and the United States”. Technology and Culture 21 (2): 187-208. doi:10.2307/3103338. JSTOR 3103338.
- ^ Rittenhouse, P. A. (1979). “Potash and politics”. Economic Geology 74 (2): 353-357. doi:10.2113/gsecongeo.74.2.353.
- ^ “消防法(昭和二十三年法律第百八十六号)”. e-Gov法令検索. 総務省行政管理局 (2018年6月27日). 2020年2月10日閲覧。 “2019年7月1日施行分”
- ^ “毒物及び劇物取締法(昭和二十五年法律第三百三号)”. e-Gov法令検索. 総務省行政管理局 (2018年6月27日). 2020年2月10日閲覧。 “2016年4月1日施行分”
- ^ “Alkali Metals Sodium, Potassium, NaK, and Lithium”. DOE Handbook. Washington, D.C.: U.S. Department of Energy (1994年). 2010年10月16日閲覧。
- ^ Wray, Thomas K. (1992年). “Danger: peroxidazable chemicals”. Environmental Health & Public Safety (North Carolina State University). 2011年5月16日閲覧。
カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/01/03 09:14 UTC 版)
カリウムは細胞内の主要なイオンで、体内のカリウム量は1.6から1.9g /kg体重程度である。体内のカリウムの90%は細胞内にあり、細胞内では60~100 mEq/L、血清では3.6~4.8 mEq/Lと、細胞内外で大きな濃度差がある。カリウムの細胞内外の移動により血清カリウムは大きく変動する。 カリウムは、細胞内浸透圧の維持、膜電位の維持、神経興奮伝達、心興奮伝導の調整、筋収縮、酸塩基平衡の調節、などに関与する。 カリウム値の異常は、日常、よく遭遇する電解質異常である。
※この「カリウム」の解説は、「電解質異常」の解説の一部です。
「カリウム」を含む「電解質異常」の記事については、「電解質異常」の概要を参照ください。
カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/04/25 14:32 UTC 版)
血液中のナトリウムイオンの増加を防ぎ、高血圧などに良い。可食部100gあたり140mg。
※この「カリウム」の解説は、「ナシ」の解説の一部です。
「カリウム」を含む「ナシ」の記事については、「ナシ」の概要を参照ください。
カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/06/13 04:33 UTC 版)
農業ではカリ(加里)と省略している。主に根の発育と細胞内の浸透圧調整に関係するため、根肥(ねごえ)といわれる。水溶性のため流亡しやすいので、追肥で小出しに与えるのがよい。細胞内ではイオンの形で存在するため、細胞が死ぬと細胞外へ流出しやすい。また、植物体内での転流も容易。
※この「カリウム」の解説は、「肥料」の解説の一部です。
「カリウム」を含む「肥料」の記事については、「肥料」の概要を参照ください。
カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/07/03 05:45 UTC 版)
カリウムは、根の発育と細胞内の浸透圧調節に必須であるため根肥(ねごえ)といわれ、根菜類では他の植物以上に必要である。また、葉や生長点においても重要である。 主に肥料として利用されるものは、硫酸カリウム(硫酸カリ)と塩化カリウム(塩化カリ)由来のもので、カリ岩塩として採掘されたものを精製したものが利用される。
※この「カリウム」の解説は、「肥料の三要素」の解説の一部です。
「カリウム」を含む「肥料の三要素」の記事については、「肥料の三要素」の概要を参照ください。
カリウム
出典:『Wiktionary』 (2021/06/12 13:13 UTC 版)
名詞
カリウム
翻訳
- アイスランド語: kalín (is)
- アイルランド語: potaisiam (ga)
- アフリカーンス語: kalium (af)
- アラビア語: بُوتَاسيُوم (ar) (butásyum) 男性
- アルバニア語: kalium (sq)
- アルメニア語: կալիում (hy) (kalium)
- イタリア語: potassio (it) 男性
- インターリングア: potassium (ia), kalium (ia)
- インドネシア語: kalium (id)
- ウェールズ語: potasiwm (cy)
- ウクライナ語: калій (uk) (kálij) 男性
- ウズベク語: калий (uz) (kalii)
- 英語: potassium (en)
- エストニア語: kaalium (et)
- エスペラント: kalio (eo)
- オランダ語: kalium (nl) 中性, potas (nl) 女性
- カザフ語: калий (kk) (kálii)
- カシューブ語: kali
- カタルーニャ語: potassi (ca)
- ガリシア語: potasio (gl) 男性
- ギリシア語: κάλιον (el) (kálion) 中性
- グルジア語: კალიუმი (ka) (kaliumi)
- クロアチア語: kalij (hr)
- コーンウォール語: calyum (kw)
- スウェーデン語: kalium (sv) 中性
- スコットランド・ゲール語: potaisiam (gd)
- スペイン語: potasio (es) 男性
- スロヴァキア語: draslík (sk)
- スロヴェニア語: kalij (sl)
- セルビア語: калијум (sr) (kalijum) 男性
- タイ語: โพแทสเซียม (th) (phōthaetsiam)
- タジク語: kali'
- タミル語: வெடியம் (ta) (vediyam)
- チェコ語: draslík (cs)
- 中国語: 鉀 (zh) (jiǎ)
- 広東語: 鉀 (gaap3)
- 朝鮮語: 칼륨 (ko) (kallyum)
- デンマーク語: kalium (da)
- ドイツ語: Kalium (de) 中性
- トルコ語: potasyum (tr)
- ノルウェー語: kalium (no)
- バスク語: potasioa
- ハンガリー語: kálium (hu)
- フィンランド語: kalium (fi)
- フェロー語: kalium (fo)
- フランス語: potassium
- フランス語: potassium (fr) 男性
- フリウリ語: potassi
- 西フリジア語: kalium (fy)
- ブルガリア語: калий (bg) (kálij) 男性
- ブルトン語: potasiom (br), kaliom (br) 男性
- ベトナム語: kali (vi)
- ヘブライ語: אשלגן (he) (ashlegán) 男性
- ベラルーシ語: калій (be) (kálij) 男性
- ペルシア語: پتاسيم (fa) (potâsim)
- ポーランド語: potas (pl) 男性
- ボスニア語: kalij (bs)
- ポルトガル語: potássio (pt) 男性
- マケドニア語: калиум (mk) (kálium) 男性
- マルタ語: potassju (mt)
- マレー語: kalium (ms)
- マン島語: potashum (gv)
- モンゴル語: кали (mn) (kali)
- ラテン語: kalium (la) 中性
- ラトヴィア語: kālijs (lv)
- リトアニア語: kalis (lt)
- ルーマニア語: potasiu (ro) 中性, kaliu (ro) 中性
- ルクセンブルク語: Kalium
- ロシア語: калий (ru) (kálij) 男性
「 カリウム」の例文・使い方・用例・文例
- カリウムは9個のリン化物を持つ。
- 高濃度水酸化カリウム水溶液
- 過マンガン酸カリウム.
- 土は、切に炭酸カリウムを必要とした
- 岩石試料と崩壊生成物、アルゴンの放射性カリウムの割合を頼りに地質学的年代を定めること
- (他の用途以外に)アストリンゼントとして用いられるアルミとカリウムの二重硫酸塩
- ニトログリセリンが木材パルプの基とナトリウムまたは硝酸カリウムにおいて吸収されるダイナマイトのタイプ
- 亜鉛の陽極、酸化水銀の陰極、水酸化カリウムの電解質からなる初歩的な電池
- 水酸化カリウムの電解質がある酸化ニッケル陰極と鉄の陽極がある蓄電池
- 英国の化学者で、電気化学の先駆者であり、要素ナトリウム、カリウム、バリウム、ホウ素、カルシウム、マグネシウム、および塩素を分離するのにそれを使用した(1778年−1829年)
- 英国の生理学者で、アンドリュー・ハックスレーとともに、神経インパルスの伝達でのカリウムとナトリウム原子の役割を発見した(1914年−1998年)
- イギリスの生理学者で、アラン・ホジキンと共に神経刺激の伝達におけるカリウム・イオンとナトリウム・イオンの役割を発見した(1917年生まれ)
- それを中性化するために、ミリグラムで計測される水酸化カリウムのような脂肪に存在する遊離酸量
- 健康と正常な身体の機能に不可欠な、電解質(カルシウム、ナトリウム、カリウムなど)量の均衡
- 循環血液の中で通常の水準のカリウムよりも高い
- 衰弱と心臓異常に繋がる循環血液中のカリウムの異常低濃度
- 循環する血液中の過剰なカリウムの存在
- 尿の中の過剰なカリウムの存在
- 動物性組織に対して等浸透圧のナトリウム、カリウム、カルシウムの塩化物を含んでいる水溶液
- 2倍のアルミニウムの硫酸塩の白色結晶性:カリウム、アルミニウムの2倍の硫酸塩
カリウムと同じ種類の言葉
- カリウムのページへのリンク