cycle
「cycle」の意味
「cycle」とは、一連の出来事や状況が繰り返し起こること、またはその繰り返しの過程を指す。自然界や社会現象など、さまざまな分野で用いられる。例えば、水循環や昼夜のサイクル、経済の景気循環などが該当する。「cycle」の発音・読み方
「cycle」の発音は、IPA表記では /ˈsaɪkəl/ であり、カタカナ表記では「サイクル」となる。日本人が発音する際のカタカナ英語では「サイクル」と読むことが一般的である。「cycle」の定義を英語で解説
A cycle is defined as a series of events or situations that recur in a regular or predictable pattern. It can be applied to various fields, such as natural phenomena, social events, and economic trends. Examples include the water cycle, day-night cycle, and economic business cycle.「cycle」の類語
「cycle」の類語には、""circle"", ""rotation"", ""revolution"", ""recurrence"", ""periodicity"" などがある。これらの単語は、それぞれ独自のニュアンスや用途があるが、繰り返しや循環の概念を表す点で共通している。「cycle」に関連する用語・表現
「cycle」に関連する用語や表現には、""life cycle"", ""vicious cycle"", ""virtuous cycle"", ""menstrual cycle"", ""sleep cycle"" などがある。これらは、それぞれ特定の分野や状況における繰り返しや循環を指している。「cycle」の例文
1. The water cycle is an essential process for the Earth's ecosystem.(水循環は地球の生態系にとって不可欠なプロセスである。) 2. The economy goes through cycles of growth and recession.(経済は成長と不況のサイクルを繰り返す。) 3. The life cycle of a butterfly consists of four stages: egg, larva, pupa, and adult.(チョウの生活史は、卵、幼虫、さなぎ、成虫の4つの段階からなる。) 4. The menstrual cycle is a regular biological process in women.(月経周期は女性における定期的な生物学的プロセスである。) 5. A good sleep cycle is important for maintaining overall health.(良い睡眠サイクルは全体的な健康維持に重要である。) 6. The vicious cycle of poverty and crime is a major social issue.(貧困と犯罪の悪循環は、重要な社会問題である。) 7. The virtuous cycle of education and economic development benefits society.(教育と経済発展の良い循環は社会に利益をもたらす。) 8. The rotation cycle of the Earth around the Sun is approximately 365.25 days.(地球が太陽の周りを回る周期は約365.25日である。) 9. The carbon cycle plays a crucial role in regulating the Earth's climate.(炭素循環は地球の気候を調節する上で重要な役割を果たす。) 10. The agricultural cycle includes planting, growing, harvesting, and resting periods.(農業サイクルには、植え付け、成長、収穫、休閑期が含まれる。)サイクル【cycle】
サイクル
ある状態から出発していろいろの変化を経たあと、再び最初の状態にもどることを繰り返すとき、このような状態変化をサイクルという。ピストン機関のサイクル論においては、燃焼による熱量の供給の状態によって、(1)容積一定のもとで行われるとした定容サイクル(オットーサイクル)、(2)圧力一定のもとで行われるとした定圧サイクル(ディーゼルサイクル)、(3)一部が定容のもとで残りが定圧のもとで行われるとした複合サイクル(サバテサイクル)に分けられる。実際のエンジンでは火花点火機関が定容サイクルに近く、低速の圧縮着火機関は定圧サイクルに、高速の圧縮着火機関は複合サイクルに近似している。
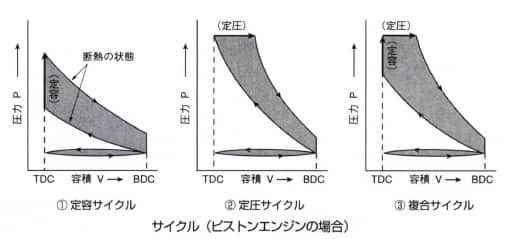
サイクル cycle
プロシアジン
| 分子式: | C10H13ClN6 |
| その他の名称: | プロシアジン、シクレ【除草剤】、CGA-18762、Procyazine、Cycle【herbicide】、シクル、サイクル、Cycle、2-[(4-Chloro-6-cyclopropylamino-1,3,5-triazin-2-yl)amino]-2-methylpropanenitrile、2-[[4-Chloro-6-(cyclopropylamino)-1,3,5-triazin-2-yl]amino]-2-methylpropanenitrile |
| 体系名: | 2-[[4-クロロ-6-(シクロプロピルアミノ)-1,3,5-トリアジン-2-イル]アミノ]-2-メチルプロパンニトリル、2-[(4-クロロ-6-シクロプロピルアミノ-1,3,5-トリアジン-2-イル)アミノ]-2-メチルプロパンニトリル |
サイクル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/05/12 05:32 UTC 版)
サイクル (英: cycle) とは、状態が続けて変化し、再び最初の状態に戻ること。
- サイクル (単位) - 周波数や回数などの単位。
- 熱力学サイクル
- レシプロエンジンの回転。
- 航空機の飛行回数 - 1回の離陸定格出力から停止までを含むエンジンの連続運転を伴った飛行回数。その時点までのサイクルは総サイクル数。
- サイクル (グラフ理論)
- チェイン複体の d の核
- 自転車 (bicycle)
- その他
- サイクル安打 - 英語のHitting for the cycleの和訳。
- サイクル (競輪) - 東京都、神奈川県の競輪場で発行されている競輪予想紙。
- サイクル (cutman-boocheの曲) - cutman-booche のアルバムMy Wayのリード曲。
- CYCLE (CHERRYBLOSSOMの曲) - CHERRYBLOSSOM の 3rdシングル。
- CYCLE (バンド) - 日本のロックバンド。
- CYCLE - 旧サイクルスタイル。日本のウェブサイト。
サイクル (単位)
(サイクル から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/01/22 15:20 UTC 版)
| サイクルまたはサイクル毎秒 | |
|---|---|
| 記号 | c,∼,c/s, (cps) |
| 系 | 非SI単位、非法定計量単位(1997年10月1日以降) |
| 量 | 周波数 |
| SI | 1 Hz |
| 定義 | 1秒に1周期 |
| サイクル毎ミリメートル | |
|---|---|
| 記号 | c/mm, c |
| 度量衡 | メートル法 |
| 系 | 非SI単位、非法定計量単位 |
| 量 | 空間周波数・線数 |
| SI | 1 /mm = 1000 /m |
| 定義 | 1mmに1周期 |
サイクル (cycle) またはサイクル毎秒 (cycle per second) は、周波数の単位である。1997年10月1日以降は計量法上の非法定計量単位であり、取引・証明に用いることは禁止されている[1]。
本来は、波や振動など周期的な現象の回数を数える単位であり、無次元量として単位なしで表す。いくつかの派生単位を、単にサイクルと称する場合もある。
サイクルまたはサイクル毎秒

1000kC(=キロサイクル)と表記されている
サイクルとサイクル毎秒は、物象の状態の量である周波数の単位としては、同一の計量単位である[2]。
サイクルとサイクル毎秒は、1948年の第9回国際度量衡総会で提案され1960年の第11回国際度量衡総会で正式に決定されたヘルツ (Hz) に置き換えられた。1 ヘルツ = 1 サイクル = 1 サイクル毎秒 である。このことから、日本の計量法では、1997年10月1日以降は、取引・証明における使用が禁止された。
単位記号は「c、∼又はc/s」と規定されている[3]が、「cps」や「⏦」も用いられた。cpsはカウント毎秒、キャラクター毎秒の記号としても用いられることがある。
サイクル毎分 (c/min, cpm)、サイクル毎時 (c/h, cph) もあったが、同じく非SI単位かつ非法定計量単位である。文脈によっては、これらを単にサイクルと称する場合がある。
1997年9月30日までは、派生単位として次の4単位と記号が認められていた[3]が。計量法上はSI接頭語が付加された単位としての位置づけではなかった。これらの4単位の記号としては、「∼」を用いることはできない。
- キロサイクル又はキロサイクル毎秒(kc又はkc/s)= キロヘルツ
- メガサイクル又はメガサイクル毎秒(Mc又はMc/s)= メガヘルツ
- ギガサイクル又はギガサイクル毎秒(Gs又はGc/s)= ギガヘルツ
- テラサイクル又はテラサイクル毎秒(Tc又はTc/s)= テラヘルツ
俗な用法としてギガヘルツで動作する電子回路のはしりの時期に、キロメガサイクルの語が見られた[4]。
サイクル毎ミリメートル
空間周波数の単位として、サイクル毎ミリメートルを単にサイクルと称することがある。SIでは毎ミリメートル (/mm, mm−1) で表す。
注
- ^ 新計量法とSI化の進め方-重力単位系から国際単位系(SI)へ- 通商産業省 SI単位等普及推進委員会、p.11、1999年3月発行
- ^ 計量法附則第三条の計量単位等を定める政令 別表第2、項番2、計量単位の欄に「サイクル又はサイクル毎秒」とある。
- ^ a b 計量法附則第三条の計量単位の記号等を定める規則 別表、周波数の欄
- ^ https://cir.nii.ac.jp/crid/1572261552042804992
サイクル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2021/08/28 03:31 UTC 版)
次の各過程が準静的(可逆的)に行われるものとする。 1-2 断熱圧縮 2-3 温度 T H {\displaystyle T_{\mathrm {H} }} で Q H {\displaystyle Q_{\mathrm {H} }} の熱を等温吸熱、膨張 3-4 断熱膨張 4-1 温度 T L {\displaystyle T_{\mathrm {L} }} で Q L {\displaystyle Q_{\mathrm {L} }} の熱を等温放熱、圧縮
※この「サイクル」の解説は、「カルノーサイクル」の解説の一部です。
「サイクル」を含む「カルノーサイクル」の記事については、「カルノーサイクル」の概要を参照ください。
サイクル
「サイクル」の例文・使い方・用例・文例
- 市議会は提出されていた水リサイクル計画を否決した
- リサイクルするほうが環境にはやさしい
- 彼が樹脂複合材料のリサイクル技術を確立する
- 会社がリサイクルの費用を負担します
- 空いたペットボトルは必ずリサイクルボックスへ入れてください。
- 多くの仏教徒は出生、苦しみ、死、および再生の無限のサイクルを信じている。
- 路面のくぼみは主に凍結融解サイクルのためにできる。
- 我々はPDCAサイクルを活用して、業務を継続的に改善しています。
- プロダクトライフサイクルの考え方を考慮した上で次の戦略を決めなさい。
- 典型的なマネジメントサイクルとしてPDCA (計画・実行・検証・改善)が有名です。
- そろそろその商品のライフサイクルエクステンション戦略を練らなければ。
- ライフサイクルコストの観点からこの車にしたんだ。
- ビジネスサイクルの中で、企業は景気後退局面への抜かりのない準備を怠ってはならない。
- 最も短い景気サイクルの一つがキチンサイクルである。
- ステープル商品とは、定番商品の事で、長い期間にわたって販売されるサイクル寿命の長い商品をいいます。
- 利益を増幅するためには、営業サイクルを短縮する必要がある。
- 日本は大衆消費社会からリサイクルを基本とする持続可能社会に変わるべきである。
- このサイクルはずっと続いている。
- サイクルの最小の温度
- 40秒毎の完璧なサイクル
- サイクルのページへのリンク