リシン
猛毒として知られるタンパク質の一種。唐胡麻の種子から抽出できる。致死量は150マイクログラム。
リシンを大量に含む飲食物を摂取したり、静脈などに注入されたりすると、消化器・循環器をはじめ複数の臓器が炎症を起こし、壊死するに至る。
日本救急医学会はリシンを「容易かつ安価に生成でき、毒性が高く、エアロゾルとして安定で、特異的治療法やワクチンがない」ため「生物兵器」として捉えることができる、としている。実際、ヒマシ油を生産した際に生じる屑から大量のリシンを得ることができる。
米国ではリシンを利用した殺人および殺人未遂事件がたびたび発生している。2013年4月16日にも、共和党の上院議員ロジャー・ウィッカーに宛てて送られた封書から、事前検査の過程でリシンが検出されている。
リシン【lysine】
リシン【ricin】
り‐しん【離心】
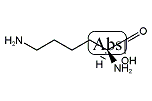
D‐リシン
| 分子式: | C6H14N2O2 |
| その他の名称: | (-)-リシン、(-)-リジン、D-Lysine、(-)-Lysine、(-)-D-Lysine、(2R)-2,6-Diaminohexanoic acid、(R)-2,6-Diaminohexanoic acid |
| 体系名: | (2R)-2,6-ジアミノヘキサン酸、(R)-2,6-ジアミノヘキサン酸、(-)-D-リシン、D-リシン |
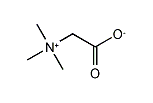
ベタイン
| 分子式: | C5H11NO2 |
| その他の名称: | ベタイン、Betaine、Trimethylammonioacetate、α-Carboxylato-N,N,N-trimethylmethanaminium、Trimethylglycine、グリココールベタイン、α-アールレイン、Rubrine C、Loramine AMB-13、Abromine、Glycylbetaine、Trimethylglycocoll、Oxyneurine、Lycine、α-Earleine、Glycocoll betaine、ロラミンAMB-13、Glycine betaine、ルブリンC、アブロミン、グリシルベタイン、トリメチルグリココール、オキシニューリン、オキシノイリン、グリシンベタイン、リシン【ベタイン】、2-Oxo-2-oxylato-N,N,N-trimethylethanaminium、N,N,N-Trimethyl-2-oxylato-2-oxoethanaminium、トリメチルグリシン、(Trimethylaminio)acetic acid anion、Lycine【betaine】、(Trimethylaminio)acetate、Carboxylatomethyltrimethylammonium、2-(Trimethylaminio)acetic acid anion、N,N,N-Trimethylaminioacetate、Carboxylatomethyltrimethylaminium、(2-Oxo-2-oxylatoethyl)trimethylaminium |
| 体系名: | 2-(トリメチルアミニオ)酢酸アニオン、N,N-ジメチル-N-(カルボキシラトメチル)メタンアミニウム、トリメチルアミニオアセタート、N,N,N-トリメチルアミニオアセタート、カルボキシラトメチルトリメチルアミニウム、カルボキシラト-N,N,N-トリメチルメタンアミニウム、N,N,N-トリメチルカルボキシラトメタンアミニウム、(カルボキシラトメチル)トリメチルアミニウム、N,N-ジメチル-N-カルボキシラトメチルメタンアミニウム、α-カルボキシラト-N,N,N-トリメチルメタンアミニウム、2-オキソ-2-オキシラト-N,N,N-トリメチルエタンアミニウム、N,N,N-トリメチル-2-オキシラト-2-オキソエタンアミニウム、(トリメチルアミニオ)酢酸アニオン、(トリメチルアミニオ)アセタート、カルボキシラトメチルトリメチルアンモニウム、(2-オキソ-2-オキシラトエチル)トリメチルアミニウム |
リジン
| 分子式: | C6H14N2O2 |
| その他の名称: | (+)-リジン、L-Lysine、(+)-Lysine、(+)-L-Lysine、L-リジン、リシン、Lysine、リジン、L-2,6-ジアミノカプロン酸、L-2,6-Diaminocaproic acid、(+)-S-リシン、(+)-S-Lysine、(S)-リシン、(S)-Lysine、α-リシン、α-Lysine、アミヌトリン、Aminutrin、リシン酸、Lysine acid、マランジル、Malandil、(2S)-2-Amino-6-aminohexanoic acid、(2S)-2,6-Diaminohexanoic acid、(S)-2,6-Diaminohexanoic acid |
| 体系名: | (2S)-2,6-ジアミノヘキサン酸、L-Lys-OH、(S)-2,6-ジアミノヘキサン酸、(+)-L-リシン、L-リシン、(2S)-2-アミノ-6-アミノヘキサン酸 |
リシン
リシン
リシン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/06/13 03:45 UTC 版)
| リシン | |
|---|---|
 |
 |
|
Lysine |
|
|
別称
2,6-diaminohexanoic acid
|
|
| 識別情報 | |
| CAS登録番号 | 70-54-2, 56-87-1 L, 923-27-3 D |
| PubChem | 866 |
| ChemSpider | 843  5747 L |
| KEGG | C16440  C00047(L体) |
| ChEMBL | CHEMBL28328  |
| 724 | |
|
|
|
|
| 特性 | |
| 化学式 | C6H14N2O2 |
| モル質量 | 146.19 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
リシン(英: lysine)は、α-アミノ酸のひとつで側鎖に 4-アミノブチル基を持つ。リジンと表記あるいは音読する場合もある。 タンパク質構成アミノ酸で、必須アミノ酸である。略号は Lys あるいは K である。側鎖にアミノ基を持つことから、塩基性アミノ酸に分類される。リシンは、クエン酸回路に取り込まれてエネルギーを生み出すケト原性アミノ酸である。
栄養学
必須アミノ酸であるが、植物性蛋白質における含量が低く、動物性蛋白質摂取量の少ない地域での栄養学上の大きな問題となっている。3大穀物である米、小麦、トウモロコシなど穀類のリシン含有量が少ないので、リシンを豊富に含む副食(肉、魚、乳製品、豆、そば粉など)を必要とする[1]。サプリメントとしてヘルペスの予防にも利用される。
WHOによるリシンの成人向け一日当たり推奨摂取量は2.1グラムである[2]。
穀物中には豊富には含まれないが、豆類には豊富である。肉、魚、乳製品にも多く含まれる。多量のリシンを含む植物には以下のようなものがある。
- バッファロー・ゴーアド(Buffalo Gourd, ウリ科の植物)の種 - 10,130–33,000 ppm
- クレソン(オランダガラシ) - 1,340–26,800 ppm
- ダイズの種 - 24,290–26,560 ppm
- イナゴマメの種 - 26,320 ppm
- インゲンマメの芽 - 2,390–25,700 ppm
- モリンガの芽 - 5,370–25,165 ppm
- レンズマメの芽 - 27,120–23,735 ppm
- シカクマメの種 - 21,360–23,304 ppm
- アカザの種 - 3,540–22,550 ppm
- レンズマメの種 - 19,570–22,035 ppm
- ルピナスの種 - 19,330–21,585 ppm
- キャラウェイの種 - 16,200–20,700 ppm
- ホウレンソウ - 1,740–20,664 ppm
生化学
リシンは蛋白質分子に対してメチル化やアセチル化による翻訳後修飾を行う。コラーゲンはリシンの誘導体であるヒドロキシリシンを含む。細胞から分泌が行われる際に、小胞体またはゴルジ体におけるリシン残基のO-グリコシル化が特定の蛋白質に印を付けるのに使われる。
代謝
リシンには複数の代謝経路が存在するが、哺乳類では主に肝臓ミトコンドリア内で行われるサッカロピンを中間体とした経路で代謝される[3][4]。この経路は植物、動物、細菌で報告されており、リシン-ケトグルタル酸レダクターゼ/サッカロピンデヒドロゲナーゼ(LKR/SDH)およびα-アミノアジピン酸セミアルデヒドデヒドロゲナーゼ(AASADH)によって触媒される3つの酵素反応によって、リシンがα-アミノアジピン酸に変換される[5]。α-アミノアジピン酸はその後も代謝されていき、最終的にアセチルCoAやアセト酢酸になる。

植物においては前述のサッカロピンを経由する代謝経路の他、カダベリンを経由する経路、ピペコリン酸を経由する経路の3つの代謝経路が報告されている[5]。一部のマメ科の植物はリシン脱炭酸酵素の働きによってリシンからカダベリンを生成し、これをキノリジジンアルカロイドを生合成するための前駆体として用いる[6]。ピペコリン酸を経由する経路では、リシンはAGD2-like defense response protein 1(ALD1)によってα-アミノ基転移を受け、Δ1-piperideine-2-carboxylateを経てピペコリン酸になる[7]。この経路は植物内で微生物病原体の攻撃を受けると活性化され、植物の免疫において中心的な役割を果たす[7]。
また、一部の細菌においては、リシンはカダベリンを経由する経路で代謝されることが報告されている[8][9]。
生合成
リシンの生合成はアスパラギン酸→β-アスパルチルリン酸→アスパラギン酸セミアルデヒド→ジアミノピメリン酸の順に行われる。カビ類においては、α-ジアミノピメリン酸を経由する。

脚注
- ^ 「リシン【lysine】」『漢方薬・生薬・栄養成分がわかる事典』講談社
- ^ FAO/WHO/UNU (2007年). “PROTEIN AND AMINO ACID REQUIREMENTS IN HUMAN NUTRITION” (PDF). WHO Press p. 2009年12月3日閲覧。, page 150
- ^ “Metabolite of the Weekリジン”. ヒューマン・メタボローム・テクノロジーズ株式会社 (2022年12月12日). 2023年11月29日閲覧。
- ^ João Leandro, Sander M Houten (2019-02-04). “Saccharopine, a lysine degradation intermediate, is a mitochondrial toxin”. J Cell Biol. 218 (2). doi:10.1083/jcb.201901033..
- ^ a b Paulo Arruda, Pedro Barreto (2020-03-21). “Lysine Catabolism Through the Saccharopine Pathway: Enzymes and Intermediates Involved in Plant Responses to Abiotic and Biotic Stress”. Front Plant Sci. 11 (587). doi:10.3389/fpls.2020.00587..
- ^ Amy L. Jancewicz, Nicole M. Gibbs, Patrick H. Masson (2016-06-21). “Cadaverine’s Functional Role in Plant Development and Environmental Response”. Front Plant Sci. 7 (870). doi:10.3389/fpls.2016.00870..
- ^ a b Michael Hartmann, Jürgen Zeier (2018-07-23). “l-lysine metabolism to N-hydroxypipecolic acid: an integral immune-activating pathway in plants”. the plant journal 96 (1). doi:10.1111/tpj.14037.
- ^ J C Fothergill, J R Guest (1977-03). “Catabolism of L-lysine by Pseudomonas aeruginosa”. J Gen Microbiol. 99 (1). doi:10.1099/00221287-99-1-139..
- ^ Sebastian Knorr, Malte Sinn, Dmitry Galetskiy, Rhys M. Williams, Changhao Wang, Nicolai Müller, Olga Mayans, David Schleheck, Jörg S. Hartig (2018-11-29). “Widespread bacterial lysine degradation proceeding via glutarate and L-2-hydroxyglutarate”. JNature Communications 9 (1). doi:10.1038/s41467-018-07563-6..
関連項目
外部リンク
- リシン(リジン) - 素材情報データベース<有効性情報>(国立健康・栄養研究所)
「リシン」の例文・使い方・用例・文例
固有名詞の分類
- (-)-リシンのページへのリンク