グリシン【glycine】
グリシン
グリシン
グリシン
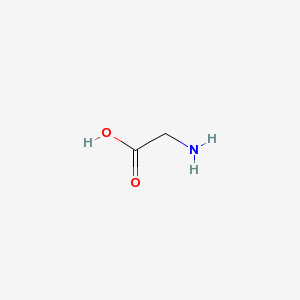
側鎖がなく、光学異性(L-,D-)もない最も単純なアミノ酸。語源はその甘みから。さまざまな生合成経路で現れ、たとえば、ヘモグロビンの補因子であるポルフィリン環はグリシンとスクシニルCoAから生合成される。
非必須アミノ酸。ゼラチンや絹フィブロインに含まれており、治療用の栄養剤としても用いられる。また、速い神経伝達抑制物質でもある。

CC Attribution-Noncommercial-Share Alike 3.0 Unported
グリシン
グリシン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/12/23 11:53 UTC 版)
| グリシン[1] | |
|---|---|
 |
 |
 |
 |
|
Glycine |
|
|
別称
Aminoethanoic acid
Aminoacetic acid |
|
| 識別情報 | |
| 略称 | Gly, G |
| CAS登録番号 | 56-40-6  |
| PubChem | 750 |
| ChemSpider | 730  |
| UNII | TE7660XO1C  |
| EC番号 | 200-272-2 |
| E番号 | E640 (調味料) |
| KEGG | C00037  |
| ChEMBL | CHEMBL773  |
| 727 | |
|
|
|
|
| 特性 | |
| 化学式 | C2H5NO2 |
| モル質量 | 75.07 g mol−1 |
| 示性式 | H2NCH2COOH |
| 外観 | 白色の固体 |
| 密度 | 1.1607 g/cm3 |
| 融点 | 233 °C (分解) |
| 水への溶解度 | 25 g/100 mL |
| 溶解度 | エタノール、ピリジンに可溶。エーテルには不溶。 |
| 酸解離定数 pKa | 2.34 (カルボキシル基), 9.6 (アミノ基)[2] |
| 危険性 | |
| 半数致死量 LD50 | 2600 mg/kg (マウス;経口) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |


グリシン(英: glycine)とは、2-アミノ酢酸の事であり、地球生物のDNAに規定されている20種類のアミノ酸の中の1つでもある。アミノ酸の構造の側鎖が –H で不斉炭素を持たないため、生体を構成する α-アミノ酸の中では唯一、 D-, L- の立体異性体が無い。非極性側鎖アミノ酸に分類される。
多くの種類のタンパク質ではグリシンはわずかしか含まれていないが、ゼラチンやエラスチンといった、動物性タンパク質のうちコラーゲンと呼ばれるものに多く(全体の3分の1くらい)含まれる。
1820年にフランス人化学者アンリ・ブラコノーによりゼラチンから単離された。 甘かったことからギリシャ語で甘いを意味する glykys に因んで glycocoll と名付けられ、後に glycine に改名された。
生合成・代謝
グリシンは糖原性アミノ酸の1つである。
グリシン開裂系はテトラヒドロ葉酸により以下の反応でグリシンを開裂する[3]。
- テトラヒドロ葉酸 + グリシン + NAD+ = 5,10-メチレンテトラヒドロ葉酸+ NH3 + CO2 + NADH + H+
グリシン開裂系とは別に、グリシンヒドロキシメチルトランスフェラーゼ(セリンヒドロキシメチルトランスフェラーゼ)(EC 2.1.2.1)の働きにより、可逆的にグリシンをL-セリンに相互に変換し、5,10-メチレンテトラヒドロ葉酸をテトラヒドロ葉酸に変換する反応が触媒される[4][5]。
- 5,10-メチレンテトラヒドロ葉酸+ グリシン + H2O = テトラヒドロ葉酸 + L-セリン [6]
グリシン開裂系とセリンヒドロキシメチルトランスフェラーゼによる2つの反応を複合すると以下の反応式が示される。また、その全容は図の通りである。
-
2 グリシン

| 脂肪族 | |
|---|---|
| 芳香族 | |
| 極性なし | |
| 正電荷 (pKa) | |
| 負電荷 (pKa) |
「グリシン」の例文・使い方・用例・文例
固有名詞の分類
- グリシンのページへのリンク