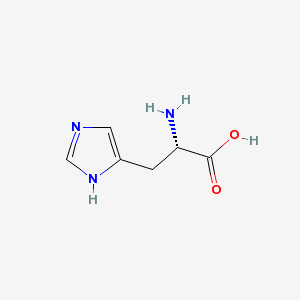
ヒスチジン
| 分子式: | C6H9N3O2 |
| その他の名称: | (-)-ヒスチジン、グリオキサリン-5-アラニン、L-Histidine、(-)-Histidine、(-)-L-Histidine、Glyoxaline-5-alanine、(S)-2-Amino-3-(4-imidazolyl)propionic acid、Histidine、3-(3H-Imidazole-4-yl)alanine |
| 体系名: | (S)-α-アミノ-1H-イミダゾール-4-プロパン酸、L-His-OH、ヒスチジン、(S)-2-アミノ-3-(1H-イミダゾール-4-イル)プロピオン酸、(S)-2-アミノ-3-(4-イミダゾリル)プロピオン酸、(-)-L-ヒスチジン、L-ヒスチジン、3-(3H-イミダゾール-4-イル)アラニン |
D‐ヒスチジン
ヒスチジン
ヒスチジン
Histidine, His, H
側鎖にイミダゾール基を持つ塩基性アミノ酸。必須アミノ酸。イミダゾール基は酵素反応において基質の中間体を安定化させたり、金属イオンの配位子となって酵素の活性部位で重要な役割を果たすことが多い。ヒスタミンの前駆体である。

CC Attribution-Noncommercial-Share Alike 3.0 Unported
ヒスチジン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/02/14 09:52 UTC 版)
|
|
| L-ヒスチジン | |
|---|---|
 |
 |
|
Histidine |
|
|
別称
2-Amino-3-(1H-imidazol-4-yl)propanoic acid
|
|
| 識別情報 | |
| CAS登録番号 | 71-00-1  |
| PubChem | 773 |
| ChemSpider | 6038  |
| UNII | 4QD397987E  |
| DrugBank | DB00117 |
| KEGG | D00032  |
| ChEBI | |
| ChEMBL | CHEMBL17962  |
| 3310 | |
|
|
|
|
| 特性 | |
| 化学式 | C6H9N3O2 |
| モル質量 | 155.15 g mol−1 |
| 水への溶解度 | 4.19g/100g @ 25 °C [1] |
| 危険性 | |
| 安全データシート | データページを参照する |
| NFPA 704 | |
| 関連する物質 | |
| 関連する官能基 | イミダゾール基 |
| 関連物質 | ウロカニン酸 ホルムイミノグルタミン酸 イミダゾールジペプチド |
| 補足データページ | |
| 構造および特性 | n, εr, etc. |
| 熱力学的データ | 相挙動 固体、液体、気体 |
| スペクトルデータ | UV, IR, NMR, MS |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ヒスチジン (histidine) はアミノ酸の一種で2-アミノ-3-(1H-イミダゾール-4-イル)プロピオン酸のこと。略号は His あるいは H。名前はギリシャ語で「組織」という意味。
塩基性アミノ酸の一種で、必須アミノ酸。糖原性を持つ。側鎖にイミダゾリル基という複素芳香環を持ち、この部分の特殊な性質により酵素の活性中心や、蛋白質分子内でのプロトン移動に関与している。蛋白質中では金属との結合部位となり、あるいは水素結合やイオン結合を介してその高次構造の維持に重要な役割を果たしている。
1896年に、ドイツの医学博士アルブレヒト・コッセルとSven Gustaf Hedinによって単離された[2]。
必須アミノ酸
当初、乳幼児にのみ必須なアミノ酸と考えられていたが、1975年に大人も必要とする必須アミノ酸であるという根拠が出された[3]。1985年に、国際連合食糧農業機関(FAO)、世界保健機関(WHO)、国際連合大学(UNU)が発表した基準アミノ酸をもとに、必須アミノ酸として扱われるようになった[4]。
イミダゾリル基
窒素原子に結合したプロトン (H+) の着脱を起こし、塩基または非常に弱い酸として働く。また、二重結合の位置と水素原子が移動した互変異性体が平衡状態にある。いずれの構造の場合でも、水素原子を持たない側の窒素原子が容易に水素原子と反応し、同時に他方の窒素原子上にある水素原子を放出する。結果として、水素原子を運ぶ担体として機能することができる。

炭酸脱水酵素中では活性中心の亜鉛に結合した水分子からプロトンを引き抜いて活性型を再生させ、触媒三残基においてはセリン、トレオニン、システインからプロトンを引き抜き、それらを求核剤として活性化させる役割を果たす。
合成法
フルクトースとホルマリンとアンモニアからヒドロキシメチルイミダゾールを作り、この塩化物にアセトアミドマロン酸エステルを縮合して作る。
安全性
ヒトにて1日4.5グラムまでの投与で副作用は報告されていない。1日24-64グラムではいくつかの副作用が報告されている[5]。
ヒスチジンは青魚に多く含まれる傾向にあり、青魚が死んでから時間が経つと魚肉に含まれる酵素によりヒスタミンに変化するため、スコンブロイド食中毒(ヒスタミン食中毒)の原因になることが有る。
脚注
- ^ http://prowl.rockefeller.edu/aainfo/solub.htm[要文献特定詳細情報]
- ^ Vickery, Hubert Bradford; Leavenworth, Charles S. (1928-08-01). “On the Separation of Histidine and Arginine” (英語). Journal of Biological Chemistry 78 (3): 627–635. doi:10.1016/S0021-9258(18)83967-9. ISSN 0021-9258.
- ^ Kopple, J D; Swendseid, M E (1975-05-01). “Evidence that histidine is an essential amino acid in normal and chronically uremic man.” (英語). Journal of Clinical Investigation 55 (5): 881–891. doi:10.1172/JCI108016. ISSN 0021-9738.
- ^ 対象外物質 評価書ヒスチジン 食品安全委員会
- ^ “The Nature of Human Hazards Associated with Excessive Intake of Amino Acids”. The Journal of Nutrition 134 (6): pp.1633S–1639S,HISTIDINE. (2004). doi:10.1093/jn/134.6.1633S.
関連項目
- 金属タンパク質
- Hisタグ
- ヒスタミン
- ヒスチジン血症
- カルノシン血症 ‐β-アラニンとヒスチジンから成るジペプチドであるカルノシンの過剰症
- パウリ反応(パウリ比色定量法) - タンパク質中のヒスチジンの存在を可視化する方法。スルファニル酸と反応し赤色となる。
外部リンク
- ヒスチジン - 素材情報データベース<有効性情報>(国立健康・栄養研究所)
「ヒスチジン」の例文・使い方・用例・文例
- ヒスチジンのページへのリンク