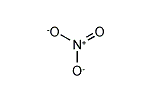
硝酸イオン
硝酸塩
(硝酸イオン から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/07/13 07:18 UTC 版)


無機化学において、硝酸塩(しょうさんえん、英: nitrate)は、1個の窒素原子と3個の酸素原子からなる硝酸イオン NO3− を持つ塩である。食物、特に野菜から得られる硝酸塩は消化器で亜硝酸塩に変換され、魚に多い2級アミンと反応し、ラットなどの小動物実験では発がん性をもつニトロソアミンを生成するという(硝酸態窒素、亜硝酸塩も参照のこと)。しかし人間が対象の臨床試験や医学論文などでは発がんに関わるという有意なデータが出ておらず、国連食糧農業機関(FAO)と世界保健機関(WHO)が合同で運営する、添加物、汚染物質について科学的データに基づくリスク評価を行っているFAO/WHO合同食品添加物専門家会議(JECFA)は、硝酸塩の摂取と発がんリスクとの間に関連があるという証拠にはならないという見解を発表した。
有機化学では、硝酸とアルコールが脱水縮合してできたNO3基を持つ化合物(例:硝酸メチル)は硝酸塩とは呼ばず、硝酸エステルと呼ぶ。英語では硝酸塩も硝酸エステルも nitrate である。
性質
硝酸イオンは化学式 NO3− によって表される分子イオンで、分子量は62.00である。硝酸の共役塩基であり、1個の窒素原子と、それをとりまく3個の等価な酸素原子が平面三角形を構成している。N−O結合距離はほぼ125pmである。全体として1価の負電荷を帯びており、各酸素原子はそれぞれ −2/3、窒素原子は +1 の形式電荷を持つ。共鳴構造の例として取り上げられるように、負電荷は3個の酸素原子上に等しく分散している。
ほとんどすべての硝酸塩は標準状態において水に溶ける。これはハロゲン化物 MX の場合、電離によりそれぞれ単原子イオン M+、X− を生じ、回転による自由度を失うのに伴いエントロピーが減少するため比較的電離しにくく、陽イオンの種類によっては溶解度が小さいのに対し、硝酸塩MNO3では電離したときの自由度の減少が小さく、電離しやすいためである[1]。
水棲生物への影響
地面に近接する淡水域および三角江では硝酸塩濃度の上昇が起こることがあり、これは魚の死の原因となる。硝酸塩はアンモニアや亜硝酸塩よりは毒性が低い[2]ものの、濃度が30ppmに達すると成長の阻害や免疫系の阻害を起こすことがあり、水棲生物に悪影響を及ぼす。たいていの場合、硝酸塩濃度の上昇は、主に農地あるいは過剰な硝酸塩肥料が残留する地域からの表面流出によって起こる。高濃度の硝酸塩は藻類の増殖をも引き起こす。カリウムやリン酸塩、硝酸塩などの栄養素が増加すると富栄養化の原因となる。これは低酸素状態の原因ともなり、生態系においてある種の生物がほかのものより圧倒的に増殖する現象の引き金となる。これらのことから、硝酸塩は全蒸発残留物を構成する成分のひとつに含まれ、水質を表す指標として広く用いられる。
硝酸塩は水の浄化の際の副生物であり、動物やヒトの排泄物が分解されたあとに生成する。水質は水源によって影響を受ける。腐敗物は地上の水源や帯水層を経て水源の近辺へ流入する。このため、雨水以外を主な水源とする湖などは、そのような過程による硝酸塩濃度の増加が起こることがある。
主な硝酸塩
硝酸塩鉱物
鉱物学において、硝酸塩からなる鉱物を硝酸塩鉱物(しょうさんえんこうぶつ、英: nitrate mineral)という。硝石(KNO3)、チリ硝石(NaNO3)などがある。
一般的に、日本では湿度が高い事から硝酸塩鉱物は存在しないと考えられていたが、一部では産出記録が存在する(チリ硝石の項を参照)。
脚注
- ^ 篠田耕三『溶液と溶解度 : 機能性溶液・組織体溶液』(第3版)丸善、1991年。ISBN 4-621-03600-9。
- ^ Romano, N.; Zeng, C. (2007). "Acute toxicity of sodium nitrate, potassium nitrate and potassium chloride and their effects on the hemolymph composition and gill structure of early juvenile blue swimmer crabs (Portunus pelagicus, Linneaus 1758) (Decapoda, Brachyura, Portunidae)." Environmental Toxicology and Chemistry 26: 1955−1962.
関連項目
硝酸イオン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/05/05 08:11 UTC 版)
硝酸イオン(しょうさんイオン、NO3−, nitrate)は硝酸およびその化合物の電離、分解によって主に生じる1価の陰イオン、窒素化合物であり、硝酸塩中にも存在し、平面正三角形型構造で N−O 結合距離は硝酸三水和物中において 124.7 – 126.5 pm である。 硝酸は強い酸化剤であり、多くの金属と反応するため多種の塩を生成する。また一般に、金属の硝酸塩は水に溶解しやすい。 希薄水溶液中における標準酸化還元電位は以下の通りである。 NO 3 − ( aq ) + 2 H + ( aq ) + 2 e − = NO 2 − ( aq ) + H 2 O ( l ) , {\displaystyle {\ce {NO3^{-}(aq){}+2H^{+}(aq){}+2{\mathit {e}}^{-}\ =\ NO2^{-}(aq){}+H2O(l),}}} E ∘ = 0.832 V {\displaystyle E^{\circ }=0.832~\mathrm {V} } NO 3 − ( aq ) + 10 H + ( aq ) + 8 e − = NH 4 + ( aq ) + 3 H 2 O ( l ) , {\displaystyle {\ce {NO3^{-}(aq){}+10H^{+}(aq){}+8{\mathit {e}}^{-}\ =\ NH4^{+}(aq){}+3H2O(l),}}} E ∘ = 0.883 V {\displaystyle E^{\circ }=0.883~\mathrm {V} } 硝酸イオンは白金電極を用いた水溶液の電解により陰極でアンモニアまで還元される。
※この「硝酸イオン」の解説は、「硝酸」の解説の一部です。
「硝酸イオン」を含む「硝酸」の記事については、「硝酸」の概要を参照ください。
硝酸イオンと同じ種類の言葉
- 硝酸イオンのページへのリンク