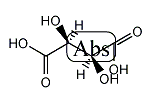
D‐酒石酸
| 分子式: | C4H6O6 |
| その他の名称: | D-酒石酸、(-)-酒石酸、D-Tartaric acid、(-)-Tartaric acid、(-)-D-Tartaric acid、(2S,3S)-(-)-Tartaric acid、(D)-(-)-酒石酸、(2S,3S)-(-)-酒石酸、D-(-)-2,3-ジヒドロキシこはく酸、D-(-)-Tartaric acid、(2S,3S)-Tartaric acid、D-(-)-2,3-Dihydroxysuccinic acid |
| 体系名: | (2S,3S)-2,3-ジヒドロキシこはく酸、(2S,3S)-2,3-ジヒドロキシブタン二酸、(-)-D-酒石酸、(2S,3S)-酒石酸 |
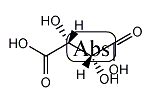
L‐酒石酸
| 分子式: | C4H6O6 |
| その他の名称: | トレアル酸、(+)-酒石酸、Threaric acid、(+)-Tartaric acid、L-Tartaric acid、[2R,3R,(+)]-2,3-Dihydroxybutanedioic acid、(+)-L-Tartaric acid、L-(+)-酒石酸、d-酒石酸、L(+)-酒石酸、L(+)-Tartaric acid、(2R,3R)-Tartaric acid、(R,R)-酒石酸、(R,R)-Tartaric acid、(2R,3R)-(+)-酒石酸、(2R,3R)-(+)-Tartaric acid、L-2,3-ジヒドロキシこはく酸、L-2,3-Dihydroxysuccinic acid、L-(+)-Tartaric acid、E-334、NSC-62778、d-Tartaric acid |
| 体系名: | (2R,3R)-2,3-ジヒドロキシこはく酸、(2R,3R)-2,3-ジヒドロキシブタン二酸、L-酒石酸、[2R,3R,(+)]-2,3-ジヒドロキシブタン二酸、(+)-L-酒石酸、(2R,3R)-酒石酸 |
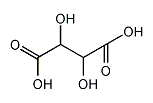
酒石酸
酒石酸
不斉炭素原子を2個持つ有機酸。カリウム塩はワイン製造時に樽の中にl-型の塩として結晶化するが、人工合成した酒石酸を用いるとラセミ体が生じる。光学異性が結晶型に反映される例として有名。COOH-CHOH-CHOH-COOH
| 化合物名や化合物に関係する事項: | 過マンガン酸カリウム 過酸化脂質 遮断抗体 酒石酸 酒石酸ナトリウムカリウム 酢酸オルセイン 酢酸カーミン |
酒石酸
酒石酸
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2023/11/08 14:20 UTC 版)
| 酒石酸 | |
|---|---|
 |
|
| 一般情報 | |
| IUPAC名 | 2,3-ジヒドロキシブタン二酸 |
| 分子式 | C4H6O6 |
| 示性式 | (CH(OH)COOH)2 |
| 分子量 | 150.09 |
| 形状 | 無色固体 |
| CAS登録番号 | [147-71-7](D体) [87-69-4](L体) [133-37-9](ラセミ体) [147-73-9](メソ体) [526-83-0](立体不定) |
| SMILES | C(C(C(=O)O)O)(C(=O)O)O |
| 性質 | |
| 水への溶解度 | 20.6g/100mL(20°C、ラセミ体) |
| 融点 | 168–170 °C(L体、D体) 151°C(メソ体) 206°C(ラセミ体) |
| 比旋光度 [α]D | +12.0(L体、c=20、水中、20°C) |
| 出典 | ICSC(ラセミ体) |
酒石酸(しゅせきさん Tartaric acid)は酸味のある果実、特に葡萄、ワインに多く含まれる有機化合物で、ヒドロキシ酸である。IUPAC命名法では 2,3-ジヒドロキシブタン二酸(2,3-dihydroxy butanedioic acid)となる。ワインの樽にたまる沈殿(酒石、tartar)から、カリウム塩(酒石酸水素カリウム)として発見されたためこの名がある。常温常圧で無色の固体。極性溶媒によく溶ける。水への溶解は、L体、D体、メソ体はよく溶けるが、ラセミ体は比較的溶けにくい。英語のTartaric acidからタルタル酸とも呼ばれる。
不斉炭素

酒石酸は2つの不斉炭素を持つため、L-(+)-酒石酸(2R,3R)、D-(−)-酒石酸(2S,3S)、メソ酒石酸(2R,3S)の3種類の異性体が存在する。フランスのルイ・パスツールがラセミ体(DL体)の酒石酸塩(酒石酸ナトリウムアンモニウム)を、その結晶の形をもとに光学分割することに成功し、光学異性体の概念を史上初めて示したことで知られる。天然に比較的多く存在するのはL体である。メソ酒石酸は天然には存在せず、キラリティを持たない。また、ラセミ体はブドウ酸と呼ばれる。
用途
酒石酸は食品添加物としての使用が認められており、ベーキングパウダーや酸味料などとして食品に添加される。医薬においては水溶性を改善するため、酒石酸の塩として供給されているものがある。有機合成化学の分野では光学分割剤として用いられるほか、誘導体が不斉触媒などとして使われている(酒石酸ジエチルを用いるシャープレス酸化が有名)。
相撲部屋ではちゃんこに使うポン酢は市販のものを買うのではなく、酒石酸を湯に溶かし、それを醤油に混ぜ、香りづけに柑橘類を絞ったものを入れることがある[1][2]。
「疲労を回復する」、「整腸作用がある」などといわれているが、ヒトでの有効性・安全性については科学的に信頼できる十分なデータがない[3]。ラットを用いた実験では、リン・カルシウムの腸管からの吸収を阻害するというデータが得られている[4]。
出典
- ^ 北の富士勝昭、嵐山光三郎『大放談!大相撲打ちあけ話』(新講舎、2016年)p192
- ^ 鳴戸俊英『親方はちゃんこ番』(ポプラ社、2003年)p138
- ^ 酒石酸 - 素材情報データベース<有効性情報>(国立健康・栄養研究所)
- ^ 小川竜平、真鍋厚史、中山貞男、小口勝司. “カルシウムとリンの吸収ならびに実験的骨粗鬆症に対するシュウ酸、酒石酸の影響”. 昭和医学会雑誌 54 (2): 118-127. doi:10.14930/jsma1939.54.118.
関連項目
酒石酸
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2021/03/30 08:45 UTC 版)
酒石酸は、ワインの化学的安定性や色に大きく関わり、また最終的な味にも影響を与えるため、最も重要な酸である。大部分の植物では、この有機酸はほとんど含まれないが、ブドウ属にはかなりの濃度で含まれる。酒石酸の含有量は、ブドウの種類や土壌条件等によって異なる。パロミノは含有量が大きく、マルベックやピノ・ノワールは一般的に含有量が小さい。開花期には、花に多くの酒石酸が蓄積し、その後、若い果実に移行する。果実が熟す過程において酒石酸はリンゴ酸と異なり、呼吸等で代謝されず、そのため比較的保存される。 ブドウ中の酒石酸の半分以上は遊離酸ではなく、大部分はカリウム酸塩として存在する。発酵中、これらの酒石酸は発酵かすやパルプ屑、沈殿したタンニンや色素に結合している。ブドウの種類や地域により差異はあるが、一般的に約半分の沈殿物はワインのアルコール混合物に溶ける。これらの酒石酸の結晶化は任意の時間に起こり、ワインボトルが割れたガラスのように見えることがあるが、無害である。ワイン中の酒石酸を結晶化させて沈殿させるために、ワインを凝固点以下の温度に置くこともある。
※この「酒石酸」の解説は、「ワインの酸」の解説の一部です。
「酒石酸」を含む「ワインの酸」の記事については、「ワインの酸」の概要を参照ください。
「酒石酸」の例文・使い方・用例・文例
(-)-酒石酸と同じ種類の言葉
- (-)-酒石酸のページへのリンク