ミトコンドリア‐びょう〔‐ビヤウ〕【ミトコンドリア病】
ミトコンドリア病
ミトコンドリアはエネルギーを産生する細胞内小器官です。ミトコンドリアはよく車のエンジンに例えられます。もしミトコンドリアに異常をきたすと、大量のエネルギーを必要とする骨格筋、中枢神経系にまず異常をきたすのです。ミトコンドリア病はしばしばミトコンドリア脳筋症と呼ばれるのはそのためです。心筋も当然侵されるし、難聴、糖尿病、腎障害などの合併症も多くみられます。ミトコンドリア病の60ー70%は以下に述べるいわゆる3大病型に属します。3大病型以外ではLeigh脳症、チトクロームc酸化酵素欠損が最も多く報告されています。3大病型とLeigh脳症の臨床的まとめを表6に示しました。
| 病 型 | CPEO (慢性進行性外眼筋麻痺) | MELAS (メラス) | MERRF (マーフ) | Leigh脳症 (リー脳症) | |
| 家族歴(母系遺伝) | − | + | + | +(20%のみ) | |
| 発症年齢 | 小児〜70歳 | 2〜15歳 | 小児〜40歳 | 乳児 | |
| 臨 床 症 状 | 低身長 知能低下 筋力低下 感音性難聴 周期性頭痛・嘔吐 皮質盲 片麻痺・半盲 痙攣 ミオクローヌス 小脳失調 外眼筋麻痺 網膜色素変性 心伝導障害 | + −〜± + + − − − − − − [+] [+] [+] | + + + + [+] [+] [+] [+] −* − − − − | + + + + − − − [+] [+] [+] − − − | − + + − − − − + +〜− − − − − |
| 検 査 所 見 | 高乳酸血症 髄液タンパク質上昇 CT異常:脳萎縮 局所性低吸収域,淡蒼球石灰化 | + + − − | + −* + + | + − + − | + − + 脳幹、脳基底核の変化 |
| 筋 生 検 | RRF SSV | + −* | + + | + + | − − |
| 酸素欠損(複合体) | IV>I | I | IV | IV(10%のみ) | |
| mtDNA異常 | 欠失(種々の大きさ) | 点変異(3243,3271) | 点変異(.8344) | 点変異(8933)** | |
| CPEO:chronic progressive external ophthalmoplegia, MELAS:mitochondrial myopathy,encephalopathy,lactic acidosis,and stroke-like episodes, MERRF:myoclonus epilepsy associated with ragged-red fibers, RRF:ragged-red fibers, SSV:strongly SDH-reactive blood vessels, CT:computed tomography, mtDNA:mitochondrial DNA *:まれに+,**:患者の約20%のみ,[ ]:重要な鑑別点 | |||||
| 表6:ミトコンドリア病の3大病型とLeigh脳症の特徴 | |||||
(1)病因、病態、病理
表6に示したように3大病型にはそれぞれ疾患特異的なミトコンドリアDNA(mtDNA)変異をみます。またLeigh脳症の約20ー30%もmtDNAの変異によることが知られています。チトクロームc酸化酵素欠損の一部は核遺伝子の変異によることが明らかにされています。それはチトクロームc酸化酵素の合成に関係する遺伝子、SURF1遺伝子の変異によるものでした。この病気は核遺伝子の変異ですから、常染色体劣性遺伝をとります。
mtDNAは環状のDNAで、16、569塩基対からなっていて、イントロンはなく全てエクソンからなっています(図30)。われわれの体の細胞のミトコンドリアは全て母親由来であるのでmtDNA変異の主な病気(慢性進行性外眼筋麻痺症候群を除く)は母系遺伝を示します。
 | 斜線部はtRNA コード領域,12S,16SはrRNA コード領域. ND:複合体� CO:シトクロムcオキシダーゼ(複合体�) ATP:ATP合成酵素 cyt b:シトクロムbのコード領域 CPEOの矢印はこの範囲内でいろいろな長さの欠失を見る。 外側:重鎖, 内側:軽鎖 |
| 図30:ミトコンドリアDNA(mtDNA)と主な疾患の変異 | |
ミトコンドリア病の大半は骨格筋が侵されるので、骨格筋細胞のミトコンドリアに形態学的な異常をみます。筋線維内のミトコンドリアは巨大化し、その数も増加します。増加したミトコンドリアはGomoriトリクローム変法という染色で赤染し、すこしボロボロした感じを与えるので。赤色ぼろ線維(ragged-red fiber: RRF)とよばれています(図31)。
 | 赤色ぼろ線維。 ゴモリトリクローム変法染色という簡単な染色で、正常筋(左:N)では赤い顆粒状のミトコンドリアはほとんど見えない。ミトコンドリア病(右:Mit Dis)では筋線維の大小不同と赤く染まる筋線維(赤いのは全て異常に増加したミトコンドリア)がみられる。多くの場合、この赤色ぼろ線維があるとミトコンドリア病と診断できる。 |
| 図31:赤色ぼろ線維 |
電子顕微鏡で見るとミトコンドリアは巨大化し、複雑に増殖したクリステ(cristae)をもち、しばしば類格子様封入体(paracrystalline inclusion)をもっています。
(2)症状
☆慢性進行性外眼筋麻痺症候群(chronic progressive external ophthalmoplegia: CPEO)
本疾患の約70ー80%の患者さんにミトコンドリアDNA(mtDNA)の欠失をみます。欠失とは遺伝子の一部が欠けていて、遺伝子が短くなっていることです。欠失の部位は個人によって異なり、一定ではありません。ごくまれに優性遺伝をみますが、大半(95%以上)は突然変異によるもので遺伝性はありません。
発症は小児期から成人までと幅広く、10ー20歳に気付かれることが最も多いのです。まず眼瞼下垂(上まぶたがさがること)で気付かれます。病初期は片方のみのこともありますが、早晩両側性の眼瞼下垂となります。眼球運動制限もあり、進行すると全方向への運動が制限されます。眼症状のみのものもいますが、大半は易疲労性とか四肢の筋力低下も伴います。眼症状、網膜色素変性、心伝導障害を伴うものはKearns-Sayre syndrome (KSS)とよばれています。Kerns とSayreはこの病気をみつけた人の名前です。この病気では難聴、低身長、髄液の蛋白増加をよく認めます。また幼少時では知的退行をしばしば伴います。
血清乳酸値の上昇、筋生検で赤色ぼろ線維(ragged-red fiber)の存在の確認、チトクロームc酸化酵素染色で酵素活性が欠損した線維があること(部分欠損)で、診断が確定します。骨格筋内のmtDNAには変異がみられますが、血液から分離したものにはみられません。すなわち、本症は血液では遺伝子診断は出来ず、筋生検が必要です。
治療法には特別なものはありません。コエンザイムQ製剤(ノイキノン)の多めの投与で効果がある人がいます。目が下がってものが見ずらい方には、二重瞼を作るアイプッチというのが化粧品屋さんにあります。いちど試されてはいかがですか。
☆.メラス(mitochondrial myopathy, encephalopathy, lactic acidosis and stroke-like episodes:MELASは神経学用語集では、「ミトコンドリア脳筋症・乳酸アシドーシス・脳卒中様症候群」と訳されていますが、一般にはメラスと呼ばれています)
脳卒中様症状を主症状とする疾患で、母系遺伝(母から子どもへの遺伝)をとります。mtDNAの転移(t)RNALeu(UUR)のコード領域にある3、243番目のA→G変異(3243変異)をとるものが80%、3271番目のT→C変異が10%です。
本症は母系遺伝をとるので、母親、同胞の多くは変異をもっています。しかし変異mtDNAをもっていても、無症状なものから、非特異的症状(筋力低下、易疲労性、低身長、糖尿病など)のみ、典型的メラス症状を示すものまでと幅があります。病理学的に血管(小動脈)の異常がある(血管平滑筋に異常ミトコンドリアが増加している)ことから、血管系の異常が本症の発症に大きく関与していると考えられています。
成人発症もありますが、多くは小児期に最初の脳卒中に似た症状が出現します。患者さんの80%は15歳までに第1回目のエピソードを経験します。脳卒中様症状が出現する前から、低身長、易疲労、軽度の筋力低下をみることが多いとされています。脳卒中様症状は嘔吐を伴う発作性の頭痛、痙攣、意識障害で、回復後に片麻痺、視力障害(多くは一過性)を残します。脳卒中様症状は数時間から数日続き、その間は高乳酸血症による代謝性アシドーシスをみます。成人にみられる脳卒中と異なり、麻痺のような症状は一過性で通常は速やかに快復します。
発作症状を繰り返すにつれ、知的退行、てんかん、半盲(時に両側性)、筋力低下が進行し、るいそう、感染、腎不全などでをみることもあります。
血清とくに髄液の乳酸値が正常の2倍以上と高くなります。脳CT/MRIでは多巣性の脳梗塞類似の所見を後頭部優位に認めます(図32)。
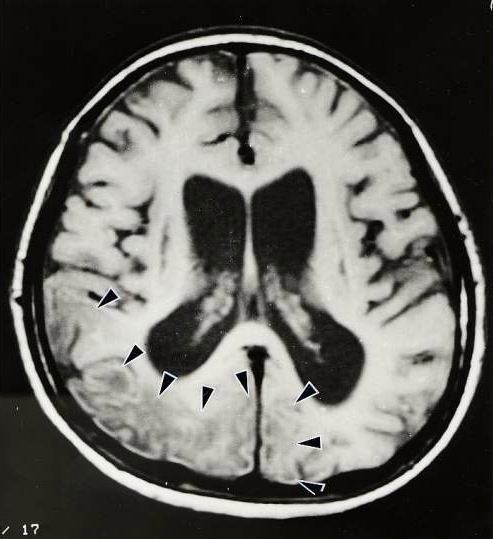 | 後頭部(写真の左下の方で、矢尻印で囲んである部位)は薄くみえる(シグナル強度が低い)。この部は血流が少なく脳梗塞の後の所見に似る。メラスではこのように、後頭葉に病変が強い傾向がある。 病気が進行すると、本症のように脳室の拡大、脳の萎縮が目立つようになる。 |
| 図32:メラスの脳MRI(T1強調画像) | |
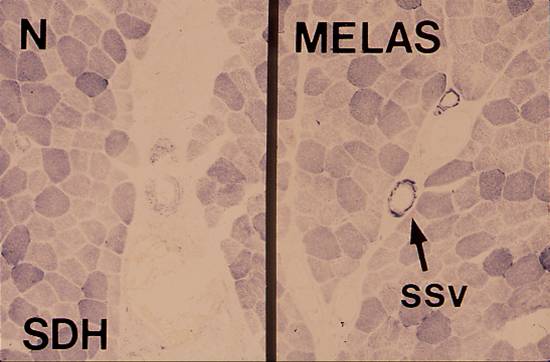 | ミトコンドリアをよく染めるコハク酸脱水素酵素(succinate dehydrogenase: SDH) 染色すると、正常筋(左:N)では血管はほとんど染まらない。 メラス(右:MELAS)では血管壁が強く染まり、異常なミトコンドリアが血管壁に蓄積していることが分かる。 |
| 図33:筋組織内の異常血管(SSV) | |
☆マーフ(myoclonus epilepsy associated with ragged-red fibers:MERRFは神経学用語集では赤色ぼろ線維・ミオクローヌスてんかん症候群と訳されているがマーフと呼ぶのが一般的である。あるいは福原病ともよばれる)
マーフはミオクローヌス、全身性のてんかん発作、小脳性失調を主症状とし母系遺伝をとります。約90%の患者にmtDNAのtRNAlysコード領域の8、344番目のA→G変異がみられ、これは血液から分離したDNAでも証明できます。MELASでみられたように、母や同胞は無症状から典型例までと幅があります。
発症は小児期から成人までと幅広いです。多くはミオクローヌス(筋肉がピクピクと動く現象です)、小脳失調で気付かれます。けいれん発作は全身性の強直、間代性です。多くは発症前から易疲労性が見られます。経過とともに痙攣、筋力低下、知的退行が進行していきます。約40%の患者に心筋症を合併します。
検査では血液、特に髄液の乳酸値の上昇がみられます。筋生検では赤色ぼろ線維、チトクロームc酸化酵素部分欠損、SSVなどが80%以上の患者でみられます。
治療は対症的で、メラスと同じです。バルプロ酸はミトコンドリアのカルニチン代謝に影響するので使用しない方がよいと考えられています。
☆リー(Leigh)脳症(Leigh encephalomyelopathy)
本症は脳基底核、脳幹部に左右対称性の壊死性病変をみる神経病理学的診断名(病理解剖をして、はじめて原因が分かる診断名)でした。しかし、画像診断の進歩により、病変部位が確認できるようになって、臨床診断名となっています。
典型例は乳児期に発症します。発育発達の停止、筋力・筋緊張低下、呼吸障害、知的退行を主症状とします。進行例では筋緊張が亢進することもあります。呼吸不全、るいそうで発症後数年で死の転帰をとることもありますが、中には治療により改善する人もいます。血清、髄液の乳酸値は上昇します。脳CT/MRIで脳基底核や脳幹(脳の中心部にあります)の異常が診断的です(図34)。
| 脳の基底核(線条体)に 左右対称性の壊死病変(→) がみえる。 |  |
| 図34:リー脳症の脳CT像 | |
治療法としては特別なものはありません。ただ、中にはビタミンB1が著効する例がある(B1依存性PDHC欠損など)ので、ビタミンの投与を行います。またアシドーシス(血液の酸性度が強くなる)にはジクロロ酢酸が効果あります。
☆チトクロームc酸化酵素欠損(cytochrome c oxidase: COX deficiency)
ミトコンドリア病には酵素欠損がみいだされ、生化学的な分類での診断名があります。その中で最も多いのがチトクロームc酸化酵素(COX)(複合体IV)欠損です。この酵素欠損でリー脳症にもなります。リー脳症以外の疾患として次の2つの病気が代表的です。
乳児重症型(fatal infantile form)
乳児期から筋力・筋緊張低下、呼吸不全、意識障害、強いアシドーシスを伴い1歳以下で死亡する重症型です。約半数に糖尿、蛋白尿、汎アミノ酸尿(DeToni-Fanconi-Debre症候群)をともないます。
乳児良性型(benign infantile form)
きわめてまれでまだ日本では、10例以下の報告しかありません。症状は乳児期に筋力・筋緊張低下、呼吸不全などで、人工呼吸器が必要なこともあります。1歳過ぎから症状は改善し、多くは全く正常となります。一部は完全には回復しません。中枢神経障害はありません。
上記いずれの疾患も常染色体劣性遺伝と考えられています。筋生検では赤色ぼろ線維をみとめ、COX活性は組織化学的にも生化学的にも低下ないし欠損しています。ただ乳児良性型では酵素の活性は次第に上昇していきます。
☆メンギー(mitochondrial neurogastrointestinal encephalomyopathy: MNGIE)
常染色体劣性伝形式をとるまれな疾患です。通常10代から20代に疾患に気づかれます。最も目立つ症状は、著明な全身のやせと消化器症状(消化管運動不全や下痢)で、他に、眼瞼下垂、末梢神経障害による手足のしびれなどが見られます。筋生検では赤色ぼろ線維、チトクロームc酸化酵素部分欠損など、何らかのミトコンドリア異常の所見が見られます。骨格筋のミトコンドリアDNAを調べると、ミトコンドリアDNAの欠乏(量の減少)や多重欠失と呼ばれる変異が検出できます。
この疾患は、チミジン・ホスフォリラーゼという酵素の欠損で起こります。チミジン・ホスフォリラーゼは、DNAの原料であるチミジンを分解する酵素ですが、この酵素がないために、患者さんの血液中では、チミジンの濃度が通常の60倍程度にまで増加しています。この高濃度のチミジンが、正常なミトコンドリアDNAの合成を妨げているのだと考えられています。
血液中のチミジン濃度とチミジン・ホスフォリラーゼ活性を測定することで、診断を付けることが出来ます。チミジン・ホスフォリラーゼ遺伝子の変異を見いだせば、さらに確実な診断になります。血液10mlで、これら全ての検査を行うことが出来ます。
ミトコンドリア病
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2023/07/29 03:31 UTC 版)
ミトコンドリア病(ミトコンドリアびょう)とは、真核生物の細胞小器官の1つであるミトコンドリアの異常が原因で発症する疾患である。1980年代から脚光を浴びるようになった。ミトコンドリア病によって障害の起き易い場所に因んで、ミトコンドリア脳筋症やミトコンドリアミオパチーとも呼ばれる。ただし、一口にミトコンドリア病と言っても多彩な病態を示すため、病型分類が行われてきた。
注釈
- ^ ミトコンドリアで行う好気的なATP産生は、ミトコンドリア以外で行う嫌気的なATP産生に比べて、圧倒的に効率が良い。ミトコンドリア外で行われる嫌気的な解糖系だけの場合と、ミトコンドリア内でのTCAサイクルと電子伝達系との合計を比較して、グルコース1分子につき、何分子のATPが産生できるかを計算すれば、一目瞭然である。
- ^ チトクロームc酸化酵素欠損症の一部などが、その例である。
- ^ 詳細はMELASの項目を参照。
出典
- ^ “タウリン散98%「大正」における効能・効果追加等の承認取得に関するお知らせ” (html). 大正製薬 (2019年2月21日). 2020年1月2日閲覧。
- ^ 後藤雄一. “21 ミトコンドリア病” (PDF). 2015年12月13日閲覧。
- ^ 佐藤 哲男・仮家 公夫・北田 光一(編集)『医薬品トキシコロジー(改訂第3版)』 p.31 南江堂 2006年4月15日発行 ISBN 4-524-40212-8
- 1 ミトコンドリア病とは
- 2 ミトコンドリア病の概要
- 3 治療法
- 4 脚注
固有名詞の分類
- ミトコンドリア病のページへのリンク
