ベリリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/03/07 01:36 UTC 版)
名称


1798年にルイ=ニコラ・ヴォークランが「グルキニウム(旧元素記号Gl、glucinium)」と名づけた。語源のglykysは、ギリシア語で「甘さ」という言葉を意味する。これは、ベリリウム化合物が甘みを持つことに由来している[2]。
1828年には、マルティン・ハインリヒ・クラプロートが「ベリリウム」と命名した。この名前は緑柱石(beryl、ギリシア語で beryllos)に由来している[3][4]。
歴史
初期の分析において緑柱石とエメラルドは常に類似した成分が検出されており、この物質はケイ酸アルミニウムであると誤って結論づけられていた。鉱物学者であったルネ=ジュスト・アユイはこの2つの結晶が著しい類似点を示すことを発見し、彼はこれを化学的に分析するために化学者であるルイ=ニコラ・ヴォークランに尋ねた。1797年、ヴォークランは緑柱石をアルカリで処理することによって水酸化アルミニウムを溶解させ、アルミニウムからベリリウム酸化物を分離させることに成功した[5]。
1828年にフリードリヒ・ヴェーラー[6]とアントワーヌ・ビュシー[7]がそれぞれ独自に、金属カリウムと塩化ベリリウムを反応させることによるベリリウムの単離に成功した。

ベリリウムの電子殻 ベリリウム原子の電子配置は[He]2s2である。ベリリウムはその原子半径の小ささに対してイオン化エネルギーが大きいため電荷を完全に分離することは難しく、そのためベリリウムの化合物は共有結合性を有している[25]。また、ベリリウムの高い正の電荷密度からも共有結合性を説明できる。ファヤンスの法則によると、イオン結合で、サイズが小さく高い正の電荷を持つ陽イオンは、陰イオンの最外殻電子を引っ張り、(これを分極という。)共有結合性を生じる。ベリリウムイオンはサイズが小さく2+と電荷も高いため、共有結合性を有する[8]。第2周期元素は原子量が大きくなるにしたがってイオン化エネルギーも増大する法則が見られるが、ベリリウムはその法則から外れており、より原子量の大きなホウ素よりもイオン化エネルギーが大きい。これは、ベリリウムの最外殻電子が2s軌道上にあり、ホウ素の最外殻電子は2p軌道上にあることに起因している。2p軌道の電子は内殻に存在するs軌道の電子によって遮蔽効果(有効核電荷も参照)を受けるため、2p軌道に存在する最外殻電子のイオン化エネルギーが低下する。一方で2s軌道の電子は遮蔽効果を受けないため、相対的に2p軌道の電子よりもイオン化エネルギーが大きくなり、これによってベリリウムとホウ素の間でイオン化エネルギーの大きさの逆転が生じる[26]。
ベリリウムの錯体もしくは錯イオンは、たとえばテトラアクアベリリウム(II)イオン(Be[(H2O)4]2+)やテトラハロベリリウム酸イオン(BeX42−)のように、多くの場合4配位を取る[25]。EDTA はほかの配位子よりも優先してベリリウムに配位して八面体形の錯体を形成するため、分析技術にこの性質が利用される。たとえば、ベリリウムのアセチルアセトナト錯体にEDTAを加えると、EDTAがアセチルアセトンよりも優先してベリリウムとの間で錯体を形成してアセチルアセトンが分離するため、ベリリウムを溶媒抽出することができる。このようなEDTAを用いた錯体形成においてはAl3+のようなほかの陽イオンによって悪影響を受けることがある[27]。
化合物

硫酸ベリリウム 硫酸ベリリウムや硝酸ベリリウムのようなベリリウム塩の溶液は
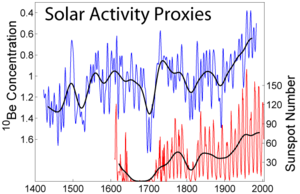
太陽活動の変化による10Be濃度変化のプロット。10Be濃度を示す左側の縦軸は上にいくほど値が小さくなっていることに注意 詳細は「ベリリウムの同位体」を参照ベリリウムの安定同位体は9Beのみであり、したがってベリリウムはモノアイソトピック元素である。9Beは恒星において宇宙線の陽子が炭素などのベリリウムよりも重い元素を崩壊させることによって生成され、超新星爆発によって宇宙中に分散する。このようにして宇宙中にチリやガスとして分散した9Beは、分子雲を形成する原子のひとつとして星形成に寄与し、新しくできた星の構成元素として取り込まれる[33]。
10Beは、地球の大気に含まれる酸素および窒素が宇宙線による核破砕を受けることで生成される。宇宙線による核破砕によって生成したベリリウム同位体の大気中の滞在時間は成層圏で1年程度、対流圏で1か月程度とされており、その後は地表面に蓄積する。10Beはベータ崩壊によって10B になるものの、その136万年という比較的長い半減期のために10Beとして地表面に長期間滞留し続ける。そのため、10Beおよびその娘核種は、自然界における土壌の侵食や形成、ラテライトの発達などを調査するのに利用される[34]。また、太陽の磁気的活動が活発化すると太陽風が増大し、その期間は太陽風の影響によって地球に到達する銀河宇宙線が減少するため、銀河宇宙線によって生成される10Beの生成量は太陽活動の活発さに反比例して減少する。したがって10Beは、同様に宇宙線によって生成される14C(炭素14)とともに太陽活動の変動を記録しているため、極地方のアイスコア中に残された10Beおよび14Cの解析をすることで、過去の太陽活動の変遷を間接的に知ることができる[35]。
核爆発もまた10Beの生成源であり、核爆発によって発生した高速中性子が大気中の二酸化炭素に含まれる13Cと反応することによって生成される。これは、核実験試験場の過去の活動を示す指標のひとつである[36]。
半減期53日の同位体7Beもまた宇宙線によって生成され、その大気中の存在量は10Beと同様に太陽活動と関係している。8Beの半減期はおよそ7×10−17 sと非常に短く、この半減期の短さはベリリウムよりも重い元素がビッグバン原子核合成によっては生成されなかった原因ともなっている[37]。すなわち、8Beの半減期が非常に短いためにビッグバン原子核合成段階の宇宙において核融合反応に利用できる8Beの濃度が非常に低く、そのような低濃度の8Beが4Heと核融合して炭素を合成するにはビッグバン原子核合成段階の時間が不十分であったことに起因する。イギリスの天文学者であるフレッド・ホイルは、8Beおよび12Cのエネルギー準位から、より多くの時間を元素合成に利用することが可能なヘリウムを燃料とする恒星内であれば、いわゆるトリプルアルファ反応と呼ばれる反応によって炭素の生成が可能であることを示し、それによって超新星によって放出される塵とガスから炭素を基礎とした生命の創生が可能となることを明らかにした[38]。
ベリリウムのもっとも内側の電子は化学結合に関与することができるため、7Beの電子捕獲による崩壊は、化学結合に関与することのできる原子軌道から電子を奪うことによって起こる。その崩壊確率はベリリウムの電子構成に大部分を依存しており、核崩壊においてまれなケースである[39]。
既知のベリリウム同位体のうち、もっとも半減期が短いものは中性子放出によって崩壊する13Beであり、その半減期は2.7×10−21 sである。6Beもまた非常に半減期が短く、5.0×10−21 sである[40]。エキゾチック原子核である11Beおよび14Beは、中性子が原子核の周りを周回する中性子ハローを示すことが知られている[41]。この現象は、液滴模型において、古典的なトーマス・フェルミ理論による表面対称エネルギーの影響によって、中性子の分布が陽子分布よりも外部に大きく広がっていると理解することができる[42]。
ベリリウムの不安定な同位体元素は恒星内元素合成においても生成されるが、これらは生成後すぐに崩壊する[43]。
なお、原子番号が偶数で、安定同位体が1つしかない元素はベリリウムだけである[44]。通常、原子番号が20以下の元素においては、ベーテ・ヴァイツゼッカーの質量公式のペアリング項に現われるように、陽子と中性子が偶数であるものは奇数のものと比較して結合エネルギーが大きく安定であるのに加え、対称性項に現われるように陽子数と中性子数が同数のものほどのため安定となるが、陽子数および中性子数がともに4である8Beは例外的に不安定である[45]。これは、8Beの崩壊生成物である4Heが魔法数を取っているため非常に安定であることによる。
- ^ “Webster's Revised Unabridged Dictionary (1913)”. ONLINE Encyclopedia. 2011年10月12日閲覧。
- ^ a b c Weeks, Mary Elvira (1933), “XII. Other Elements Isolated with the Aid of Potassium and Sodium: Beryllium, Boron, Silicon and Aluminium”, The Discovery of the Elements, Easton, PA: Journal of Chemical Education, ISBN 0-7661-3872-0
- ^ 山口 (2007) 58頁。
- ^ a b 村上雅人『元素を知る事典: 先端材料への入門』海鳴社、2004年、68頁。ISBN 487525220X。
- ^ Vauquelin, Louis-Nicolas (1798), “De l'Aiguemarine, ou Béril; et découverie d'une terre nouvelle dans cette pierre”, Annales de Chimie (26): 155-169
- ^ Wöhler, Friedrich (1828), “Ueber das Beryllium und Yttrium”, Annalen der Physik 89 (8): 577-582, Bibcode: 1828AnP....89..577W, doi:10.1002/andp.18280890805
- ^ Bussy, Antoine (1828), “D'une travail qu'il a entrepris sur le glucinium”, Journal de Chimie Medicale (4): 456-457
- ^ a b Muki kagaku.. Rayner-Canham, Geoffrey., Overton, T. (Tina), Nishihara, hiroshi., Takagi, shigeru., Moriyama, hiroshi., 西原, 寛. 東京化学同人. (2009). ISBN 978-4-8079-0684-0. OCLC 1022213386
- ^ Kane, Raymond; Sell, Heinz (2001), “A Review of Early Inorganic Phosphors”, Revolution in lamps: a chronicle of 50 years of progress, p. 98, ISBN 9780881733785
- ^ a b c d e f g h i j Behrens, V. (2003), “11 Beryllium”, in Beiss, P., Landolt-Börnstein - Group VIII Advanced Materials and Technologies: Powder Metallurgy Data. Refractory, Hard and Intermetallic Materials, 2A1, Berlin: Springer, pp. 1-11, doi:10.1007/10689123_36, ISBN 978-3-540-42942-5
- ^ 千谷 (1959) 187頁。
- ^ 千谷 (1959) 198頁。
- ^ 櫻井、鈴木、中尾 (2005) 26頁。
- ^ コットン、ウィルキンソン (1987) 267頁。
- ^ 千谷 (1959) 199頁。
- ^ Lawrence A. Warner et al.. “Occurrence of nonpegmatite beryllium in the United States”. U.S. Geological Survey professional paper (United States Geological Survey) 318: 2.
- ^ a b c d e 千谷 (1959) 193頁。
- ^ 無機化学ハンドブック編集委員会 (1965). 無機化学ハンドブック. 技報堂出版. p. 1229. ISBN 4765500020
- ^ a b 吉田直亮 (1995). “PFC開発における材料損傷研究”. プラズマ・核融合学会誌 (プラズマ・核融合学会) 71 (5) 2012年1月25日閲覧。.
- ^ “ベリリウム反射体要素欠陥評価法に関する検討”. 日本原子力研究開発機構. p. 6. 2014年8月19日閲覧。
- ^ シャルロー (1974) 295頁。
- ^ a b c d N. N. Greenwood, A. Earnshaw (1997), Chemistry of the Elements (2nd ed. ed.), Oxford: Elsevier Science Ltd (Butterworth-Heinemann), ISBN 0080379419
- ^ a b c d コットン、ウィルキンソン (1987) 271頁。
- ^ 千谷 (1959) 195頁。
- ^ a b c d コットン、ウィルキンソン (1987) 269頁。
- ^ 伊藤和明『物理化学II: 量子化学編』化学同人〈理工系基礎レクチャー〉、2008年、112頁。ISBN 4759810854。
- ^ Okutani, T.; Tsuruta, Y.; Sakuragawa, A. (1993), “Determination of a trace amount of beryllium in water samples by graphite furnace atomic absorption spectrometry after preconcentration and separation as a beryllium-acetylacetonate complex on activated carbon”, Anal. Chem. 65 (9): 1273-1276, doi:10.1021/ac00057a026
- ^ コットン、ウィルキンソン (1987) 272頁。
- ^ 千谷 (1959) 222頁。
- ^ a b c Wiberg, Egon; Holleman, Arnold Frederick (2001), Inorganic Chemistry, Elsevier, ISBN 0123526515
- ^ 井上和彦、坂本幸夫. “ベリリウムフィルターの散乱冷中性子による透過スペクトル歪”. 北海道大學工學部研究報告 (北海道大学) 97: 57-61頁。.
- ^ a b Hausner, Henry H, “Nuclear Properties”, Beryllium its Metallurgy and Properties, University of California Press, p. 239
- ^ Brian, Monica (2010) p. 58
- ^ “Beryllium: Isotopes and Hydrology”. University of Arizona, Tucson. 2011年4月10日閲覧。
- ^ 堀内一穂ほか (2009年5月20日). “ベリリウム10と炭素14を用いた最終退氷期の太陽活動変遷史に関する研究” (PDF). 科学研究費補助金研究成果報告書. 2018年11月4日時点のオリジナルよりアーカイブ。2018年11月4日閲覧。
- ^ Whitehead, N; Endo, S; Tanaka, K; Takatsuji, T; Hoshi, M; Fukutani, S; Ditchburn, Rg; Zondervan, A (Feb 2008), “A preliminary study on the use of (10)Be in forensic radioecology of nuclear explosion sites”, Journal of environmental radioactivity 99 (2): 260-70, doi:10.1016/j.jenvrad.2007.07.016, PMID 17904707
- ^ Boyd, R. N.; Kajino, T. (1989), “Can Be-9 provide a test of cosmological theories?”, The Astrophysical Journal 336: L55, Bibcode: 1989ApJ...336L..55B, doi:10.1086/185360
- ^ Arnett, David (1996), Supernovae and nucleosynthesis, Princeton University Press, p. 223, ISBN 0691011478
- ^ Johnson, Bill (1993年). “How to Change Nuclear Decay Rates”. University of California, Riverside. 2011年10月10日閲覧。
- ^ Hammond, C. R. "Elements" in Lide, D. R., ed. (2005), CRC Handbook of Chemistry and Physics (86th ed.), Boca Raton (FL): CRC Press, ISBN 0-8493-0486-5
- ^ Hansen, P. G.; Jensen, A. S.; Jonson, B. (1995), “Nuclear Halos”, Annual Review of Nuclear and Particle Science 45: 59 1, Bibcode: 1995ARNPS..45..591H, doi:10.1146/annurev.ns.45.120195.003111
- ^ 親松和浩. “原子核の表面対称エネルギーの検討”. 2011年10月10日閲覧。
- ^ Ekspong, G. et al. (1992), Physics: 1981-1990, World Scientific, p. 172, ISBN 9789810207298
- ^ Kenneth (2009) p. 151
- ^ “原子核物理学概論 平成14年度講義資料 第3章 質量公式”. 東京工業大学 武藤研究室. pp. 44-45, 49. 2011年10月13日閲覧。
- ^ シャルロー (1974) 287頁。
- ^ a b シャルロー (1974) 297頁。
- ^ a b WHO, NIHS (2001) 12頁。
- ^ a b 加藤 (1932) 100頁。
- ^ シャルロー (1974) 296頁。
- ^ 加藤 (1932) 102頁。
- ^ 加藤 (1932) 101、104頁。
- ^ 加藤 (1932) 104頁。
- ^ “要調査項目等調査マニュアル(水質、底質、水生生物)” (pdf). 環境庁水質保全局水質管理課 (2000年). 2011年12月23日閲覧。
- ^ WHO, NIHS (2001) 12-13頁。
- ^ “Abundance in the universe”, Mark Winter, The University of Sheffield and WebElements Ltd, UK (WebElements) 2011年9月19日閲覧。
- ^ “Abundance in the sun”, Mark Winter, The University of Sheffield and WebElements Ltd, UK (WebElements) 2011年9月19日閲覧。
- ^ a b WHO, NIHS (2001) 16頁。
- ^ “Abundance in oceans”, Mark Winter, The University of Sheffield and WebElements Ltd, UK (WebElements) 2011年9月19日閲覧。
- ^ “Abundance in stream water”, Mark Winter, The University of Sheffield and WebElements Ltd, UK (WebElements) 2011年9月19日閲覧。
- ^ “Beryllium: geological information”, Mark Winter, The University of Sheffield and WebElements Ltd, UK (WebElements) 2011年9月19日閲覧。
- ^ Charles R. Cowley (1995). An Introduction to Cosmochemistry. Cambridge University Press. p. 201. ISBN 0521459206
- ^ Rick Adair (2007). Beryllium. The Rosen Publishing Group. p. 48. ISBN 1404210032
- ^ Kenneth (2009) p. 65
- ^ “梶原・正路(1997)による〔『エネルギー・資源ハンドブック』(1015-1020p)から〕”. 広島大学地球資源論研究室. 2012年1月28日閲覧。
- ^ “鉱物資源を考える(5)”. 広島大学地球資源論研究室. 2012年1月28日閲覧。
- ^ WHO, NIHS (2001) 15頁。
- ^ WHO, NIHS (2001) 15-16頁。
- ^ Babu, R. S.; Gupta, C. K. (1988), “Beryllium Extraction - A Review”, Mineral Processing and Extractive Metallurgy Review 4: 39, doi:10.1080/08827508808952633 2011年9月20日閲覧。
- ^ a b 田中和明『よくわかる最新レアメタルの基本と仕組み』秀和システム、2007年、115頁。ISBN 4798018090。
- ^ Aldinger et al. (1985) p. 16
- ^ a b c Aldinger et al. (1985) p. 17
- ^ Aldinger et al. (1985) pp. 17-18
- ^ Aldinger et al. (1985) p. 18
- ^ “Sources of Beryllium”, Materion Brush Inc. (Materion Brush Inc.) 2011年9月19日閲覧。
- ^ Brush Wellman - Elmore, Ohio Plant :: Company History, オリジナルの2008年7月24日時点におけるアーカイブ。 2011年9月20日閲覧。
- ^ Lindsey, David A., Slides of the fluorspar, beryllium, and uranium deposits at Spor Mountain, Utah, United States Geological Survey 2011年9月19日閲覧。
- ^ “Brush Wellman Beryllium Plant”, The Center for Land Use Interpretation (The Center for Land Use Interpretation) 2011年9月19日閲覧。
- ^ Commodity Summary 2000: Beryllium, United States Geological Survey 2011年9月19日閲覧。
- ^ Commodity Summary 2010: Beryllium, United States Geological Survey 2011年9月19日閲覧。
- ^ Beryllium Statistics and Information, United States Geological Survey 2011年9月19日閲覧。
- ^ Petzow, Günter et al. "Beryllium and Beryllium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_011.pub2
- ^ Veness, R.; Ramos, D.; Lepeule, P.; Rossi, A.; Schneider, G.; Blanchard, S., Installation and commissioning of vacuum systems for the LHC particle detectors, CERN 2011年9月26日閲覧。
- ^ Wieman, H (2001), “A new inner vertex detector for STAR”, Nuclear Instruments and Methods in Physics Research Section a Accelerators Spectrometers Detectors and Associated Equipment 473: 205, Bibcode: 2001NIMPA.473..205W, doi:10.1016/S0168-9002(01)01149-4
- ^ Davis, Joseph R. (1998), “Beryllium”, Metals handbook, ASM International, pp. 690-691, ISBN 9780871706546
- ^ Schwartz, Mel M. (2002), Encyclopedia of materials, parts, and finishes, CRC Press, p. 62, ISBN 1566766613
- ^ Museum of Mountain Bike Art & Technology: American Bicycle Manufacturing, オリジナルの2011年7月20日時点におけるアーカイブ。 2011年9月26日閲覧。
- ^ ポルシェ909ベルクスパイダーのブレーキディスクなどに使用された。christophorus 336 2009年2月/3月 The Porsche Magagine, 39
- ^ Robert Irion (2010-10), “Origami Observatory: Behind the Scenes with the Webb Space Telescope”, Scientific American Magazine 2011年9月25日閲覧。
- ^ Werner, M. W.; Roellig, T. L.; Low, F. J.; Rieke, G. H.; Rieke, M.; Hoffmann, W. F.; Young, E.; Houck, J. R. et al. (2004), “The Spitzer Space Telescope Mission”, Astrophysical Journal Supplement 154: 1, arXiv:astro-ph/0406223, Bibcode: 2004ApJS..154....1W, doi:10.1086/422992
- ^ Alan L. Geiger, Eric Ulph, Sr. (1992-9-16), Production of metal matrix composite mirrors for tank fire control systems (Proceedings Paper), doi:10.1117/12.137998 2011年9月25日閲覧。
- ^ Kojola, Kenneth ; Lurie, William (1961年8月9日). “The selection of low-magnetic alloys for EOD tools”. Naval Weapons Plant Washington DC 2011年9月26日閲覧。
- ^ Dorsch, Jerry A. and Dorsch, Susan E. (2007), Understanding anesthesia equipment, Lippincott Williams & Wilkins, p. 891, ISBN 0781776031
- ^ MobileReference (1 January 2007), Electronics Quick Study Guide for Smartphones and Mobile Devices, MobileReference, pp. 2396-, ISBN 9781605011004 2011年9月26日閲覧。
- ^ Johnson, Jr., John E. (2007年11月12日). “Usher Be-718 Bookshelf Speakers with Beryllium Tweeters”. 2011年10月11日閲覧。
- ^ “Beryllium use in pro audio Focal speakers”. 2011年10月11日閲覧。
- ^ “Exposé E8B studio monitor”. KRK Systems. 2011年10月11日閲覧。
- ^ “ヤマハ開発者の「実は黙っていたこと」 第3回「Soavo篇」”. STEREO SOUND. 2011年10月11日閲覧。
- ^ 浜田基彦 (2005年9月21日). “パイオニア,高級スピーカシステム「S-7EX」のツイータにベリリウム振動板を採用”. 日経ものづくり. 2011年10月11日閲覧。
- ^ “PUカートリッジ F-8L”. 国立科学博物館 産業技術史資料情報センター. 2011年10月11日閲覧。
- ^ “TECHNICAL DATA”. Eimac. p. 4. 2011年11月12日閲覧。
- ^ Svilar, Mark (2004年1月8日). “Analysis of "Beryllium" Speaker Dome and Cone Obtained from China”. 2009年2月25日時点のオリジナルよりアーカイブ。2009年2月13日閲覧。
- ^ a b Barnaby, Frank (1993), How nuclear weapons spread, Routledge, p. 35, ISBN 0415076749
- ^ Clark, R. E. H.; Reiter, D. (2005), Nuclear fusion research, Springer, p. 15, ISBN 3540230386
- ^ Petti, D; Smolik, G; Simpson, M; Sharpe, J; Anderl, R; Fukada, S; Hatano, Y; Hara, M et al. (2006), “JUPITER-II molten salt Flibe research: An update on tritium, mobilization and redox chemistry experiments”, Fusion Engineering and Design 81 (8-14): 1439, doi:10.1016/j.fusengdes.2005.08.101
- ^ Diehl, Roland (2000). High-power diode lasers. Springer. p. 104. ISBN 3540666931
- ^ “Purdue engineers create safer, more efficient nuclear fuel, model its performance”. Purdue University (2005年9月27日). 2011年10月12日閲覧。
- ^ Breslin AJ (1966). “Chap. 3. Exposures and Patterns of Disease in the Beryllium Industry”. In Stokinger, HE. in Beryllium: Its Industrial Hygiene Aspects. Academic Press, New York. pp. 30-33
- ^ Kenneth (2009) pp. 20-26
- ^ Mining, Society for Metallurgy, Exploration (U.S) (2006-03-05), “Distribution of major deposits”, Industrial minerals & rocks: commodities, markets, and uses, pp. 265-269, ISBN 9780873352338
- ^ 崎川 (1980) 31-36頁。
- ^ 鉱物科学萌研究会『鉱物―萌えて覚える鉱物科学の基本』PHP研究所、2010年、157頁。ISBN 4569773745。
- ^ 崎川 (1980) 37-38頁。
- ^ “ベリリウム銅ガイド”. ブラッシュ ウエルマン ジャパン. p. 6. 2011年10月12日閲覧。
- ^ ばね技術研究会 編『ばね用材料とその特性』日刊工業新聞社、2000年、pp. 190, 203–204頁。
- ^ “ベリリウム銅ガイド”. ブラッシュ ウエルマン ジャパン. p. 37. 2011年10月12日閲覧。
- ^ “Defence forces face rare toxic metal exposure risk”. The Sydney Morning Herald. (2005年2月1日) 2011年9月25日閲覧。
- ^ 櫻井、鈴木、中尾 (2005) 30頁。
- ^ 宇佐見隆行、江口立彦、大山好正、栗原正明、平井崇夫 (2001年). “端子・コネクター用銅合金EFTEC®-97の開発” (pdf). 古河電工. 2011年12月24日閲覧。
- ^ “日本精線、ベリリウム使用せず 高強度銅合金線を開発”. 日刊産業新聞 (2011年4月18日). 2011年12月24日閲覧。
- ^ “大和合金株式会社(三芳合金工業株式会社)”. 東京都産業労働局. 2011年12月24日閲覧。
- ^ “製品安全データシート ベリリウム”. 中央労働災害防止協会 安全衛生情報センター. 2011年10月12日閲覧。
- ^ 金井豊:ベリリウム同位体を用いる堆積学的研究 堆積学研究 2014年 73巻 1号 p.19-26, doi:10.4096/jssj.73.19
- ^ a b c d e f g 環境保健クライテリア No.106 ベリリウム, 国立医薬品食品衛生研究所 2011年9月13日閲覧。
- ^ 国際化学物質安全性カード ベリリウム ICSC番号:0226 (日本語版), 国立医薬品食品衛生研究所 2011年12月11日閲覧。
- ^ a b WHO, NIHS (2001) 37頁。
- ^ a b WHO, NIHS (2001) 36頁。
- ^ WHO, NIHS (2001) 35頁。 より引用
- ^ WHO, NIHS (2001) 35頁。
- ^ “肺疾患”, ベリリウム症, Merck & Co., Inc., Kenilworth, N.J., U.S.A 2018年11月5日閲覧。
- ^ WHO, NIHS (2001) 38頁。
- ^ a b 西村 (2006) 9頁。
- ^ IARC Monograph, Volume 58, International Agency for Research on Cancer, (1993) 2011年9月13日閲覧。
- ^ 西村 (2006) 10頁。
- ^ WHO, NIHS (2001) 6頁。
- ^ 豊田智里, 金田良夫, 河上牧夫 ほか「慢性ベリリウム症の2剖険例」『東京女子医科大学雑誌』第64巻、第12号、東京女子医科大学、1063-1064頁、1994年。2020年7月16日閲覧。
- ^ Photograph of Chicago Pile One Scientists 1946, Office of Public Affairs, Argonne National Laboratory, (2006-06-19) 2011年9月13日閲覧。
ベリリウムと同じ種類の言葉
- ベリリウムのページへのリンク