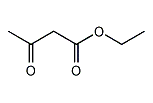
アセト酢酸エチル
| 分子式: | C6H10O3 |
| その他の名称: | Ethyl acetoacetate、Acetoacetic acid ethyl、EAA、Ethyl 3-oxobutanoate、3-Oxobutanoic acid ethyl ester、Acetoacetic acid ethyl ester、3-Oxobutyric acid ethyl ester、5-Oxa-2,4-heptanedione、3-ヒドロキシ-2-ブテン酸エチル、Ethyl 3-hydroxy-2-butenoate、3-Oxobutanoic acid ethyl、Acetylacetic acid ethyl、1-Ethoxy-1,3-butanedione、1-Ethoxybutane-1,3-dione、2-Acetylacaetic acid ethyl、Ethyl 3-oxobutyrate |
| 体系名: | 1-エトキシブタン-1,3-ジオン、1-エトキシ-1,3-ブタンジオン、2-アセチル酢酸エチル、アセチル酢酸エチル、エチル3-オキソブチラート、3-オキソ酪酸エチル、3-オキソブタン酸エチル、アセト酢酸エチル、5-オキサ-2,4-ヘプタンジオン |
アセト酢酸エチル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/06/18 12:59 UTC 版)
| アセト酢酸エチル | |
|---|---|
 |
|
 |
|
|
Ethyl 3-oxobutanoate
|
|
|
別称
|
|
| 識別情報 | |
| CAS登録番号 | 141-97-9  |
| PubChem | 8868 |
| ChemSpider | 13865426  |
| UNII | IZP61H3TB1  |
| EC番号 | 205-516-1 |
| 国連/北米番号 | 1993 |
| KEGG | C03500  |
| ChEBI | |
| ChEMBL | CHEMBL169176  |
| RTECS番号 | AK5250000 |
|
|
|
|
| 特性 | |
| 化学式 | C6H10O3 |
| モル質量 | 130.14 g/mol |
| 外観 | 無色の液体 |
| 匂い | フルーツまたはラム酒 |
| 密度 | 1.030 g/cm3, 液体 |
| 融点 | −45 °C, 228 K, -49 °F |
| 沸点 | 180.8 °C, 454 K, 357 °F |
| 水への溶解度 | 2.86 g/100 ml (20 °C) |
| 酸解離定数 pKa |
|
| 磁化率 | −71.67×10−6cm3/mol |
| 屈折率 (nD) | 1.420 |
| 危険性 | |
| GHSピクトグラム |  |
| GHSシグナルワード | 警告(WARNING) |
| Hフレーズ | H319 |
| Pフレーズ | P305+351+338 |
| NFPA 704 | |
| 引火点 | 70 °C (158 °F; 343 K) |
| 関連する物質 | |
| 関連するエステル | |
| 関連物質 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
アセト酢酸エチル (ethyl acetoacetate) は、エステルの一種で、アセト酢酸とエタノールが脱水縮合した構造を持つ有機化合物である。消防法による第4類危険物 第3石油類に該当する[1]。
性質
無色で果実のような芳香を持つ液体。水にもかなり溶解する (2.86 g/100 mL (20 ℃))ほか、多くの有機溶媒とは任意の割合で混ざり合う。
活性メチレン
アセト酢酸エチルの2位のメチレン部位上の水素 (CH3C(=O)CH2COOC2H5) は、炭素上にあるにもかかわらず、比較的高い酸性 (pKa= 10.7 (25 ℃、水中)) を示す。それは、アセト酢酸エチルの共役塩基にあたるカルバニオンが2種類のエノラート構造と共鳴の関係にあることで、負電荷が非局在化し、安定化されているためである。
このように 2つの電子求引基(例:カルボニル基、シアノ基など)にはさまれることでその場所のプロトンの酸性が強められている状態のメチレン基を、活性メチレン (activated methylene) と呼ぶ。同様の化合物としては、マロン酸エステル、アセチルアセトン、シアノ酢酸エステルなどが挙げられる。アセト酢酸エステル合成や、マロン酸エステル合成では、このカルバニオンの安定性を C-C 結合生成のために利用している。
合成
ジケテンとエタノールの反応によって工業的に大量生産されている。
実験室では、酢酸エチルに、金属ナトリウムあるいはナトリウムエトキシド (C2H5ONa) を加え縮合させて合成する。この反応はクライゼン縮合の一例である。

反応
アセト酢酸エチルは上記で述べたように活性メチレン部位を持ち、塩基を作用させて発生するカルバニオンが比較的安定である。そのカルバニオンを利用したアセト酢酸エステル合成 (acetoacetic ester synthesis) は、有力な C-C 結合生成反応である。活性メチレン化合物はまた、マイケル付加やクロスカップリング反応における求核種としても利用される。
希酸または希アルカリの存在で加水分解を行うと、同時に二酸化炭素が脱離してアセトンを生成するが、強アルカリを作用させると酢酸になる。
用途
各種有機化合物の原料として重要な物質であり、アンチピリン・アタブリンなどの医薬の原料としても用いられる。頻度は高くないが、アンズなどの果実やウイスキー・ラム酒の香料としても使用されることがある[2]。
出典
- ^ 法規情報 (東京化成工業株式会社)
- ^ 『合成香料 化学と商品知識』印藤元一著 2005年増補改訂 化学工業日報社 ISBN 4-87326-460-X
- アセト酢酸エチルのページへのリンク