デフェラシロクス
デフェラシロクス
デフェラシロクス
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/08/30 08:46 UTC 版)
 |
|
 |
|
| IUPAC命名法による物質名 | |
|---|---|
|
|
| 臨床データ | |
| 発音 | de FER a sir ox |
| 販売名 | Exjade, others |
| Drugs.com | monograph |
| MedlinePlus | a606002 |
| ライセンス | US Daily Med:リンク |
| 胎児危険度分類 |
|
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | 70% |
| 血漿タンパク結合 | 99% |
| 代謝 | Liver glucuronidation |
| 半減期 | 8 to 16 hours |
| 排泄 | Fecal (84%) and kidney (8%) |
| データベースID | |
| CAS番号 |
201530-41-8  |
| ATCコード | V03AC03 (WHO) |
| PubChem | CID: 214348 |
| DrugBank | DB01609  |
| ChemSpider | 4591431  |
| UNII | V8G4MOF2V9  |
| KEGG | D03669  |
| ChEBI | CHEBI:49005 |
| ChEMBL | CHEMBL550348  |
| 別名 | CGP-72670, ICL-670A, IC L670 |
| 化学的データ | |
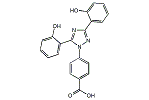
| 化学式 | |
| 分子量 | 373.37 g·mol−1 |
|
|
|
|
|
| 物理的データ | |
| 密度 | 1.4±0.1 g/cm3 [2] |
デフェラシロクス(英:Deferasirox)は、Exjadeなどの商品名で販売されている経口鉄キレート剤である。主な用途は、β-サラセミアやその他の慢性貧血などの疾患で長期輸血を受けている患者の慢性鉄過剰症を軽減することである[3][4]。この目的でアメリカ合衆国で承認された最初の経口薬である[5]。
2005年11月にアメリカ食品医薬品局(FDA)によって承認された[3][5]。FDA(2007年5月)によると、デフェラシロクス経口懸濁液用錠剤を投与された患者で腎不全と細胞減少症が報告されている。ヨーロッパでは、欧州医薬品庁(EMA)により、6歳以上の小児の反復輸血による慢性鉄過剰症を対象に承認されている[6][7][8]。WHO必須医薬品モデル・リストに掲載されている[9]。
2020年7月、Tevaはデフェラシロクスの販売中止を決定した[10]。後発医薬品として利用可能である[11]。
性質

デフェラシロクスの半減期は8~16時間で、1日1回の投与が可能である。デフェラシロクス2分子は1原子の鉄と結合することができ、その後糞便から排泄される。デフェラシロクスより低分子量で親油性が高いために静脈注射しなければならないデフェロキサミンとは異なり、経口投与が可能である。デフェリプロンとともに、デフェラシロックスは細胞(心筋細胞や肝細胞)から鉄を除去し、血液からも鉄を除去することができると考えられている。
合成
デフェラシロクスは、簡単な市販の出発物質(サリチル酸、サリチルアミド、4-ヒドラジノ安息香酸)から、以下の2段階の合成順序で生成できる:

塩化サリチロイル(サリチル酸と塩化チオニルからその場で生成)とサリチルアミドを脱水反応条件下で縮合させると、2-(2-ヒドロキシフェニル)-1,3(4H)-ベンゾオキサジン-4-オンが生成する。この中間体を単離し、塩基の存在下で4-ヒドラジノ安息香酸と反応させると、4-(3,5-ビス(2-ヒドロキシフェニル)-1,2,4-トリアゾール-1-イル)安息香酸(デフェラシロクス)が得られる[12]。
リスク
デフェラシロクスは、Institute for Safe Medical Practicesが2019年にまとめた、報告された患者の死亡で最も頻繁に疑われる薬物のリストで2位にランクされ、1320人の死亡が疑われた[13]。同年、腎不全、肝不全、胃腸出血に関するBoxed warningが追加された[14]。この死亡例急増の主な要因は、ノバルティスによる有害事象データの再解析に関連していると疑われている[13]。
出典
- ^ “Exjade EPAR”. European Medicines Agency (2006年8月28日). 2024年6月21日閲覧。
- ^ “Material Safety Data Sheet (MSDS): Deferasirox”. ChemSrc (2018年). Template:Cite webの呼び出しエラー:引数 accessdate は必須です。
- ^ a b “Current status of iron overload and chelation with deferasirox”. Indian Journal of Pediatrics 74 (8): 759–64. (August 2007). doi:10.1007/s12098-007-0134-7. PMID 17785900. Free full text Archived 29 April 2014 at the Wayback Machine.
- ^ “Deferasirox : a review of its use in the management of transfusional chronic iron overload”. Drugs 67 (15): 2211–30. (2007). doi:10.2165/00003495-200767150-00007. PMID 17927285.
- ^ a b “FDA Approves First Oral Drug for Chronic Iron Overload” (Press release). United States Food and Drug Administration. 9 November 2005. 2005年11月26日時点のオリジナルよりアーカイブ. 2007年10月31日閲覧.
- ^ “Exjade – deferasirox”. European Medicines Agency (2018年). 2017年12月29日時点のオリジナルよりアーカイブ。2012年11月26日閲覧。
- ^ “Turning a blind eye to deferasirox's toxicity?”. Lancet 381 (9873): 1183–4. (April 2013). doi:10.1016/S0140-6736(13)60799-0. PMID 23561999.
- ^ “Review: Exjade side effects”. 2016年3月4日時点のオリジナルよりアーカイブ。2013年4月20日閲覧。
- ^ The selection and use of essential medicines 2023: web annex A: World Health Organization model list of essential medicines: 23rd list (2023). Geneva: World Health Organization. (2023). hdl:10665/371090. WHO/MHP/HPS/EML/2023.02
- ^ “Deferasirox Discontinuation”. U.S. Food and Drug Administration (FDA). 2020年7月21日時点のオリジナルよりアーカイブ。2020年7月20日閲覧。
- ^ “Drugs@FDA: FDA-Approved Drugs”. U.S. Food and Drug Administration. 2020年8月15日閲覧。
- ^ “Complex Formation of ICL670 and Related Ligands with FeIII and FeII”. European Journal of Inorganic Chemistry 2004 (21): 4177–4192. (2004). Bibcode: 2004EJIC.2004.4177S. doi:10.1002/ejic.200400363.]
- ^ a b “QuarterWatch™ (Quarter 4 and 2009 totals): Reported Patient Deaths Increased by 14% in 2009” (英語). Institute For Safe Medication Practices. 2021年6月28日閲覧。
- ^ Pediatrics, American Academy of (19 February 2010). “Black box warning added to Exjade” (英語). AAP News. doi:10.1542/aapnews.20100219-1. ISSN 1073-0397. オリジナルの28 June 2021時点におけるアーカイブ。 2021年6月28日閲覧。.
- デフェラシロクスのページへのリンク