後発医薬品
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/04/12 15:09 UTC 版)
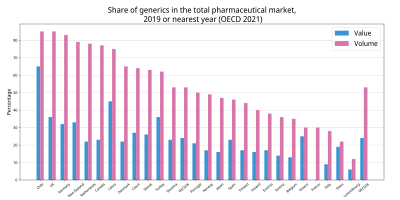
青は金額比、赤は数量比[1]。
新薬の創薬には多大な開発経費がかかるため、その知的財産権は特許として保護されている[3]。後発医薬品は、先発医薬品の特許期間(日本では20年から25年[3][4])終了後に発売される[3][4]。さらに、先発医薬品の製造販売承認後の再審査期間(日本では6年から10年[3])終了後でなければ、特許が切れていても後発医薬品の承認申請はできない[3]。
かつての日本では、医師の間で「ゾロ」「ゾロ品」「ゾロ薬」などと称され[5]、先発医薬品の特許権が消滅したとき、後発医薬品がゾロゾロと出てくることから、そう呼ばれていた[* 1]。
かつて、日本の後発医薬品の普及率は欧米に比べ遅れていたが[2]、厚生労働省主導で普及へ向けての政策や診療報酬の見直しが進められた結果、日本における後発医薬品の普及率は、78.3%(2020年12月。数量ベース)[6]となり、欧米と同等の普及率となっている。なお、アメリカ82%、イギリス81%、ドイツ79%、カナダ70%、オランダ69%、デンマーク54%、オーストラリア50%となっている(2013年・数量ベース)[1]。しかし小林化工や日医工でみられたように、後発品メーカーは利益を追求して品質を軽視する傾向があり[7]、厚生労働省職員の講演では「使用促進は拙速だった」と発言されている[8]。
日本における後発医薬品の薬価は、最初の発売時は原則として先発医薬品の7割、その後は薬価改定を受けて先発医薬品の2割程度となる[要出典]。期限切れになった先発医薬品の特許内容を参考として製造されるため、有効成分が同じであっても、後発医薬品は複数の企業から発売されている。
承認申請
先発医薬品の承認申請には、発見の経緯や外国での使用状況、物理的化学的性質や規格・試験方法、安全性、毒性・催奇性、薬理作用、吸収・分布・代謝・排泄、臨床試験など数多くの試験を行い、26の資料を提出する必要がある。
これに対して、後発医薬品では「規格及び試験方法」「安定性試験」「生物学的同等性試験」の3つの資料と、添付文書記載事項(添付文書案)の提出によって、独立行政法人医薬品医療機器総合機構(PMDA)により審査され、製造承認が下りる。
先発医薬品と比較して、後発医薬品の承認申請資料が少ないのは、有効成分に関する有効性・安全性は、既に先発医薬品において確認されている(毒性試験、薬理試験、臨床試験等)ため、同一の有効成分を使用する後発医薬品では、それらの試験の必要がないとする為である。
この考え方は、アメリカ食品医薬品局 (FDA) 、欧州医薬品庁 (EMA) をはじめ、諸外国でも同様に認められており[9]、後発医薬品の実施試験が少ないからといって、先発医薬品と比べて有効性・安全性・品質が劣ることはないとされている。
生物学的同等性試験
後発医薬品が、先発医薬品と同等の薬効・作用を持つことを証明するために、後発医薬品の承認申請には、生物学的同等性試験(biological equivalence study, BE試験)のデータが必要になる。
生物学的同等性試験では原則として、ヒト(健常人)に先発医薬品・後発品を投与し、両者の血中濃度推移に統計学的な差がないことを確認する[10]。より具体的には、先発医薬品・後発品を各10〜20名程度の健常人に投与し、一定時間ごとに採血を行い、薬物血中濃度の推移を比較し、両群の間に統計学的な差がないことを示す手法がとられる。ただし、倫理的な面や、製剤特性等の理由から、ヒト以外の動物での試験が認められることもある。
日本では、厚生労働省より通達されている「後発医薬品の生物学的同等性試験ガイドライン」に従って、生物学的同等性試験が行われている。
品質再評価
1997年4月以降、新薬の承認時には溶出試験規格の認定が義務付けられ、当該医薬品の後発品についても溶出試験規格が求められていたが、それ以前の経口薬には溶出試験規格がない製品もあった。そこで、溶出試験規格がない医薬品のうち、後発医薬品があり、かつ先発医薬品との同等性を設定する必要がある約550成分(約7000品目)を対象として、1997年2月から厚生省が品質の再評価を始めた。
手順としては、対象成分が選定されると先に標準製剤(通常は先発医薬品)に溶出試験の条件を設定し、次いで標準製剤と後発医薬品の溶出試験結果を比較、類似していることが確認されれば、後発医薬品にも溶出試験が設定される。先発医薬品と後発医薬品の溶出挙動が類似しているのであれば、バイオアベイラビリティーに著しい差が生じる可能性はなくなる、という考え方に基づいたものである。
その結果、先発医薬品との溶出同等性が保証されていると考えられている。しかし、薬物濃度の測定にはクロマトグラフィーが多く用いられるが、製造工程が異なり不純物が異なるにも拘らず同一の条件で測定されており、有効成分と不純物が分離されず不純物濃度を有効成分濃度の一部と見做している可能性は否定されない。
オレンジブック
オレンジブック (Approved Drug Products with Therapeutic Equivalence Evaluations) とは、後発医薬品の使用促進のため米国で発刊されているもので、アメリカ食品医薬品局(FDA)が先発医薬品と後発医薬品の生物学的同等性の判定を行い(生物学的同等性試験)、その治療上の同等性についての評価を掲載したものである。この本の表紙がオレンジ色であることから「オレンジブック」といわれている。
日本版オレンジブックとは「医療用医薬品品質情報集」のことで、上記の品質再評価の経過や結果を掲載したものである[11]。日本版オレンジブックは通知のごとに発行されるため一覧性がなく、通知に含まれない重要な品質再評価情報が掲載されないことがあるため、日本ジェネリック製薬協会がこれらを補い、さらに広範囲の情報を掲載したものを「オレンジブック総合版」として、ウェブサイトで公開している。
- ^ a b Health at a Glance 2013 (Report). OECD. 21 November 2013. pp. 104–105. doi:10.1787/health_glance-2013-en. ISBN 978-92-64-205024。
- ^ a b OECD Economic Surveys: Japan 2009 (Report). OECD. 13 August 2009. pp. 115–116. doi:10.1787/eco_surveys-jpn-2009-en. ISBN 9789264054561。
- ^ a b c d e “ジェネリック医薬品をもっと良く知っていただくために | ジェネリック医薬品って何?”. 日本ジェネリック株式会社. 2020年12月27日閲覧。
- ^ a b “後発医薬品(ジェネリック医薬品)をご存知ですか?”. 東京都福祉保健局. 2020年12月27日閲覧。
- ^ ジェネリック医薬品関連で発生している各種回収事案についての緊急声明文 日本ジェネリック医薬品・バイオシミラー学会、2020年12月18日、2020年12月27日閲覧
- ^ “2018年8月の後発品割合は76.5%”. 2018年12月20日閲覧。
- ^ “後発医薬品 品質不正が示す「薄利多売ビジネス」の限界 | AnswersNews”. 製薬業界の転職サイト Answers(アンサーズ) (2021年10月18日). 2023年5月24日閲覧。
- ^ “第17回日本ジェネリック医薬品・バイオシミラー学会より 厚労省「後発品の使用促進は拙速だった」”. 日経メディカルDI. 2023年5月24日閲覧。
- ^ “生物学的同等性”. ジェネリック医薬品. 長崎県保険医協会. 2011年1月6日閲覧。
- ^ 厚生労働省 2012, p. 6.
- ^ 日本公定書協会『医療用医薬品品質情報集 : Orange book』薬事日報社、1999年6月。ISBN 9784840811385。
- ^ わたしたちのお薦め オーソライズド・ジェネリック - 第一三共エスファ株式会社
- ^ ジェネリック医薬品の臨床効果は先発医薬品と同等と言えるのか? - 日本ジェネリック製薬協会
- ^ “【日医工】日本初オーソライズドジェネリック 『SANIK』に照準”. 薬事日報 (2013年7月23日). 2015年10月26日閲覧。
- ^ “【TREND】後追いAG続々、成熟市場で巻き返し。ティーエスワン、後発品内シェア8割超に”. MRジャーナル(株式会社アクセライズ) (2018年9月3日). 2019年2月18日閲覧。
- ^ “「シムビコート」は3社、「ロナセン」は12社 6月後発品追補へ承認”. 日刊薬業(じほう) (2019年2月15日). 2019年2月18日閲覧。
- ^ 後発品メーカー国内初の売上1000億円世界のトップ10入りの計画も活発化 NIKKEI Drug Information(2014.12) (PDF)
- ^ 多田智裕 (2012年5月22日). “Vol.494 ジェネリックは「先発品と同じ薬」ではありません。短絡的すぎる「薬剤費の抑制=ジェネリックの使用促進」という図式” (HTML). 医療ガバナンス学会. 2019年8月18日閲覧。
- ^ a b c d e f g h i j k l m 健保連海外医療保障 No.89 2011年3月 健康保険組合連合会、2020年12月31日閲覧。
- ^ “世界のジェネリック医薬品事情”. 女性を応援する乳がん情報サイト 乳がんINFOナビ. 日本化薬 (2014年7月31日). 2018年2月11日閲覧。[リンク切れ]
- 1 後発医薬品とは
- 2 後発医薬品の概要
- 3 オーソライズド・ジェネリック(AG)
- 4 各国の状況
- 5 注釈
後発医薬品と同じ種類の言葉
- 後発医薬品のページへのリンク