グリコシルトランスフェラーゼ
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2023/11/11 07:34 UTC 版)
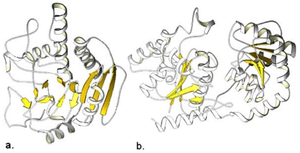
グリコシル基の転移の結果、炭水化物、配糖体、オリゴ糖または多糖が形成される。一部のグリコシルトランスフェラーゼは、無機リン酸や水への転移を触媒する。グリコシル基の転移はタンパク質の残基に対しても行われ、通常チロシン、セリンまたはスレオニンに対する反応によってO-結合型糖タンパク質が形成されるか、アスパラギンに対する反応によってN-結合型糖タンパク質が形成される。トリプトファンに対してマンノシル基の転移が行われ、C-マンノシルトリプトファンが形成されることもある。これは真核生物で比較的豊富に存在する。トランスフェラーゼは脂質を受容体として利用して糖脂質を形成することや、ドリコールリン酸のような脂質結合型糖リン酸を供与体として利用することもある。
糖ヌクレオチドを供与体として利用するグリコシルトランスフェラーゼはLeloir enzyme(ルロワール型酵素)と呼ばれ、その名称は糖ヌクレオチドを最初に発見し、炭水化物の代謝に関する業績によって1970年にノーベル化学賞を受賞したルイ・ルロワールに由来する。ドリコール、ポリプレノールピロリン酸など糖ヌクレオチド以外の供与体を利用するグリコシルトランスフェラーゼはnon-Leloir enzyme(非ルロワール型酵素)と呼ばれる。
哺乳類のグリコシルトランスフェラーゼは9種類の糖ヌクレオチドを供与体として利用する[2]。UDP-グルコース、UDP-ガラクトース、UDP-GlcNAc、UDP-GalNAc、UDP-キシロース、UDP-グルクロン酸、GDP-マンノース、GDP-フコース、CMP-シアル酸である。通常これらの供与体分子のリン酸基にはマンガンなどの二価イオンが配位するが、金属非依存的な酵素も存在する。
多くのグリコシルトランスフェラーゼは1回膜貫通タンパク質で、通常ゴルジ体の膜に固定されている[3]。
機構
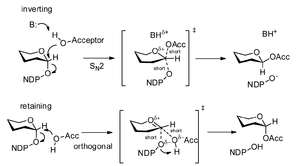
グリコシルトランスフェラーゼは、転移過程によって供与体のアノマー構造の立体化学が保持されるか(α→α)反転するか(α→β)によって、保持型(retaining)と反転型(inverting)の酵素へと分類することができる。反転型の機構は単純であり、受容体原子からの1度の求核攻撃によって立体化学が反転する。
保持型の機構については議論があるが、二重置換機構(立体化学の保持のためにアノマー炭素の2度の反転が引き起こされる)または解離機構(SNi機構のバリエーション)に対しては強い反証が存在する。Orthogonal associative mechanismと呼ばれる機構が提唱されており、反転型酵素と同様に受容体からの1度の求核攻撃のみが必要であるが、(多くの結晶構造で観察されているように)非直線的な角度からの攻撃によってアノマーが保持される[4]。
反応の可逆性
近年、反転型グリコシルトランスフェラーゼによって触媒される反応の多くが可逆的であることが発見され、研究分野にパラダイムシフトが生じるとともに、糖ヌクレオチドを活性化供与体と呼ぶことに関して疑問が提起されている[5][6][7][8][9]。
- ^ Williams, GJ; Thorson, JS (2009). Natural product glycosyltransferases: properties and applications.. Advances in Enzymology - and Related Areas of Molecular Biology. 76. 55–119. doi:10.1002/9780470392881.ch2. ISBN 9780470392881. PMID 18990828
- ^ Essentials of Glycobiology (2nd ed.). Plainview, N.Y: Cold Spring Harbor Laboratory Press. (2008). ISBN 978-0-87969-770-9
- ^ Transferases in Membranome database.
- ^ “Geometric Attributes of Retaining Glycosyltransferase Enzymes Favor an Orthogonal Mechanism”. PLoS ONE 8 (8): e71077. (August 2013). doi:10.1371/journal.pone.0071077. PMC 3731257. PMID 23936487.
- ^ Zhang, C; Griffith, BR; Fu, Q; Albermann, C; Fu, X; Lee, IK; Li, L; Thorson, JS (1 September 2006). “Exploiting the reversibility of natural product glycosyltransferase-catalyzed reactions.”. Science 313 (5791): 1291–4. doi:10.1126/science.1130028. PMID 16946071.
- ^ Zhang, C; Albermann, C; Fu, X; Thorson, JS (27 December 2006). “The in vitro characterization of the iterative avermectin glycosyltransferase AveBI reveals reaction reversibility and sugar nucleotide flexibility.”. Journal of the American Chemical Society 128 (51): 16420–1. doi:10.1021/ja065950k. PMID 17177349.
- ^ Zhang, C; Fu, Q; Albermann, C; Li, L; Thorson, JS (5 March 2007). “The in vitro characterization of the erythronolide mycarosyltransferase EryBV and its utility in macrolide diversification.”. ChemBioChem: A European Journal of Chemical Biology 8 (4): 385–90. doi:10.1002/cbic.200600509. PMID 17262863.
- ^ Zhang, C; Moretti, R; Jiang, J; Thorson, JS (13 October 2008). “The in vitro characterization of polyene glycosyltransferases AmphDI and NysDI.”. ChemBioChem: A European Journal of Chemical Biology 9 (15): 2506–14. doi:10.1002/cbic.200800349. PMC 2947747. PMID 18798210.
- ^ Gantt, RW; Peltier-Pain, P; Cournoyer, WJ; Thorson, JS (21 August 2011). “Using simple donors to drive the equilibria of glycosyltransferase-catalyzed reactions.”. Nature Chemical Biology 7 (10): 685–91. doi:10.1038/nchembio.638. PMC 3177962. PMID 21857660.
- ^ “Glycosyltransferases - CAZypedia” (英語). cazypedia.org. 2020年9月4日閲覧。
- ^ “CAZy - GT”. www.cazy.org. 2020年9月4日閲覧。
- ^ Singh, S; Phillips GN, Jr; Thorson, JS (October 2012). “The structural biology of enzymes involved in natural product glycosylation”. Natural Product Reports 29 (10): 1201–37. doi:10.1039/c2np20039b. PMC 3627186. PMID 22688446.
- ^ Chang, A; Singh, S; Phillips GN, Jr; Thorson, JS (December 2011). “Glycosyltransferase structural biology and its role in the design of catalysts for glycosylation”. Current Opinion in Biotechnology 22 (6): 800–8. doi:10.1016/j.copbio.2011.04.013. PMC 3163058. PMID 21592771.
- ^ “SCOPe: Structural Classification of Proteins — extended. Release 2.07 (updated 2020-07-16, stable release March 2018)” (英語). scop.berkeley.edu. 2020年9月4日閲覧。
- ^ “Structural insight into the transglycosylation step of bacterial cell-wall biosynthesis”. Science 315 (5817): 1402–5. (March 2007). doi:10.1126/science.1136611. PMID 17347437.
- ^ Kocev, A; Melamed, J; Wang, S; Kong, X; Vlahakis, JZ; Xu, Y; Szarek, WA; Brockhausen, I (June 2020). "Inhibition of bacterial growth and galactosyltransferase activity of WbwC by α, ω-bis(3-alkyl-1H-imidazolium)alkane salts: Effect of varying carbon content". Bioorganic and Medicinal Chemistry. 28 (11): 115494. doi:10.1016/j.bmc.2020.115494. PMID 32312486.
- ^ Gantt, RW; Peltier-Pain, P; Thorson, JS (October 2011). “Enzymatic methods for glyco(diversification/randomization) of drugs and small molecules.”. Natural Product Reports 28 (11): 1811–53. doi:10.1039/c1np00045d. PMID 21901218.
- 1 グリコシルトランスフェラーゼとは
- 2 グリコシルトランスフェラーゼの概要
- 3 配列による分類
- 4 利用
- グリコシルトランスフェラーゼのページへのリンク