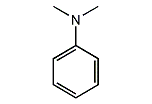
N,N‐ジメチルアニリン
| 分子式: | C8H11N |
| その他の名称: | Phenyldimethylamine、バースネラーNL63/10、Versneller NL63/10、NCI-C-56428、N,N-Dimethylaniline、N,N-Dimethylbenzenamine、Dimethylphenylamine、Dimethyl(phenyl)amine、Dimethylaminobenzene、N,N-Dimethylphenylamine、1-(Dimethylamino)benzene、3-(Dimethylamino)benzene、4-(Dimethylamino)benzene |
| 体系名: | フェニルジメチルアミン、ジメチル(フェニル)アミン、ジメチルアミノベンゼン、4-(ジメチルアミノ)ベンゼン、1-(ジメチルアミノ)ベンゼン、3-(ジメチルアミノ)ベンゼン、N,N-ジメチルベンゼンアミン、N,N-ジメチルアニリン、ジメチルフェニルアミン、N,N-ジメチルフェニルアミン |
ジメチルアニリン
(N,N‐ジメチルアニリン から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/10/14 15:21 UTC 版)
|
|||
| 物質名 | |||
|---|---|---|---|
|
N,N-ジメチルアニリン |
|||
|
別名
DMA; ジメチルアミノベンゼン |
|||
| 識別情報 | |||
|
3D model (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.085 | ||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard (EPA)
|
|||
|
|
|||
|
|||
| 性質 | |||
| C8H11N | |||
| モル質量 | 121.18 g·mol−1 | ||
| 外観 | 無色の液体 | ||
| 匂い | アミンのような | ||
| 密度 | 0.956 g/mL[1] | ||
| 融点 | 2 °C (36 °F; 275 K)[1] | ||
| 沸点 | 194 °C (381 °F; 467 K)[1] | ||
| 2% (20°C)[2] | |||
| 蒸気圧 | 1 mmHg (20°C)[2] | ||
| 磁化率 | −89.66·10−6 cm3/mol | ||
| 危険性 | |||
| 引火点 | 63 °C (145 °F; 336 K) | ||
| 致死量または濃度 (LD, LC) | |||
|
半数致死量 LD50
|
1410 mg/kg (ラット, 経口)[3] | ||
|
LCLo (最低致死濃度)
|
50 ppm (ラット, 4 時間)[3] | ||
| NIOSH(米国の健康曝露限度): | |||
|
PEL
|
TWA 5 ppm (25 mg/m3) [skin][2] | ||
|
REL
|
TWA 5 ppm (25 mg/m3) ST 10 ppm (50 mg/m3) [skin][2] | ||
|
IDLH
|
100 ppm[2] | ||
| 安全データシート (SDS) | External MSDS | ||
|
特記無き場合、データは標準状態 (25 °C [77 °F], 100 kPa) におけるものである。
|
|||
N,N-ジメチルアニリン (N,N-dimethylaniline) は、アニリンから誘導される有機化合物である。ベンゼン環と、2個のメチル基で置換されたアミノ基(ジメチルアミノ基)からなる第三級アミンである。アミン臭を持つ有毒な油状の液体で、溶媒や合成の原料として使われる。純物質は無色であるが、販売されている液体は黄色である。クリスタルバイオレットなどの染料の前駆体として重要である。消防法に定める第4類危険物 第3石油類に該当する[4]。
合成と反応
ジメチルアニリンは1850年、アウグスト・ヴィルヘルム・フォン・ホフマンがアニリンとヨードメタンを加熱して初めて合成した。
- C6H5NH2 + 2 CH3I → C6H5N(CH3)2 + 2 HI
現在、工業的にはアニリンとメタノールを硫酸を触媒として縮合させ(アルキル化)、生じる硫酸塩を塩基で中和して得る[1]。
- C6H5NH2 + 2 CH3OH → C6H5N(CH3)2 + 2 H2O
また同様にジメチルエーテルを使用してメチル化で合成することもできる。
ジメチルアニリンはアニリンと同様に弱塩基や求核剤としての性質を示す。混酸でニトロ化(英:nitration)するとテトリルを生成する。これは4個のニトロ基を持ち、爆発性を示す。またn-ブチルリチウムを作用させるとジメチルアミノ基のオルト位がリチオ化される。ジメチルアミノ基はアルキル化を受け、第四級アンモニウム塩を生ずる[5]。
- C6H5N(CH3)2 + (CH3O)2SO2 → C6H5N(CH3)3+ CH3OSO3-
また、氷冷下でスルファニル酸を亜硝酸ナトリウムでジアゾ化して作ったスルファニル酸のジアゾニウム塩溶液にジメチルアニリン塩酸塩溶液を加えてジアゾカップリングさせると、酸塩基指示薬のメチルオレンジが合成できる。
応用
ジメチルアニリンはマラカイトグリーンやクリスタルバイオレットなどのトリアリールメタン系染料(英:triarylmethane dye)の前駆体として重要であるほか[6]、その他の有機化合物の前駆体としても使用される。またポリエステルやビニルエステル樹脂の成型の際に促進剤として利用される[7]。モルモットやウサギとガスクロマトグラフィーを使用する試験管内でのジメチルアニリンの新陳代謝の研究で新陳代謝のサイクルでの脱メチル化やN-オキシド化の仕組みが確認され、環状ヒドロキシ化のシステムを確立した[8]。
出典
- ^ a b c d Merck Index 14th ed., 3234.
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards 0223
- ^ a b “N,N-Dimethylaniline”. 生活や健康に直接的な危険性がある. アメリカ国立労働安全衛生研究所(NIOSH). 2025年10月15日閲覧。
- ^ 法規情報 (東京化成工業株式会社)
- ^ J. Jacques and A. Marquet (1988). “Selective α-Bromination of an Aralkyl Ketone with Phenyltrimethylammonium Tribromide: 2-Bromoacetyl-6-methoxynaphthalene and 2,2-Dibromoacetyl-6-Methoxynaphthalene”. Organic Syntheses (英語).; Collective Volume, vol. 6, p. 175
- ^ Thomas Gessner and Udo Mayer "Triarylmethane and Diarylmethane Dyes" ウルマン産業化学百科事典 2002年版, Wiley-VCH, Weinheim.doi:10.1002/14356007.a27_179
- ^ General Info on DMA (N,N-Dimethylaniline) Archived 2007年8月29日, at the Wayback Machine., オーストラリア合成化合物事典
- ^ Brimecombe, R. D.; Fogel, R.; Limson, J. L. Electrochemical monitoring of the biodegradation of 2,4-dimethylaniline. J. Agric. Food. Chem.2006 54 8799-8803.
- N,N‐ジメチルアニリンのページへのリンク