硫酸ジメチル
硫酸ジメチル
| 化合物名や化合物に関係する事項: | 硫酸イオン 硫酸カリウム 硫酸カルシウム 硫酸ジメチル 硫酸ドデシルナトリウム 硫酸ナトリウム 硫酸バリウム |
硫酸ジメチル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/05/24 14:22 UTC 版)
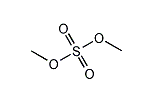
硫酸ジメチル(りゅうさんジメチル、dimethyl sulfate)は化学式 (CH3O)2SO2 で表される化合物で、硫酸のジメチルエステル。結合様式を表現せずに (CH3)2SO4 あるいは Me2SO4 とも表記する。
- ^ a b c Suter, C. M. (1944). The Organic Chemistry of Sulfur (Tetracovalent Sulfur Compounds). New York: John Wiley & Sons. pp. 49–53
- ^ Shirley, D. A. (1967). Organic Chemistry. Texas: Holt, Rinehart and Winston. pp. 253
- ^ a b アメリカ合衆国保健福祉省. “12th Report on Carcinogens”. 2011年11月4日閲覧。
- ^ アメリカ合衆国保健福祉省. “Substance Profiles - Dimethyl Sulfate (PDF)”. 12th Report on Carcinogens. 2011年11月4日閲覧。
- ^ Lucier, J. J.; Harris, A. D.; Korosec, P. S. (1964). "N-Methylbutylamine". Organic Syntheses (英語). 44: 72.
- ^ デュポン. “DMS Overview”. 2007年10月14日閲覧。
- ^ Streitwieser, A.; Heathcock, C. H.; Kosower, E. M. (1992). Introduction to Organic Chemistry. New Jersey: Prentice-Hall. pp. 1169
- ^ Rippey, J. C.; Stallwood, M. I. (2005). “Nine cases of accidental exposure to dimethyl sulphate - a potential chemical weapon”. Emerg. Med. J. 22: 878–879. PMID 16299199.
- ^ Fieser, L. F.; Fieser, M. (1967). Reagents for Organic Synthesis. New York: John Wiley & Sons. pp. 295
- ^ Shieh, W.-C.; Dell, S.; Repič, O. (2001). “1,8-Diazabicyclo[5.4.0]undec-7-ene (DBU) and microwave-accelerated green chemistry in methylation of phenols, indoles, and benzimidazoles with dimethyl carbonate”. Org. Lett. 3: 4279–4281. doi:10.1021/ol016949n.
- ^ 毒物及び劇物取締法 昭和二十五年十二月二十八日 法律三百三号 第二条 別表第二
- 1 硫酸ジメチルとは
- 2 硫酸ジメチルの概要
- 3 安全性
硫酸ジメチルと同じ種類の言葉
固有名詞の分類
- 硫酸ジメチルのページへのリンク