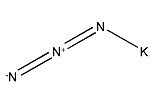
カリウムアザイド
アジ化カリウム
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/10/06 06:55 UTC 版)
|
|||

|
|||
| 物質名 | |||
|---|---|---|---|
|
Potassium azide |
|||
| 識別情報 | |||
|
3D model (JSmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.039.997 | ||
| EC番号 |
|
||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| 性質 | |||
| KN 3 |
|||
| モル質量 | 81.1184 g/mol | ||
| 外観 | 無色の結晶[1] | ||
| 密度 | 2.038 g/cm3 [1] |
||
| 融点 | 350 °C (662 °F; 623 K) (真空中)[1] | ||
| 沸点 | 分解 | ||
| 41.4 g/100 mL (0 °C) 50.8 g/100 mL (20 °C) 105.7 g/100 mL (100 °C) |
|||
| 溶解度 | 0.1375 g/100 g エタノール (16 °C)[2] エーテルに溶けない |
||
| 熱化学 | |||
| 標準生成熱 ΔfH |
−1.7 kJ/mol | ||
| 危険性 | |||
| 労働安全衛生 (OHS/OSH): | |||
|
主な危険性
|
高い毒性、強熱すると爆発 | ||
| NFPA 704(ファイア・ダイアモンド) | |||
| 致死量または濃度 (LD, LC) | |||
|
半数致死量 LD50
|
27 mg/kg (経口, ラット)[3] | ||
| 関連する物質 | |||
| その他の 陽イオン |
アジ化ナトリウム, アジ化銅(II), アジ化鉛, アジ化銀 | ||
|
特記無き場合、データは標準状態 (25 °C [77 °F], 100 kPa) におけるものである。
|
|||
アジ化カリウム(Potassium azide)は、KN3の化学式を持つ化合物である。アジ化水素のカリウム塩であり、結晶は正方晶を作る[4]。水酸化カリウムとアジ化水素との反応によって得られ[5]、熱するか紫外線を照射するとカリウムと窒素ガスに分解する[6][7]。重金属のアジ化物とは異なり、衝撃には敏感ではないが、急速に加熱すると爆発する[8]。
土壌の硝化阻害剤として働くことが知られている[9]。また、加熱分解によって金属カリウムと窒素に分解することから、純粋なカリウムを製造するために利用される[5]。
出典
- ^ a b c Dale L. Perry; Sidney L. Phillips (1995). Handbook of inorganic compounds. CRC Press. p. 301. ISBN 0-8493-8671-3
- ^ Jiri Hála (2004). “IUPAC-NIST Solubility Data Series. 79. Alkali and Alkaline Earth Metal Pseudohalides.”. J. Phys. Chem. Ref. Data 33 (1): 16. Bibcode: 2004JPCRD..33....1H. doi:10.1063/1.1563591.
- ^ “Substance Name: Potassium azide”. chem.sis.nlm.nih.gov. 2014年8月12日時点のオリジナルよりアーカイブ。2014年8月11日閲覧。
- ^ Khilji, M. Y.; Sherman, W. F.; Wilkinson, G. R. (1982). “Variable temperature and pressure Raman spectra of potassium azide KN3”. Journal of Raman Spectroscopy 12 (3): 300–303. doi:10.1002/jrs.1250120319. ISSN 03770486.
- ^ a b 宮川誠之助 著、化学大辞典編集委員会(編) 編『化学大辞典』 1巻(縮刷版第26版)、共立、1981年10月、60頁頁。
- ^ Tompkins, F. C.; Young, D. A. (1982), “The Photochemical and Thermal Formation of Colour Centres in Potassium Azide Crystals”, Proceedings of the Royal Society of London, Series A, Mathematical and Physical Sciences 236 (1204): 10–23
- ^ Pradyot Patnaik (2003). Handbook of inorganic chemicals. McGraw-Hill Professional. p. 734. ISBN 0070494398
- ^ Pradyot Patnaik (2007), A comprehensive guide to the hazardous properties of chemical substances (第3 ed.), Wiley-Interscience, p. 615, ISBN 0471714585
- ^ T. D. Hughes; L. F. Welch (1970), “Potassium Azide as a Nitrification Inhibitor”, Agronomy Journal (American Society of Agronomy) 62: 595–599
- アジ化カリウムのページへのリンク