四フッ化キセノン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/03/24 07:55 UTC 版)
ナビゲーションに移動 検索に移動| 四フッ化キセノン | |
|---|---|

| |
|
|
フッ化キセノン(IV) | |
| 識別情報 | |
| CAS登録番号 | 13709-61-0 |
| 特性 | |
| 化学式 | XeF4 |
| モル質量 | 207.2836 g mol−1 |
| 外観 | 白色固体 |
| 密度 | 4.040 g cm−3, 固体 |
| 沸点 |
117 ℃ (390 K) |
| 構造 | |
| 配位構造 | D4h |
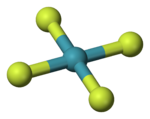
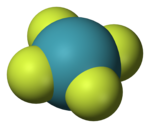
| 分子の形 | 平面四角形 |
| 双極子モーメント | 0 D |
| 危険性 | |
| 引火点 | ? ℃ |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
この物質の構造は、1963年に核磁気共鳴分光法とX線結晶構造解析により平面四角形であると報告されている[5][6]。キセノンが2対の孤立電子対をもっているため、この構造はVSEPR理論により説明される。
四フッ化キセノンは、無色の結晶として発生する。115.7℃で昇華する。
キセノンのフッ化物は標準温度で全て熱力学的に安定であるが、空気中の水分とさえ反応するので、乾燥状態で保存しなければならない。
この物質とフッ化テトラメチルアンモニウムを反応させると、ペンタフルオロキセノン酸テトラメチルアンモニウムが得られる。
脚注
出典
- ^ Claassen, H. H.; Selig, H.; Malm, J. G. "Xenon Tetrafluoride" J. Am. Chem. Soc. 1962, 84, 3593. DOI: 10.1021/ja00877a042
- ^ a b Zumdahl. Chemistry. p. 243. ISBN 0-618-52844-X
- ^ Claassen, H. H.; Selig, H.; Malm, J. G. (1962). “Xenon Tetrafluoride”. J. Am. Chem. Soc. 84 (18): 3593. doi:10.1021/ja00877a042.
- ^ C. L. Chernick, H. H. Claassen, P. R. Fields 1, H. H. Hyman, J. G. Malm, W. M. Manning, M. S. Matheson, L. A. Quarterman, F. Schreiner, H. H. Selig, I. Sheft, S. Siegel, E. N. Sloth, L. Stein, M. H. Studier, J. L. Weeks, and M. H. Zirin (1962). “Fluorine Compounds of Xenon and Radon”. Science 138 (3537): 136–138. doi:10.1126/science.138.3537.136. PMID 17818399.
- ^ Thomas H. Brown, E. B. Whipple, and Peter H. Verdier (1963). “Xenon Tetrafluoride: Fluorine-19 High-Resolution Magnetic Resonance Spectrum”. Science 140 (3563): 178. doi:10.1126/science.140.3563.178. PMID 17819836.
- ^ James A. Ibers and Walter C. Hamilton (1963:). “Xenon Tetrafluoride: Crystal Structure”. Science 139 (3550): 106–107. doi:10.1126/science.139.3550.106. PMID 17798707.
- 1 四フッ化キセノンとは
- 2 四フッ化キセノンの概要
四フッ化キセノンと同じ種類の言葉
- 四フッ化キセノンのページへのリンク
