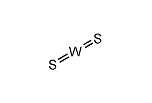二硫化タングステン
硫化タングステン(IV)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/10/27 09:10 UTC 版)

|
|

左:サファイア上のWS2フィルム
右:水面に浮くWS2フィルム |
|
| 物質名 | |
|---|---|
|
Tungsten sulfur |
|
|
Dithioxotungsten
|
|
|
別名
Tungsten(IV) sulfide |
|
| 識別情報 | |
|
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.032.027 |
| EC番号 |
|
|
PubChem CID
|
|
|
CompTox Dashboard (EPA)
|
|
|
|
|
|
| 性質 | |
| WS2 | |
| モル質量 | 247.98 g/mol |
| 外観 | 青灰色の粉末[1] |
| 密度 | 7.5 g/cm3, 固体[1] |
| 融点 | 1,250 °C (2,280 °F; 1,520 K) 分解[1] |
| わずかに溶ける | |
| バンドギャップ | ~1.35 eV (光学, 間接, バルク)[2][3] ~2.05 eV (光学, 直接, 単層)[4] |
| 磁化率 | +5850·10−6 cm3/mol[5] |
| 構造 | |
| 輝水鉛鉱 | |
| 三角柱形 (WIV) ピラミッド型(S2−) |
|
|
特記無き場合、データは標準状態 (25 °C [77 °F], 100 kPa) におけるものである。
|
|
硫化タングステン(IV)(りゅうかタングステン、英: Tungsten(IV) sulfide)は、タングステンと硫黄が化合した無機化合物で、化学式WS2で表される。天然には硫化タングステン鉱(英: tungstenite)として存在する。一般的には二硫化タングステンと呼ばれる。
結晶構造
硫化モリブデン(IV)のような層状結晶構造をとり、タングステン原子は三方晶プリズム形の配位圏をとる。そのため摩擦特性などは硫化モリブデン(IV)に近いものとなる。
製造法
素材としての硫化タングステン(IV)はタングステンと硫黄を合成して人工的に製造される。殆どの硫化モリブデン(IV)は輝水鉛鉱を粉砕、精製して製造される天然由来のものであるため、それらに比べると安定した品質のものが得られる。当然ながら価格は硫化モリブデン(IV)よりも高価なものとなる。
性質
分子量は248.02で、加圧されると電気抵抗が小さくなる半導体の性質を持っている[6]。また、薬品への耐性が強く、塩酸などの比較的弱い酸や、水酸化ナトリウム水溶液のようなアルカリにはほとんど腐食されない[6]。 高負荷に対する耐久性、-273℃~450℃ の温度範囲で潤滑剤として機能、不活性、無機、無毒、などの特性があります。[7]
用途
 |
この節の加筆が望まれています。
|
脱硫の触媒や、高温など潤滑油が使えない場合には固体の潤滑剤として使われる[8]。また、薄いトランジスタの材料としても使われる[9]。
グリース,ペースト,油への添加剤,プラスチックへの充填剤や乾燥被膜,金属系複合材としても使われる。[10]
脚注
出典
- ^ a b c Eagleson, Mary (1994). Concise encyclopedia chemistry. Walter de Gruyter. p. 1129. ISBN 978-3-11-011451-5
- ^ Kam, K. K.; Parkinson, B. A. (February 1982). “Detailed photocurrent spectroscopy of the semiconducting group VIB transition metal dichalcogenides”. Journal of Physical Chemistry 86 (4): 463–467. doi:10.1021/j100393a010.
- ^ Baglio, Joseph A.; Calabrese, Gary S.; Kamieniecki, Emil; Kershaw, Robert; Kubiak, Clifford P.; Ricco, Antonio J.; Wold, Aaron; Wrighton, Mark S. et al. (July 1982). “Characterization of n-Type Semiconducting Tungsten Disulfide Photoanodes in Aqueous and Nonaqueous Electrolyte Solutions Photo-oxidation of Halides with High Efficiency”. J. Electrochem. Soc. 129 (7): 1461–1472. Bibcode: 1982JElS..129.1461B. doi:10.1149/1.2124184.
- ^ Gutiérrez, Humberto; Perea-López, Nestor; Elías, Ana Laura; Berkdemir, Ayse; Wang, Bei; Lv, Ruitao; López-Urías, Florentino; Crespi, Vincent H. et al. (November 2012). “Extraordinary Room-Temperature Photoluminescence in Triangular WS2 Monolayers”. Nano Letters 13 (8): 3447–3454. arXiv:1208.1325. Bibcode: 2013NanoL..13.3447G. doi:10.1021/nl3026357. PMID 23194096.
- ^ Haynes, William M., ed (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. p. 4.136. ISBN 1439855110
- ^ a b “二硫化タングステンとは?”. 日本潤滑剤販売株式会社. 2022年6月24日閲覧。
- ^ https://ws2-nihon.co.jp/tungsten/
- ^ 『無機材料の表面処理・改質技術と将来展望: 金属,セラミックス,ガラス』CMC Publishing Co.,Ltd、2007年、139頁。 ISBN 9784882316978。
- ^ “日本半導体の勝ち筋、2nm以降先回りと台湾企業の取り込みが鍵”. 日経クロステック. (2022年6月24日) 2022年6月24日閲覧。
{{cite news}}: CS1メンテナンス: 先頭の0を省略したymd形式の日付 (カテゴリ) - ^ 由布子, 村田 (2016年8月16日). “二硫化タングステンの特長と用途”. ジュンツウネット21. 2023年9月7日閲覧。
関連項目
- 硫化タングステン(IV)のページへのリンク