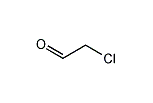
クロロアセトアルデヒド
クロロアセトアルデヒド
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/10/04 02:28 UTC 版)
|
|||
| 物質名 | |||
|---|---|---|---|
|
Chloroacetaldehyde
|
|||
|
Chloroethanal
|
|||
|
別名
2-Chloroacetaldehyde |
|||
| 識別情報 | |||
|
|||
|
3D model (JSmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.158 | ||
| EC番号 |
|
||
|
PubChem CID
|
|||
|
日化辞番号
|
|
||
| UNII |
|
||
|
CompTox Dashboard (EPA)
|
|||
|
|||
|
|||
| 性質 | |||
| C2H3ClO | |||
| モル質量 | 78.50 g mol−1 | ||
| 外観 | 無色の液体 | ||
| 匂い | 刺激臭[1] | ||
| 密度 | 1.117 g/mL | ||
| 融点 | −16.3 °C (2.7 °F; 256.8 K) 水和物は 43–50 °Cで融解[1] | ||
| 沸点 | 85 - 85.5 °C (185.0 - 185.9 °F; 358.1 - 358.6 K) | ||
| 溶ける[1] | |||
| 溶解度 | 有機溶媒 | ||
| 危険性 | |||
| 労働安全衛生 (OHS/OSH): | |||
|
主な危険性
|
アルキル化剤 | ||
| GHS表示: | |||
    |
|||
| Danger | |||
| H301, H311, H314, H330, H351, H400 | |||
| 引火点 | 87.7 °C (189.9 °F) (closed cup) | ||
| 致死量または濃度 (LD, LC) | |||
|
半数致死量 LD50
|
89 mg/kg (経口, ラット) 82 mg/kg (経口, マウス)[3] |
||
|
半数致死濃度 LC50
|
200 ppm (ラット, 1 時間)[4] | ||
| NIOSH(米国の健康曝露限度): | |||
|
PEL
|
C 1 ppm (3 mg/m3)[2] | ||
|
REL
|
C 1 ppm (3 mg/m3)[2] | ||
|
IDLH
|
45 ppm[2] | ||
| 関連する物質 | |||
| 関連物質 | 2-クロロエタノール、クロロ酢酸 | ||
|
特記無き場合、データは標準状態 (25 °C [77 °F], 100 kPa) におけるものである。
|
|||
クロロアセトアルデヒド(英: Chloroacetaldehyde)は、化学式ClCH2CHOで表される有機塩素化合物。本化合物は高活性の求電子剤であり、潜在的に危険なアルキル化作用を持つ。通常は無水物としては存在せず、水和物(アセタール、ClCH2CH(OH)2)の形をとる。クロロアセトアルデヒドは2-アミノチアゾールなど多くの医薬品の合成中間体となるほか、抗菌剤[5]や、木材から樹皮を除去する薬剤としても使用されている。
合成と反応
クロロアセトアルデヒド水和物は、塩素を使用して塩化ビニル水溶液を酸化させることにより得られる。
ClCH=CH2 + Cl2 + H2O → ClCH2CHO + 2 HCl
二官能性を持つことから、多くの複素環式化合物の前駆体となる。チオ尿素誘導体にアミノチアゾールを導入する反応は、かつては最初のサルファ薬の一種であるスルファチアゾールの製造に重要であった[6]。
クロロアセトアルデヒドは、1,2-ジクロロエタンの代謝産物であり、最初2-クロロエタノールを経て生成する。1,2-ジクロロエタンが塩化ビニルの前駆体として数十億kg生産されていることから、この代謝経路は重要である[7]。
安全性
日本の毒物及び劇物取締法では毒物に、消防法では危険物第4類第3石油類に分類される。ラットへの経口投与による半数致死量(LD50)は23 mg/kg、ウサギへの経皮投与によるLD50は67 mg/kgのデータがあり、皮膚や眼に対し重度の損傷を与える[5]。
脚注
- ^ a b c The Merck index. S Budavari, M O'Neil, A Smith (12 ed.). Merck. (1996). pp. 2108. ISBN 9780911910124
- ^ a b c NIOSH Pocket Guide to Chemical Hazards 0118
- ^ “Chloroacetaldehyde”. National Institute for Occupational Safety and Health (2014年12月4日). 2015年2月20日閲覧。
- ^ “Chloroacetaldehyde”. 生活や健康に直接的な危険性がある. アメリカ国立労働安全衛生研究所(NIOSH). 2025年10月4日閲覧。
- ^ a b “製品安全データシート クロロアセトアルデヒド”. 安全衛生情報センター (2011年1月31日). 2011年10月25日閲覧。
- ^ a b Reinhard Jira, Erwin Kopp, Blaine C. McKusick, Gerhard Röderer, Axel Bosch, Gerald Fleischmann (2007). “Chloroacetaldehydes”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a06_527.pub2
- ^ Janssen, D. B.; van der Ploeg, J. R. and Pries, F. (1994). “Genetics and biochemistry of 1,2-dichloroethane degradation”. Biodegradation 5: 249-257. doi:10.1007/BF00696463.
- クロロアセトアルデヒドのページへのリンク