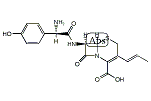
セフプロジル
| 分子式: | C18H19N3O5S |
| その他の名称: | セフプロジル、Cefprozil、BMY-28100、cis-セフプロジル、cis-Cefprozil、(6R,7R)-7-[(R)-2-Amino-2-(p-hydroxyphenyl)acetylamino]-8-oxo-3-(1-propenyl)-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid |
| 体系名: | (6R,7R)-7-[(R)-2-アミノ-2-(p-ヒドロキシフェニル)アセチルアミノ]-8-オキソ-3-(1-プロペニル)-5-チア-1-アザビシクロ[4.2.0]オクタ-2-エン-2-カルボン酸 |
セフプロジル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/08/13 21:20 UTC 版)
 |
|
| IUPAC命名法による物質名 | |
|---|---|
|
|
| 臨床データ | |
| 販売名 | Cefzil, Cefproz, others |
| Drugs.com | monograph |
| MedlinePlus | a698022 |
| ライセンス | US FDA:リンク |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 薬物動態データ | |
| 生物学的利用能 | 95% |
| 血漿タンパク結合 | 36% |
| 半減期 | 1.3 hours |
| データベースID | |
| CAS番号 |
92665-29-7  |
| ATCコード | J01DC10 (WHO) |
| PubChem | CID: 9887643 |
| DrugBank | DB01150  |
| ChemSpider | 8063315  |
| UNII | 1M698F4H4E  |
| KEGG | D07651  |
| ChEBI | CHEBI:3506  |
| ChEMBL | CHEMBL1742  |
| 別名 | Cefproxil |
| 化学的データ | |
| 化学式 | |
| 分子量 | 389.43 g·mol−1 |
|
|
|
|
|
セフプロジル(英:Cefprozil)は第二世代セファロスポリン系抗生物質である[1]。1983年に発見され、1992年に承認され[2]、ブリストル・マイヤーズ スクイブからCefzilという商品名で2010年まで販売されていたが、この商品名での販売は中止された[3]。現在も各社の後発医薬品として使用可能である[4]。咽頭炎、扁桃炎、耳炎、急性副鼻腔炎、慢性気管支炎のbacterial exacerbation、皮膚や皮膚構造の感染症の治療に使用される[5]。現在、錠剤と液体懸濁液として使用可能である。
副作用
セファロスポリン系抗生物質とペニシリン系抗生物質の交差アレルギーリスクは10%とされているが、セフプロジルと他の第二世代以降のセファロスポリン系抗生物質については、交差アレルギーのリスクは増加しないことが研究で示されている[6]。最も一般的な副作用は肝検査値の上昇(ASTおよびALGTを含む)、めまい、好酸球増多、おむつかぶれおよび重複感染、genital pruritus、膣炎、下痢、吐き気、嘔吐、腹痛であった[5]。
細菌の感受性と耐性スペクトル
現在、Enterobacter aerogenes、Morganella morganii、緑膿菌などの細菌はセフプロジルに耐性であるが、Salmonella entericaの血清型Agonaやレンサ球菌はセフプロジルに感受性である。Brucella abortus、モラクセラ・カタラーリス、肺炎レンサ球菌などのいくつかの細菌は、程度の差こそあれ、セフプロジルに耐性を獲得している。最小発育阻止濃度に関する詳細な情報は、Cefprozil Susceptibility and Resistance Data sheetに記載されている[7]。
合成

中間体(1)の塩化アリルをトリフェニルホスフィンで置換すると、ホスホニウム塩(2)が得られる。この官能性は次にイリドに変換される;アセトアルデヒドとの縮合により、ビニル誘導体(3)が得られる;脱保護されるとセフプロジルが得られる。90:10のZ/E異性体混合物からなる半合成経口セファロスポリン[12][13]。
脚注
- ^ “Cefzil (cefprozil) dosing, indications, interactions, adverse effects, and more”. reference.medscape.com. 2021年5月12日閲覧。
- ^ (英語) Analogue-based Drug Discovery. John Wiley & Sons. (2006). p. 496. ISBN 9783527607495
- ^ “Determination That CEFZIL (Cefprozil) Tablets, 250 Milligrams and 500 Milligrams, and for Oral Suspension, 125 Milligrams/5 Milliliters and 250 Milligrams/5 Milliliters, Were Not Withdrawn From Sale for Reasons of Safety or Effectiveness”. The Federal Register. National Archives (2018年9月11日). Template:Cite webの呼び出しエラー:引数 accessdate は必須です。
- ^ “Drugs@FDA: FDA-Approved Drugs”. www.accessdata.fda.gov. 2022年8月3日閲覧。
- ^ a b “Cefzil® (CEFPROZIL) Prescribing Facts”. U.S. Food and Drug Administration. Bristol Myers Squibb. Template:Cite webの呼び出しエラー:引数 accessdate は必須です。
- ^ “Cephalosporins can be prescribed safely for penicillin-allergic patients”. The Journal of Family Practice 55 (2): 106–112. (February 2006). PMID 16451776. オリジナルの2012-09-16時点におけるアーカイブ。 2011年2月26日閲覧。.
- ^ “Cefprozil Susceptibility and Resistance Data”. 2013年7月23日閲覧。
- ^ DE 3402642, Hoshi H, et al., issued 1984, assigned to Bristol-Myers
- ^ US 4520022, Hoshi H, et al., issued 1985, assigned to Bristol-Myers
- ^ “Synthesis and structure-activity relationships of a new oral cephalosporin, BMY-28100 and related compounds”. The Journal of Antibiotics 40 (7): 991–1005. (July 1987). doi:10.7164/antibiotics.40.991. PMID 3624077.
- ^ US 4727070, Kaplan MA, et al., issued 1988, assigned to Bristol-Myers
- ^ “In vitro and in vivo evaluations of BMY-28100, a new oral cephalosporin”. The Journal of Antibiotics 40 (8): 1175–1183. (August 1987). doi:10.7164/antibiotics.40.1175. PMID 3500158.
- ^ “Forty days oral toxicity of 2,6-cis-diphenylhexamethylcyclotetrasiloxane (KABI 1774)in beagle dogs with special reference to effects on the male reproductive system”. Acta Pharmacologica et Toxicologica 36 (Suppl 3): 93–130. (1975). doi:10.1111/j.1600-0773.1975.tb03087.x. PMID 1080338.
外部リンク
- Cefprozil MedlinePlus Drug Information
- セフプロジルのページへのリンク