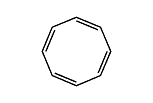
シクロオクタテトラエン
シクロオクタテトラエン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/06/27 01:21 UTC 版)
| シクロオクタテトラエン | |
|---|---|
 |
 |
 |
 |
|
別称
[8]Annulene
(1Z,3Z,5Z,7Z)-Cycloocta-1,3,5,7-tetraene 1,3,5,7-Cyclooctatetraene COT |
|
| 識別情報 | |
|
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.010.074 |
| EC番号 |
|
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard (EPA)
|
|
|
|
|
|
| 特性 | |
| 化学式 | C8H8 |
| モル質量 | 104.15 g/mol |
| 外観 | 澄んだ黄色 |
| 密度 | 0.9250 g/cm3, 液体 |
| 融点 | −5 ~ −3℃ |
| 沸点 | 142 ~ 143℃ |
| 磁化率 | −53.9·10−6 cm3/mol |
| 危険性 | |
| GHS表示: | |
   |
|
| Danger | |
| H225, H304, H315, H319, H335 | |
| P210, P233, P240, P241, P242, P243, P261, P264, P271, P280, P301+310, P302+352, P303+361+353, P304+340 | |
| NFPA 704(ファイア・ダイアモンド) | |
| 引火点 | |
| 関連する物質 | |
| 関連する炭化水素 | シクロオクタン テトラフェニレン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
シクロオクタテトラエン (cyclooctatetraene, C8H8) は、環状炭化水素の一つ。アヌレン類のひとつであり、[8]アヌレンとも呼ばれる。通常は二重結合が全てシス型の (1Z,3Z,5Z,7Z)-シクロオクタテトラエンを指す事が多い。
1905年にリヒャルト・ヴィルシュテッターによって初めて合成された。ヴィルシュテッターの合成法はプソイドペレチエリンを酸化・ホフマン脱離させて10段階を要し、不純物としてスチレンを含むなど収率は低かった。今日ではアセチレンをテトラヒドロフランに溶解させてシアン化ニッケルを触媒として15~25気圧に加圧し、加熱しながら重合させて得られる(レッペ反応)。
外気と反応して過酸化物を作りやすいため、試薬としては酸化防止剤としてヒドロキノンが添加される。
性質
シクロオクタテトラエンは4個の共役二重結合をもつが、分子構造ではベンゼンのように全原子が同一平面上にあるのではなく、二重結合が全てシス型のものは共鳴による安定化がほとんどなく芳香族としての性質を示さない。よって炭素原子間の距離は全部同じではなく、また付加反応が起こりやすい。これらの性質は、シクロオクタテトラエンのπ電子の数が8個でありヒュッケル則に反するためである。
しかし、カリウムと反応させると、カリウム原子二つと結合する際に二つ電子を受け取ってジアニオン(シクロオクタテトラエンジアニオン)となり、π電子数が10となってヒュッケル則を満たすことから芳香族性を持つようになる。同様の例としては、シクロオクタテトラエン分子2つがウランと結合したウラノセンがある。
出典
- ^ “Front Matter”. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. (2014). pp. P001–P004. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4
関連項目
シクロオクタテトラエン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2021/01/31 03:26 UTC 版)
「反芳香族性」の記事における「シクロオクタテトラエン」の解説
当初は反芳香族であるとされていたが実際にはそうではない分子のもう一つの例はシクロオクタテトラエンである。シクロオクタテトラエンはおけ型(すなわちボート型)配座であると推測されている。平面ではないため、4n π電子を持っていたとしても、これらの電子は非局在化や共役をしない。ゆえにシクロオクタテトラエンは非芳香族である。
※この「シクロオクタテトラエン」の解説は、「反芳香族性」の解説の一部です。
「シクロオクタテトラエン」を含む「反芳香族性」の記事については、「反芳香族性」の概要を参照ください。
- シクロオクタテトラエンのページへのリンク