色素
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/12/11 07:01 UTC 版)
発色機構
前述のように発色は電荷と光子の相互作用なので、量子効率の高い物質では物質固有の特性である紫外吸収が長波長側にずれたり、あるいは近赤外吸収が短波長側にずれると、吸収スペクトルの裾野が可視領域にかかるので、色として認識される。また、セレン化合物のようにエネルギー帯間遷移のエネルギー準位の波長が可視領域と一致して呈色する場合もある。つぎに主な発色機構について説明する。
発色団説
有機化合物と色との関係に初めて言及したのはドイツ人化学者グラーベ (C.Grabe) とリーベルマン (C.T.Libermann) である。彼らは1868年に、色を持つ化合物には炭素、窒素、酸素の不飽和結合が含まれることを発見した。その後、ドイツ人化学者ウィット (O.N.Witt) が学説として纏め、ウィットの発色団説と呼ばれるようになった。この理論に基づき研究と実用化が進められ、19世紀終わりから20世紀初頭にかけて石炭化学工業を元にした染料化学工業が勃興した。
1876年にウィットは色を発現する化学構造に発色団(はっしょくだん、chromophore)という名称を与え、呈色の原因として必要な原子団を色原体(しきげんたい、chromogen)、染色性を高める為の置換基を助色団(じょしょくだん、auxochrome)と命名し、両者から色素が構成されるとした。ウィットは次の原子団を色原体とした。
- >C=C<、>C=O、>C=N-、>N=N<、-N=O
そして、次の置換基を助色団とした。
- -CH3、-OH、-NH2、-NHCH3、-COOH
また、1888年にイギリスのアームストロング (H.E.Armstrong) は呈色には分子内にキノン構造を持つ必要があるとしたキノン説を提唱した。これは発色団説の特定の場合であると考えられる。
その後、呈色の説明として分子軌道法による機構に発色団説はとって代わられた。したがって、今日の発色団や助色団の意味はウィットの提唱した当時とは異なる。分子軌道法による呈色機構は後に詳説するとして、今日において発色団の意味は、不飽和結合系に作用して共役系を延長したり電荷の偏りを偏重させる原子団を指す。例を次に挙げる。
- >C=C<、>C=O、>C=N-、-N=N- (>N-N<)、-N=O、-N-O-、-NO2
また今日における助色団は塩を形成することで染色性を助け、且つ共役系に対して電子供与性あるいは電子求引性を示す置換基を指す。その多くは非共有電子対を持つ電子供与性置換基である。例を次に挙げる。
- -CH3、CN、-COOH、-O-、-OH、-OR、-NH2、-NR2、-Cl、-Br、-NO2、-SO3H
したがって、助色団も積極的に呈色に関与しており、概念上は発色団に含まれるが、呈色に関わる主たる原子団を発色団と呼ぶ。
分子軌道論による発色機構
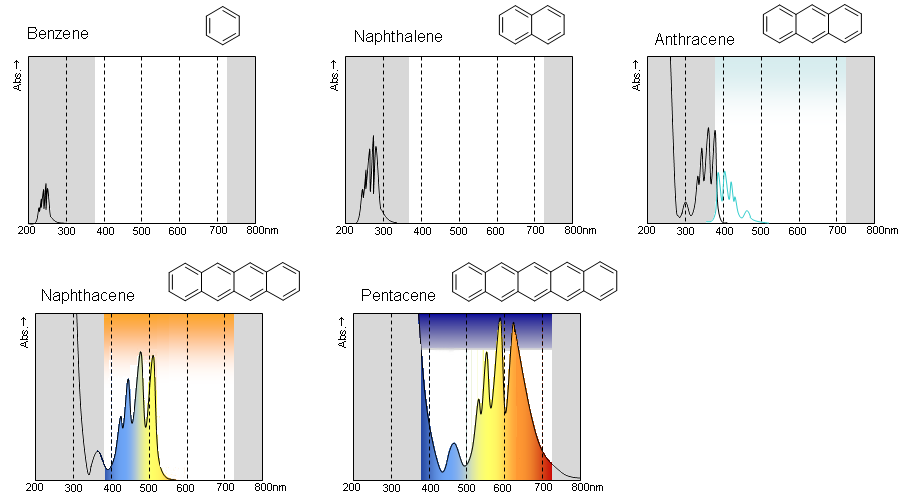
発色団説は染料化学に対して多大な影響を与えたが、物理学理論に基づいて光学的物性を説明するものではなく、また染料化学が発展するにつれ食い違う例も多く見られるようになった。今日では有機色素の呈色の多くは、共役π電子系が置換効果によりその吸収スペクトルを移動させたり、吸収強度を増大させることで物質の可視領域の吸収が増大して呈色すると考えられている。一般に長大な共役π電子系はより長波長側に吸収帯を持つ。次に縮合芳香環の環の数と極大吸収波長の例を示す[要出典]。
- ベンゼン(無色) - 255nm
- ナフタレン(無色) - 286nm
- アントラセン(淡青色) - 375nm
- ナフタセン(橙色) - 477nm(可視領域に極大吸収)
- ペンタセン(濃紺) - 575nm(可視領域に極大吸収)
上のグラフの吸収度は量子収率を加味して模式図としてスケーリングして示している。可視領域の上部には透過光の色を示し、可視領域以外の部分は灰色で示している。ベンゼンおよびナフタレンは可視領域に吸収を持たないために無色である。アントラセンは可視領域に吸収を持たないが、可視領域に蛍光を持つ為に淡青色に呈色している。ナフタセンは紫〜黄色にかけて吸収を持つ為に補色である橙色に呈色する。ペンタセンは可視領域全般に強い吸収を持つものの、青色領域に吸収の極小値を持つ為に濃紺色に呈色する。
また、前述のように、多くの置換基が置換基効果により吸収スペクトルに作用する。したがって発色団や助色団の構成によっては比較的短い共役π電子系であっても強く呈色する。
配位子吸収帯
遷移金属元素を含む化合物で、配位子場の作用で内殻の不対電子の励起による配位子吸収帯が可視領域と合致して発色する場合があり、結晶場着色とも呼ばれる。代表的な例ではルビーが挙げられる。ルビーはコランダムを構成しているAlの一部がCr3+に置換した構造を持つ。配位子場の影響でCr3+の内殻励起は紫と黄緑に配位子吸収帯を持ち、透過光は赤色に見える。同様な例として、他にもエメラルド、ヒスイ、アクアマリン、トルコ石、クジャク石あるいはザクロ石などが挙げられる。
電荷移動吸収帯
異なる金属イオン間の電荷移動や分子軌道間の電子遷移のエネルギーに起因する電荷移動吸収帯が可視領域と合致して発色する場合がある。たとえばサファイアはコランダムに不純物として含まれたFe2+とTi4+のイオン間で電子遷移が発生する際に約2電子ボルトのエネルギー差がある。その為、電荷移動吸収帯は黄色から赤にかけて吸収を持ち、透過光は青色を示す。同様な機構で酸化鉄Fe3O4、鉛丹Pb3O4も呈色することが知られている。
エネルギー帯間遷移
金属や半導体などバンド理論で説明されるエネルギー帯を持つ物質の一部に、禁止帯幅が可視領域に合致する為に色として現れる光学的性質を持つ物質も存在する。
例えば、辰砂(硫化水銀(II))は禁止帯幅が2.1電子ボルトである。そして、黄色以上の光エネルギーは電子の励起に利用されるので吸収され、それ以外は反射されるので赤く見える。カドミウムイエロー (CdS) は2.6電子ボルトで紫以上が吸収されて黄色に、セレン化カドミウムは1.6電子ボルトで可視領域すべてが吸収されるため黒ずんで見える。
色素と同じ種類の言葉
- >> 「色素」を含む用語の索引
- 色素のページへのリンク