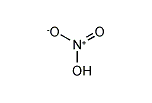
硝酸
英語:nitric acid
「硝酸」とは、化学式「HNO3」で表される無色透明で強い酸化作用をもつ有毒かつ有腐食性の液体もしくはその水溶液のことである。オストワルト法(アンモニアを酸化する手法)によって工業的に生産され、酸化剤などに利用されている。
硝酸の特徴
硝酸は常態では無色透明の液体で、刺激臭を発する。塩酸や硫酸と同じく強酸としての性質を持ち、強い酸化作用をもつ。腐食性もあり人体に有毒。「消防法」では危険物(第6類)に、「毒物及び劇物取締法」においては「劇物」(法定劇物)に指定されている。硝酸の用途
硝酸は化学産業における重要な物質である。典型例としてはニトログリセリンの生成が挙げられる。液体燃料ロケットでは液体燃料(ヒドラジン等)と混合される酸化剤に硝酸が用いられる。ごく低濃度の硝酸は肥料の原料としても用いられている。硝酸の種類
硝酸(の水溶液)のうち硝酸の濃度の高いものを「濃硝酸」といい、同じく濃度の低いものを「希硝酸」ということがある。何パーセントから濃硝酸・希硝酸に該当するのかという数値的な明確な線引き(定義)があるわけではないが、おおよそ20~30パーセント程度以下の濃度なら希硝酸と呼ばれることが多く、60~70パーセント以上の濃度なら濃硝酸と呼ばれることが多い。派生
・硝酸エステル:硝酸のエステル。硝酸とアルコールから生成される。・硝酸塩:硝酸の塩(えん)。硝酸イオンが結合した塩類の総称。
硝酸
硝酸
硝酸
(Nitric acid から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/07/15 13:11 UTC 版)
硝酸(しょうさん、英: nitric acid、独: Salpetersäure)は窒素のオキソ酸で、化学式 HNO3 で表される。代表的な強酸の1つで、様々な金属と反応して塩を形成する。有機化合物のニトロ化に用いられる。硝酸は消防法第2条第7項及び別表第一第6類3号により危険物第6類に指定され、硝酸を 10 % 以上含有する溶液は医薬用外劇物にも指定されている。
注釈
- ^ 濃度は特に定義されているわけではないが、実験室で用いる希硝酸は通常 6 mol/dm3 (32 %, d = 1.19 g · cm-3)、あるいはそれ以下のものであることが多い。
出典
- ^ a b c 厚生労働省モデルSDS
- ^ a b c FA コットン, G. ウィルキンソン著, 中原 勝儼訳 『コットン・ウィルキンソン無機化学』 培風館、1987年,原書:F. ALBERT COTTON and GEOFFREY WILKINSON, Cotton and Wilkinson ADVANCED INORGANIC CHEMISTRY A COMPREHENSIVE TEXT Fourth Edition, INTERSCIENCE, 1980.
- ^ D.F.SHRIVER, P.W.ATKINS, INORGANIC CHEMISTRY Third Edition, 1999.
- ^ シャロー 『溶液内の化学反応と平衡』 藤永太一郎、佐藤昌憲訳、丸善、1975年
- ^ D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982)
- ^ 山崎一雄他 『無機溶液化学』 南江堂、1968年
- ^ 化学大辞典編集委員会 『化学大辞典』 共立出版、1993年
- ^ a b 『改訂4版化学便覧基礎編Ⅱ』 日本化学会編、丸善、1993年
- ^ 田中元治 『基礎化学選書8 酸と塩基』 裳華房、1971年
- ^ 経済産業省生産動態統計年報 化学工業統計編
- ^ a b c d e 米田幸夫 著、化学大辞典編集委員会(編) 編『化学大辞典』 1巻(縮刷版第26版)、共立、1981年10月、531-532頁頁。
- Nitric acidのページへのリンク