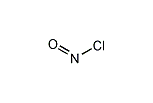オキシ塩化窒素
塩化ニトロシル
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2018/08/18 23:33 UTC 版)
Jump to navigation Jump to search| 塩化ニトロシル | |
|---|---|
 |
|
 |
|
|
塩化ニトロシル |
|
|
別称
オキシ塩化窒素
塩化ニトロソニウム |
|
| 識別情報 | |
| CAS登録番号 | 2696-92-6 |
| E番号 | E919 (その他) |
|
|
| 特性 | |
| 化学式 | NOCl |
| モル質量 | 65.46 g/mol |
| 外観 | 黄色気体、赤色液体 |
| 密度 | 1.417g/cm3、液体 @-12℃ 2.99g/L、気体 |
| 融点 | -59.6℃ |
| 沸点 | -6.4℃ |
| 水への溶解度 | 分解 |
| 構造 | |
| 分子の形 | sp2 at N |
| 双極子モーメント | 1.90D |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 1580 |
| 主な危険性 | 毒性が大きい |
| 関連する物質 | |
| 関連物質 | 次亜硝酸 (ニトロシル) フッ化ニトロシル 臭化ニトロシル |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
塩化ニトロシル(えんかニトロシル、nitrosyl chloride)は、化学式 NOCl の無機化合物である。広く一般に、王水の分解によって生成する。ハロゲン化ニトロシルは他にフッ化ニトロシル、臭化ニトロシルが知られている。
性質
黄赤色の気体で、強い酸化力を持ち、塩酸や硝酸に溶かしても反応しない金や白金も、NOClによって酸化されて塩化金や塩化白金が生じる。塩素化・ニトロ化・酸化反応を起こす。ただしタンタル、イリジウムは酸に対しての耐性が極めて高いため、塩素化できない(イリジウムは粉末にすればわずかに反応する)。
構造
化学式はNOClであるが、構造を考慮するとONClと書いた方が適している。NとOの結合は二重結合でその結合距離は1.16 Å、NとClの結合は単結合でその結合距離は1.69 Åである。また、O-N-Clの結合角は113°である[1]。
合成
NOClは活性炭のもとで一酸化窒素と塩素を作用させて発生させる。または、硫酸水素ニトロシルと塩酸から合成することもできる。
-
 この項目は、化学に関連した書きかけの項目です。この項目を加筆・訂正などしてくださる協力者を求めています(プロジェクト:化学/Portal:化学)。
この項目は、化学に関連した書きかけの項目です。この項目を加筆・訂正などしてくださる協力者を求めています(プロジェクト:化学/Portal:化学)。
- 塩化ニトロシルのページへのリンク