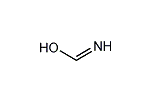
ホルムアミド
ホルムアミド
(メタンアミド から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/08/26 19:36 UTC 版)
| ホルムアミド | |
|---|---|
 |
|
 |
 |
|
Methanamide
|
|
|
別称
Carbamaldehyde
|
|
| 識別情報 | |
| CAS登録番号 | 75-12-7  |
| PubChem | 713 |
| ChemSpider | 693  |
| UNII | 4781T907ZS  |
| KEGG | C00488  |
| ChEBI | |
| ChEMBL | CHEMBL266160  |
| 4739 | |
|
|
|
|
| 特性 | |
| 化学式 | CH3NO |
| モル質量 | 45.04 g/mol |
| 外観 | 無色の油状液体[2] |
| 密度 | 1.133 g/cm3 |
| 融点 | 2 - 3 °C, 272 K, 29 °F |
| 沸点 | 210 °C, 483 K, 410 °F |
| 水への溶解度 | 混和 |
| 蒸気圧 | 0.08 mmHg at 20 °C |
| 酸解離定数 pKa | 23.5 (DMSO中)[3] |
| 磁化率 | −2.19×10−5 cm3/mol |
| 危険性 | |
| NFPA 704 | |
| 引火点 | 154 °C (309 °F; 427 K) (closed cup) |
| 許容曝露限界 | 無し[2] |
| 関連する物質 | |
| 関連物質 | カルバミン酸 ジメチルホルムアミド |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ホルムアミド(Formamide)はギ酸から誘導されるアミドである。水と任意の割合で混ざり合う透明な液体で、アンモニア臭がする。サルファ薬の製造やビタミンの合成に使われ、紙や繊維の柔軟剤としても使われる。水に不溶の様々なイオン性化合物を溶かし、溶媒として用いられる。
製造
古典的には、ギ酸とアンモニアを反応させてギ酸アンモニウムを作り、これを熱して脱水することによりホルムアミドを合成する。
- メタンアミドのページへのリンク