すい‐そ【水素】
水素
水素
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/08/04 15:53 UTC 版)

|
|||||||||||||||||||||||||
| 外見 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
無色の気体[1] プラズマ状態の紫色の輝き |
|||||||||||||||||||||||||
| 一般特性 | |||||||||||||||||||||||||
| 名称, 記号, 番号 | 水素, H, 1 | ||||||||||||||||||||||||
| 分類 | 非金属 | ||||||||||||||||||||||||
| 族, 周期, ブロック | 1, 1, s | ||||||||||||||||||||||||
| 原子量 | 1.00794(7) | ||||||||||||||||||||||||
| 電子配置 | 1s1 | ||||||||||||||||||||||||
| 電子殻 | 1(画像) | ||||||||||||||||||||||||
| 物理特性 | |||||||||||||||||||||||||
| 色 | 無色[1] | ||||||||||||||||||||||||
| 相 | 気体 | ||||||||||||||||||||||||
| 密度 | (0 °C, 101.325 kPa) 0.08988[1] g/L |
||||||||||||||||||||||||
| 融点 | 14.01[1] K, −259.14[1] °C | ||||||||||||||||||||||||
| 沸点 | 20.28[1] K, −252.87[1] °C | ||||||||||||||||||||||||
| 三重点 | 13.8033 K (−259 °C), 7.042 kPa | ||||||||||||||||||||||||
| 臨界点 | 32.97 K, 1.293 MPa | ||||||||||||||||||||||||
| 融解熱 | (H2) 0.117 kJ/mol | ||||||||||||||||||||||||
| 蒸発熱 | (H2) 0.904 kJ/mol | ||||||||||||||||||||||||
| 熱容量 | (25 °C) (H2) 28.836 J/(mol·K) | ||||||||||||||||||||||||
| 蒸気圧 | |||||||||||||||||||||||||
|
|||||||||||||||||||||||||
| 原子特性 | |||||||||||||||||||||||||
| 酸化数 | 1, −1 (両性酸化物) |
||||||||||||||||||||||||
| 電気陰性度 | 2.20(ポーリングの値) | ||||||||||||||||||||||||
| イオン化エネルギー | 1st: 1312.0 kJ/mol | ||||||||||||||||||||||||
| 共有結合半径 | 31±5 pm | ||||||||||||||||||||||||
| ファンデルワールス半径 | 120 pm | ||||||||||||||||||||||||
| その他 | |||||||||||||||||||||||||
| 結晶構造 | 六方晶系 | ||||||||||||||||||||||||
| 磁性 | 反磁性[3] | ||||||||||||||||||||||||
| 熱伝導率 | (300 K) 0.1805 W/(m⋅K) | ||||||||||||||||||||||||
| 音の伝わる速さ | (gas, 27 °C) 1310 m/s | ||||||||||||||||||||||||
| CAS登録番号 | 12385-13-6 1333-74-0 (H2)>[2] |
||||||||||||||||||||||||
| 主な同位体 | |||||||||||||||||||||||||
| 詳細は水素の同位体を参照 | |||||||||||||||||||||||||
|
|||||||||||||||||||||||||
水素(すいそ、英: hydrogen、羅: hydrogenium、仏: hydrogène、独: Wasserstoff)は、原子番号1の元素である。元素記号はH。原子量は1.00794[1]。非金属元素のひとつである。
ただし、一般的に「水素」と言う場合、元素としての水素の他にも水素の単体である水素分子(水素ガス)H2、1個の陽子を含む原子核と1個の電子からなる水素原子、水素の原子核(ふつう1個の陽子、プロトン)などに言及している可能性があるため、文脈に基づいて判断する必要がある。
名称

1783年、ラヴォアジエが「 音声、イドロジェーヌ(hydrogène)」と命名した[1]。ギリシア語の 「ὕδωρ=『水』」と 「γεννάν=『生む』『作り出す』」を合わせた語で、水を生むものを意味する[1]。英語では「
音声、イドロジェーヌ(hydrogène)」と命名した[1]。ギリシア語の 「ὕδωρ=『水』」と 「γεννάν=『生む』『作り出す』」を合わせた語で、水を生むものを意味する[1]。英語では「 音声、ハイドロジェン(hydrogen)」という。
音声、ハイドロジェン(hydrogen)」という。
日本語の「水素」は、オランダ語「 音声、ワーテルストフ(waterstof)」の意訳である。宇田川榕菴が書いた『舎密開宗』で初めて用いられた。ドイツ語の「
音声、ワーテルストフ(waterstof)」の意訳である。宇田川榕菴が書いた『舎密開宗』で初めて用いられた。ドイツ語の「 音声、ヴァッサーシュトフ(Wasserstoff)」も同じ構成の複合語である。朝鮮語でも同じく水素(ハングル:수소
音声、ヴァッサーシュトフ(Wasserstoff)」も同じ構成の複合語である。朝鮮語でも同じく水素(ハングル:수소  音声)と称する。
音声)と称する。
中国語ではその気体としての軽さから「軽」の旁を用いて「氫」(拼音:  音声)という字があてられている。
音声)という字があてられている。
詳細は「元素の中国語名称」を参照
歴史
1671年に、ロバート・ボイルが鉄と希硝酸を反応させて生じる気体が可燃性であることを記録している[1]。1766年、ヘンリー・キャヴェンディッシュが水素を気体として分離し、発見した。
量子力学における役割
陽子1つと電子1つからなるシンプルな構造ゆえ、原子構造論の発展において水素原子は中心的な役割を果たしてきた。事実、量子力学の入門として、水素原子や水素様分子をまず取り扱う教科書がほとんどである。
分布
水素は宇宙でもっとも豊富に存在する元素であり、(ダークマターとダークエネルギーを除いた)宇宙の質量の4分の3を占め[4]、総量数比では全原子の90 %以上となる[5]。これらのほとんどは星間ガスや銀河間ガス、恒星あるいは木星型惑星の構成物として存在している。
水素原子は宇宙が誕生してから約38万年後[6]に初めて生成したとされている。それまでは陽子と電子がバラバラのプラズマ状態で光は宇宙空間を直進できなかったが、電子と陽子が結合することにより宇宙空間に散乱されずに進めるようになった。これを「宇宙の晴れ上がり」という。
宇宙における主系列星のエネルギー放射のほとんどはプラズマとなった4個の水素原子核がヘリウムへ核融合する反応によるもので、比較的軽い星では陽子-陽子連鎖反応、重い星ではCNOサイクルという過程を経てエネルギーを発生させている。水素原子はいずれの核融合反応においてもこれを起こす担い手である[7]。太陽の組成に占める水素の割合は約73 %[注 1]である[8][9]。
地球表面の元素数では酸素・珪素に次いで3番目に多いが[1]、水素は質量が小さいため、質量パーセントで表すクラーク数では9番目となる[要出典]。地球表面の元素数ではほとんどは海水の状態で存在し[1]、単体の水素分子状態では天然ガスの中にわずかに含まれる程度である[要出典]。海水における推定存在度は1 Lあたりに108 g、地球の地殻における推定存在度は1 kgあたり1.4 gであり[10]、また空気中にも含まれるがごく微量であり、存在比率は容積比で5×10の−5乗%、重量比で3×10の−6乗である[11]。宇宙空間に散逸する地球の大気は少ないが、それでも1秒あたり水素が3 kg、ヘリウムが50 gずつ放出されている。これは大気が薄く原子や分子の速度が減速されずに宇宙へ飛び出すジーンズエスケープや、イオン状態の荷電粒子が地球磁場に沿って脱出する現象がある。なお、加熱された粒子がまとまって流出するハイドロダイナミックエスケープや太陽風が持ち去るスパッタリングは現在の地球では起きていないが、地球誕生直後はこの作用によって水素が大量に散逸したと考えられる[12]。
固有磁場を持たない金星は、現在でもハイドロダイナミックエスケープやスパッタリングが続き、地表には比較的重いため残った酸素や炭素が作る二酸化炭素が大気のほとんどを占め、水がない非常に乾燥した状態にある。火星も軽い水素を中心に散逸し、かろうじて氷となった水が極部分の土中に残るにとどまる[12]。
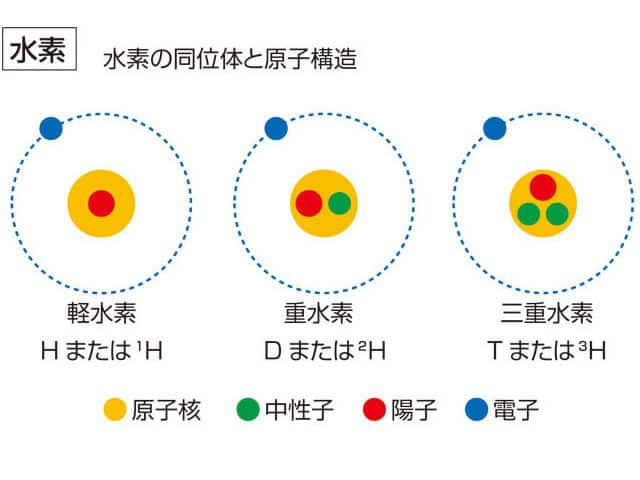
同位体

質量数が2(原子核が陽子1つと中性子1つ)の重水素(2H)、質量数が3(原子核が陽子1つと中性子2つ)の三重水素(3H)等と区別して、質量数が1(原子核が陽子1つのみ)の普通の水素(1H)を軽水素とも呼ぶ。

天然の水素には、水素(軽水素、プロチウム)1H、重水素 2H (デュウテリウム、ジューテリウム[13]、略号D)、三重水素 3H (トリチウム、略号T)の3つの同位体が知られている[1]。このうち、もっとも軽い 1H は、1つの陽子と1つの電子のみによって構成されており、原子の中で中性子を持たない核種の1つである。存在が確認されている中でほかに中性子を持たない核種はリチウム3のみである。それぞれの同位体は質量の差が2倍、3倍となり、性質の違いも大きい。たとえばD2はH2よりも融点や沸点が高くなり、溶融潜熱は倍近くに、蒸気圧は10分の1近くとなる[14]。2013年現在、より重い同位体は水素4から水素7までが確認されている。もっとも重い水素7(原子核は陽子1、中性子6よりなる)はヘリウム8を軽水素に衝突させることで合成されている。質量数が4以上のものは寿命がきわめて短く、たとえば水素7では半減期が23 ys(= 2.3×10−23 s)ほどしかない[15]。

水素の同位体は、それぞれの特徴を有効に活かした使い方をされる。重水素は原子核反応での用途で、中性子の減速に使用され、化学や生物学では同位体効果の研究、医療では診断薬の追跡[13]に使用されている。また、三重水素は原子炉内で生成され、水素爆弾の反応物質や核融合燃料、放射性を利用したバイオテクノロジー分野でのトレーサーや発光塗料の励起源として使用されている。
水素分子

水素分子は、常温常圧では無色無臭の気体として存在する、分子式 H2で表される単体である。分子量2.01588、融点 −259.14 °C(常圧)、沸点 −252.87 °C(常圧)、密度 0.0899 g/L、比重 0.0695(空気を 1 として)、臨界圧力 12.80 気圧、水への溶解度 0.021 mL/mL(0 °C)。最も軽い気体である。原子間距離は 74 pm、結合エネルギーはおよそ 435 kJ/mol[2]。
水素分子は常温では安定であり、フッ素以外とは化学反応をまったく起こさない。しかし何かしらの外部要因があればその限りではなく、たとえば光がある状態では塩素と激しい反応を起こす[14][2]。また、水素と酸素を混合したものに火をつけると起きる激しい爆発(水素爆鳴気)は、混合比下限は4.65 %、上限は93.3 %であり、空気との混合では4.1 – 74.2 %となり、これはアセチレンに次ぐ広い爆発限界の範囲を持つ[2]。
ガス密度が低い水素は速い速度で拡散する性質を持ち、また燃焼時の伝播も速い。そのため、ガス漏れを起こしやすい傾向にある[2]。原子径の小ささから、金属材料に侵入し機械的特性を低下させる(水素脆化)傾向が強い。これは高温高圧環境下で顕著となり、封入容器の材質には注意を払う必要がある。−250 °C以下で液化させると体積は 800分の1となり、さらに軽いため低温貯蔵性には優れる[16]。
ガス惑星の内部など非常に高い圧力下では性質が変わり、液状の金属になると考えられている。逆に宇宙空間など非常に圧力が低い場合、H2+やH3+、単独の水素原子などの状態も観測されている。H2分子形状の雲は星の形成などに関係があると考えられており、特に新生惑星や衛星の観察時にはそれを注視することが多い。
オルト水素とパラ水素
水素分子は、それぞれの原子核(プロトン)の核スピンの配向により、オルト(ortho)とパラ(para)の2種類の異性体が存在する[14]。オルト水素は、互いの原子核のスピンの向きが平行で、パラ水素ではスピンの向きが反平行である。この2つは、化学的性質に違いがないが、物理的性質(比熱や熱伝導率など)がかなり異なる。これは内部エネルギーにある差によるもので、パラ水素側が低い[14]。統計的な重みが大きいほうをオルトと呼ぶ。
常温以上では、オルト水素とパラ水素の存在比はおよそ3:1であるが、低温になるほどパラ水素の存在比が増し、絶対零度付近ではほぼ100パーセントパラ水素となる[14]。ただし、このオルト-パラ変換はスピン反転を伴うために、触媒を用いない場合極めて遅く、触媒を用いずに水素を液化すると、液化した後もオルト-パラ変換に伴い両者のエネルギー差に相当する熱が発生するため、液化水素が気化してしまう。これを水素のボイル・オフ問題という。[17]オルト‐パラ変換を起こす触媒は、活性炭や鉄などの金属の一部、常磁性物質またはイオンなどがある[14]。
イオン
金属水素
 |
この節は検証可能な参考文献や出典が全く示されていないか、不十分です。 (2021年4月)
|
水素は、ガス惑星の内部など非常に高い圧力下では性質が変わり、液状の金属になると考えられているが、1996年にローレンス・リバモア国立研究所のグループが、140 GPa(1 GPa = 約1万気圧)、数千°Cという状態で、100万分の1秒以下という短寿命ではあるが、液体の金属水素を観測したと報告している[18][19]。木星型惑星(木星・土星)の深部は非常に高い圧力になっており、液体金属水素が観測された条件と似ている。木星型惑星を構成するもっとも主要な元素のひとつである水素は、この状況下では金属化している可能性があり、惑星の磁場との関わりも指摘されている[20]。しかしながら、2017年現在、数百GPaのオーダーで圧力を加える実験が行われているものの、固体の金属水素が得られたという十分な証拠が示されたことはない[21][22][注 2]。
金属化そのものが達成されていないためにその真偽はいまだ不明であるが、Ashcroft (1968, p. 1748) は、金属化した水素は室温超伝導を達成するのではないかと予想している。この可能性の傍証として、周期表で水素のすぐ下のリチウムは、30 GPa以上という超高圧下で超伝導状態となることが示されている。リチウムの超伝導への転移温度は圧力48 GPaで20 K程度であるが、この数字は単体元素のものとしては高い部類に入り、いくつかの例外を除けば一般に軽い元素ほど転移温度は高くなるため、もっとも軽い元素である水素は、より高い転移温度を持つ可能性が十分ある。
また、励起状態の水素が金属化するときわめて強力な爆薬になるとの理論計算が行われ、電子励起爆薬として研究されている。この理論では圧力だけでは不十分であり、水素を励起状態にして圧力をかければ金属化するとしている。
物理的性質


元素およびガス状分子の中でもっとも軽く[2]、また宇宙でもっとも数が多く[1]、珪素量を106とした際の比率は2.79×1010である。[24]地球上では水や有機化合物の構成要素として存在する。
水素分子は常温・常圧では無色無臭の気体で、非常に軽く、非常に燃焼・爆発しやすいといった特徴を持つ。そのため日本では、高圧ガス保安法容器保安規則により、赤色のボンベに保管するように決められている[2]。従来、水素ガスの爆発濃度は4 % – 75 %であるとされてきたが[25]、慶應義塾大学環境情報学部の武藤佳恭は、10 %以下であれば爆発しないことを明らかとした[26]。
化学的性質
水素化物
| 化学式 | IUPAC組織名[27] | 慣用名 |
|---|---|---|
| BH3 | ボラン | 水素化ホウ素 |
| CH4 | カルバン | メタン |
| NH3 | アザン | アンモニア |
| H2O | オキシダン | 水 |
| HF | フッ化水素 | |
| AlH3 | アラン | 水素化アルミニウム |
| SiH4 | シラン | 水素化ケイ素 |
| PH3 | ホスファン | ホスフィン 水素化リン |
| H2S | スルファン | 硫化水素 |
| HCl | 塩化水素 | |
| GaH3 | ガラン | 水素化ガリウム |
| GeH4 | ゲルマン | 水素化ゲルマニウム |
| AsH3 | アルサン | アルシン 水素化ヒ素 |
| H2Se | セラン | セレン化水素 |
| HBr | 臭化水素 | |
| SnH4 | スタナン | 水素化スズ |
| SbH3 | スチバン | スチビン 水素化アンチモン |
| H2Te | テラン | テルル化水素 |
| HI | ヨウ化水素 | |
| PbH4 | プルンバン | 水素化鉛 |
| BiH3 | ビスムタン | ビスムチン 水素化ビスマス |
水素は電気陰性度が2.2とアルカリ金属やアルカリ土類金属よりも高くハロゲンよりも小さい値であり、酸化剤としても還元剤としても働く。このため非金属元素とも金属元素とも親和しやすい。たとえば、水素と酸素が化合するときには還元剤として働き、爆発的な燃焼とともに水H2Oを生じる。ナトリウムと水素との反応では酸化剤として働き、水素化ナトリウムNaHを生じる。このような水素とほかの元素が化合した物質を水素化物という[28]。
水素化物の結合には、イオン結合型・共有結合型のほかに、パラジウム水素化物などの侵入型固溶体(侵入型化合物)と呼ばれる3種類の形態がある[28]。イオン結合型の化合物の中では、水素はH−イオン(ヒドリドイオン)として存在する。共有結合型は電気陰性度が高いPブロック元素と電子を共有して化合する[28]。侵入型固溶体は一種の合金であり、水素原子は金属原子の隙間にはまり込むように存在している。このため、容易かつ可逆的に水素を吸収・放出することができ、水素吸蔵合金に利用される。高性能な水素吸蔵合金の中には、水素原子の密度が液体水素のそれに匹敵したり、上回るものもある。
一方、より電気陰性度の大きい元素との化合物では水素はH+イオンとなる。水中で水素イオンを生じる物質が狭義の酸である。水溶液中では水素イオンは、H+(ヒドロン)ではなく、水分子と結合してH3O+(オキソニウムイオン) として振る舞う。
水素はまた、炭素と結合することで、さまざまな有機化合物を形成する。ほとんどすべての有機化合物は構成原子に水素を含む。
おもな元素の水素化物の化学式と国際純正応用化学連合(IUPAC)による組織名、および(存在するものは)慣用名を表「元素の水素化物」に示す。
核磁気共鳴法における利用
分子構造の研究に非常によく利用される核磁気共鳴分光法(NMR)において、1Hを用いた方法は代表的である。1Hはすべての核種の中で最も強い特異吸収を示すうえ、水素はほとんどすべての有機化合物に含まれることもあり、NMRにおいてよく利用される。周囲の原子の電子から影響を受ける結果、吸収される周波数が変化する(化学シフト)ため、原子の相対位置を推測する有力な手掛かりとなる。
水素イオンと水素化物イオン
水素のイオンには、陽イオンである水素イオン(hydron、ヒドロンまたはハイドロン)と、陰イオンの水素化物イオン(hydride、ヒドリドまたはハイドライド)とが存在する。1H+はプロトン(陽子)そのものであるが、一般に水素は同位体混合物なので、水素の陽イオンに対する呼称としてはヒドロンが正確である(すなわちヒドロンは H+、D+、T+の総称である)。しかし、化学の領域において単に「プロトン」と呼ぶ際は水素イオンを指し示していると考えて差し支えはない。
水素イオンの濃度[H+]は酸性度を定量的に表す指標として用いられ、mol/L(モル毎リットル)単位で表した水素イオンの濃度の数値の対数に負号をつけた値を水素イオン指数(pH)で表す。水中の[H+]濃度は1から10−14mol/L程度の広い範囲を取り、pHでは0 – 14 程度となる。常温で中性の水には約10−7mol/Lの水素イオンが存在し、pHは約7となる[1]。
ヒドロン・プロトンとヒドロニウムイオン
H+であれ D+であれ、ヒドロンは電子殻を持たないむき出しの原子核であるため、化学的にはファンデルワールス半径を持たない正の点電荷のように振る舞う。それゆえ通常は単独で存在せず、溶媒などほかの分子の電子殻と結合したヒドロニウムイオン(hydronium ion)として存在する。水素のイオン化エネルギーは1131 kJ/mol、遊離状態の水素イオンの水和エネルギーは1091 kJ/molと見積もられており[28]、これは高い電子密度に起因する、水分子との高い親和力を示すものである。
-
[H-]
ヒドリド(別名、水素化物イオン、ヒドリドイオン[32][33][34]、英: hydride、英: hydrogen anion、化学記号H−とも表記される)は、アルカリ金属、アルカリ土類金属あるいは第13族、14族元素(共有結合性が強い)などの、電気的に陽性な元素の水素化物が電離する時に生成する水素の陰イオン(アニオン)。ヒドリドはK殻が閉殻した電子配置を持ちヘリウムと等電子的であるために、一定の大きさを持ったイオンとして振る舞う点でヒドロン(水素カチオン)とは異なる。実際、ヒドリドはフッ素アニオンよりもイオン半径が大きいように振る舞う。
ヒドリドはきわめて弱い酸でもある水素分子(pKa=35)の共役塩基であるので、強塩基として振る舞う。
ヒドリドは塩基として作用する場合と還元剤として作用する場合がある。これをヒドリド還元というが、それは金属と還元を受ける化合物との組み合わせにより変化する。ヒドリドの標準酸化還元電位は−2.25Vと見積もられている。
-

スペースシャトルのメインエンジン。1機を打ち上げるには150万リットルの液体水素が使われる[41]。 代表的な用途
- 原料 - アンモニアの製造(ハーバー・ボッシュ法)[14]のほか、塩素ガスと混合し光を当てて反応させる塩酸の製造[1]、油脂に添加して炭素同士の二重結合数を減らし固体化する改質(トウモロコシ油や綿実油のマーガリン化など)[1]、脱硫など、多方面に利用されている。
- 還元剤 - 金属鉱石(酸化物)の還元[1]、ニトロベンゼンを還元しアニリンの製造、ナイロン66製造におけるベンゼンの触媒還元、一酸化炭素を還元するメチルアルコール合成などに使われる[14]。
- 燃料 - 燃やしても水以外の排出物(粒子状物質や二酸化炭素などの排ガス)を出さないことから、代替エネルギーとして期待されている[16]。ただし、燃焼条件により窒素酸化物が生成することは不可避である。内燃機関の燃料として水素燃料エンジンを積んだ水素自動車が発売されているほか、ロケットの燃料や燃料電池に使用されている。おもに燃料電池自動車向けの「水素ステーション」の設置が始まっている。
[42] Pininfarina H2 Speedなどのスポーツカーにも使用される。
上記で述べたように、水素ガスの生産は原料を化石燃料に依存しており、水蒸気改質により発生する一酸化炭素などのうち化成品に利用されない過剰分や燃料として利用される炭化水素は二酸化炭素として環境中に放出される。水素の原料が化石燃料である限りにおいては、水素を化石燃料の代替として利用してもそのまま化石燃料の消費量が削減されたり二酸化炭素の発生が抑えられたりすることにはならない。
- 浮揚ガス - 1 Lの水素を詰めた風船は1.2 gの質量を浮揚させる[1]。この性質から気球や飛行船などに用いられていたが、ヒンデンブルク号爆発事故が起きて以来、危険性の少ないヘリウムで代用されるようになった。なお、この事故の直接的原因は外皮の塗料への引火とされている。
- 冷却剤 - 液体水素は超伝導現象を含む低温学の調査に使用される。また、一部の発電所では、水素ガスを冷却媒体として用いている発電機もある。これは空気よりも熱伝導率が7倍[1]、比熱が約14倍と高く、風損が小さい特性を利用している。一方で、空気の混入による爆発を防ぐため水素濃度を90%以上に維持する必要があるほか、水素ガスが漏れないよう水素ガス圧力よりも高い圧力の油を軸とシールリング内のすき間に充填しなければならないという作業が発生する[45]。
- 洗浄 - 工業分野では、半導体の洗浄はRCA洗浄が主流で、アンモニアや塩酸フッ化物が用いられるが、その代替として水素を水に溶かし込んだ水溶液は排水処理の面で環境負荷が低く[46]、半導体の基板表面の微粒子除去・洗浄に用いられる[47]。
- 溶接 - 水素分子をいったん2つの水素原子に解離させ、それを再結合させると多量の熱を発生する。これを利用した金属溶接法がある[14]。
- その他 - テクニカルダイビングや軍隊などで大深度潜水時の使用が試みられたが、同時に酸素も用いられるために爆発の可能性が使用中につきまとうなど、危険であるため使用されていない。
- 標準水素電極が標準電極電位の基準として用いられている。
エネルギー利用
→「水素燃料」を参照水素は燃焼すると水(水蒸気)となり、温室効果ガスとされる二酸化炭素や大気汚染物質を排出しない。現状では、化石燃料を使って製造しているものの、将来的には、水の電気分解やバイオマス・ごみなどを利用することにより、化石燃料によらないで製造できる可能性がある。このため、将来性の高いエネルギーの輸送および貯蔵手段として期待される[16]。
水素はさまざまな利用法が考えられている。燃焼を直接使う方法としては水素自動車が挙げられるほか、火力発電の燃料に水素を混ぜて二酸化炭素などを減らす技術が研究されている[48]。
水素を言わば「電池」として利用することも考えられている。鉛蓄電池、リチウム電池、NAS電池など、比較的大きな容量の充電が可能な電池がいろいろと開発されてきたものの、それでも電気エネルギーは貯めておくのが比較的困難なエネルギーとして知られている。そこで、必要以上の電力が得られるときに水を電気分解して生産した水素を貯蔵し、電力が必要となった時に貯蔵しておいた水素を使って発電を行うのである。必要以上の電力が得られるときに水をポンプで汲み上げて水の位置エネルギーとして電気エネルギーを貯める揚水発電はすでに実用化されているが、それと同様に電力需要のピーク時に対応する手法のひとつとして水素は利用できる。
ほかにも太陽光発電や風力発電といった発電法のように、発電量が比較的自然条件に左右されやすいものの、十分な発電量が得られるときに水の電気分解を行って水素を貯蔵するという方法で、これらの発電量の不安定さを解消する方法が考えられている。
また、水素を電力の輸送手段として利用することも考えられている。長距離の送電を行うと送電線の抵抗などの関係で送電によるエネルギーの損失(送電ロス)が多くなる。小水力発電や火力発電や比較的低温の熱源を利用した発電法などのように、電力需要の多い都市の近くに発電所を立地できる場合は送電ロスの問題もあまりない。しかし、必要に応じて変圧を行うなど送電ロスを少なくする工夫は行われているものの、2011年時点では送電ロスなしに長距離を送電する手法は実用化されていない。このためいわゆる自然エネルギーを利用した発電法に限らず、あらゆるエネルギーを利用した発電法において電力の供給地と需要地とが離れている場合には、どうしても送電ロスの問題が避けられない。ここで水素として輸送すれば、水素を逃がさなければ輸送中の水素のロスは発生しない。ただし水素を輸送する手段によって消費されるエネルギー(たとえば自動車で輸送すれば燃料が消費される)もあるため、どうしてもエネルギーのロスは発生してしまうという問題は残る。また、水素から電気に戻す際にもエネルギーロスが発生する。ただし、このロスは、熱として利用できる。
最近ではマグネシウムと水を反応させて水素を作り出す方法も開発されている。マグネシウムと水が反応して発生する水素のほか、反応時の熱もエネルギー源として利用できる。最大の課題は使用後のマグネシウムの還元処理で、太陽光などから変換したレーザー照射による高温により還元する方法が考えられている。ほかに燃料電池の燃料としての水素の利用はよく知られているが、コンバインドサイクル発電などに利用することも考えられている。
燃料電池
燃料電池車、トヨタ・MIRAI →詳細は「燃料電池」を参照空気中の酸素と反応させて水を生成しながら発電する水素 – 酸素型燃料電池は19世紀中ごろには実験的に成功したが、生活家電などの分野へは応用されず、20世紀の宇宙開発を通じて技術検討が進んだ。燃料電池は現時点の技術においては発電効率が35 – 60 %高く、発熱エネルギーを回収することができれば80 %まで高めることができる。環境負荷も低いという利点がある。燃料にはメタノールを用いる機械もあるが、水素ガスを利用するものでは自動車への積載を念頭に置いた固体高分子形燃料電池(PEFC)が有力視されており、電解質分離膜や電極劣化の抑制など技術開発が進められている[16]。また宇宙船では燃料電池から得られる電力のほかに、同時に生成される水の利用も行われることがある。
貯蔵技術
水素をエネルギー利用する上での課題のひとつには、ガス状水素を貯蔵する際の問題がある。既述のように空気との混合4.1 – 74.2 %という広い爆発限界の範囲を持つために、漏出しないようにする技術が必要となる。水素は原子半径が小さいために容器を透過したり、劣化させたりするため、ほかの元素や燃料を貯蔵するのとは勝手が違ってくる。2002年2月に発足した「燃料電池プロジェクト・チーム」の報告では、自動車に積載しガソリン相当の 500 km以上走行が可能な水素貯蔵を目標に据えた。これに相当する水素ガスは5 kgであり、常温常圧下では61000リットルに相当する[16]。
従来の貯蔵手法では、高圧化と液体化の2つがある。水素は金属脆化を起こすため、特に高圧ガスを密閉するにはアルミニウム – マグネシウム – シリコン合金をファイバー強化したものが開発されているが、日本の高圧ガス保安法が定める上限の350気圧では実用的に自動車積載が可能なガス量は3.5 kgにとどまり、5 kgを実現するためには安全に700気圧相当を密封できる容器が検討されている。液体化も同様の問題を解決する必要があり、オーステナイト系ステンレス鋼やアルミニウム合金・チタン合金などを素材に検討が進む。しかし、高圧化や液体化には密封する際にも加圧や冷却などでエネルギーを消費してしまう点も課題として残る[16]。
水素を貯蔵する物質には金属類である水素吸蔵合金と、無機・有機物質が提案されており、いずれも水素化物を作り効率的に水素を捕まえることができる。水素吸蔵合金は、ファンデルワールス力(分子間力の一種)で表面に吸着(物理吸着)させた水素分子を原子に解離(解離吸着、化学吸着)し、水素化合物を反応生成しながら合金の格子内に水素原子を拡散させる。取り出すには加熱または合金周囲の水素ガス量を減らすことで水素化物が分解しガスが放出される。必要な温度は通常50 °Cであり、高くとも250 °C程度、圧力も常圧から100気圧程度までであり、水素ガスの体積を1000分の1に収めることができる。課題は合金と水素の重量比にあり、現状では5 kgの水素を吸蔵するための合金重量は170 – 500 kg程度が必要になる[16]。このほか、イオン結合を主とする錯体水素化物や、アンモニアボランなども水素吸蔵性能を持つ物質として研究されている[16]。
水素循環社会
→「水素エネルギー社会」も参照自然エネルギーからの電気(太陽光発電や人工光合成)によって水の電気分解から水素を生成してエネルギー媒体として貯蔵し、燃料電池を使って発電し電気を取り出すというエネルギーの循環構想がある[49]。
一見、理想的で無駄のないサイクルに思えるが、電気分解から燃料電池による発電までの工程ではニッケル水素電池やリチウムイオン充電池と比較して効率が大幅に低い。高分子固体電解質を利用した電気分解の工程では分解時に両極でガスが発生するが、これが連続した反応を阻害する一因となる。また、燃料電池での発電工程でも同様に燃料電池のガス拡散電極の特性上、電流密度を上げるためにはスタックを重ねなければならず、取り出す電流を2倍にしようとすれば電極の面積も2倍にしなければならず、単位容積ごとの効率が低い。貯蔵時にも専用の高圧タンクや水素吸蔵合金を使用しなければならないため、単位体積ごと、あるいは単位重量ごとのエネルギー密度を下げる要因になり、利点を相殺してしまっている。
生体研究
水素に関する研究について概説する。1671年にはロバート・ボイルによって水素ガスが生成され、水素はガスであると認識され、生理的に不活性なガスだと考えられ、注目されなかった[50]。初期には、水素分子の生物学的効果は小規模に研究されてきた[51]。1975年に、Doleらは水素ガスが動物の皮膚腫瘍を退縮するという研究結果を『サイエンス』にて報告したが[52][53]、注目はされなかった[53][50]。肝臓に慢性の炎症を持つマウスでの高圧水素の抗炎症作用は、2001年に報告された[51]。こうした研究は数が限られている[51]。
水素ガスを含む吸気として、たとえば飽和潜水用のガスとして水素50 %、ヘリウム49 %、酸素1 %用の混合気が用いられており、この場合、水素に起因する毒性や安全性の問題は見られていない[54]。
ボストン小児病院、ハーバード大学医学部の研究でも、水素ガスの吸入による細胞障害、組織障害のような有害事象はないことが報告されており[55]、名古屋大学医学部産婦人科、香川大学医学部産婦人科の研究においても、水素の摂取による毒性や催奇性はないことが報告されている[56][57]。
ただし、水素は爆発性を有する気体であり、爆発濃度においては静電気のような微弱なエネルギーで爆発する危険性がある。従って、水素ガス吸入療法においては、爆発限界濃度以下(10 %以下)の水素ガスを発生させる水素ガス吸入機を用いることが重要であると、市販の水素ガス吸入機の安全性について警鐘を鳴らす論文が2019年に発表されている[58][26][59]。実際に消費者庁の事故情報データバンクによれば、水素濃度が99.99%や67%の高濃度の水素を生成する水素ガス吸入機の爆発によって顔面内骨折、聴力低下、耳鳴りなどの重大事故事例が複数報告されている[60][61][62]。さらに2024年9月30日には、水素と酸素を2:1で混合した高濃度水素ガス生成する吸入機を用いて吸入を行っていたところ、パンという音と共に口から大量出血を起こし救命救急センターに搬送された。検査の結果、内臓破裂と気管支の裂傷を起こす重大事故が消費者庁の事故データバンクに報告された[63]。
2024年に、高濃度水素ガス吸入機と電磁波を照射する温熱療法機を併用して乳癌の治療を試みた際、患者の胸部内部で水素爆発が発生し、その後、喀血する事態が起きた。CT検査の結果、肺胞中心に肺挫傷が認められ、吸入性燃焼肺障害と診断されて入院に至った[64]。この事故は、高濃度水素ガスを吸入することで、肺内でも水素濃度が爆発限界に達し体内で水素爆発が起きる可能性があることを示唆するものである。したがって、家庭や医療機関における高濃度水素ガス吸入による人体内水素爆発事故を防止するためには、水素ガスの水素濃度が爆発濃度以下(10%以下)の水素ガスを生成する吸入機を使用する必要がある。
日本における水素の医療利用の研究に関する最初の報告は、2003年のヒドロキシルラジカルによる水素分子の水素引き抜き反応によって、種々の酸化ストレスに起因する疾病を予防または改善する報告に遡る[65]。さらに2005年には、ラットの酸化剤誘発モデルに対する水素水の抗酸化効果が報告された[66]。
日本医科大学での2007年の実験[67]を受けて、慶應義塾大学では2012年から心停止のラットでの治療モデルを確立してきた[68]。2015年10月には、慶應義塾大学先導研究センター内に水素ガス治療開発センターが開設された[68]。
心肺停止時の水素ガスの吸入は先進医療Bに認定され、研究が進められている[69]。従来の研究では動物を対象として心停止の際の脳・心臓の臓器障害抑制が調査されていたが、2016年9月には、初のヒトを対象とした研究が公表され、5人中4人が90日後には普通の生活に戻った[70]。これは慶應義塾大学を中心として2月に開始された臨床研究であり、心停止の影響によって寝たきりとなる、言葉がうまく話せなくなるといった後遺症が残る事が多く、これを抑制するための医療現場への導入が目標とされている[71]。
αグルコシダーゼ阻害剤である糖尿病治療薬のアカルボースを服用すると炭水化物の吸収が抑制され、大腸の腸内細菌により水素などが発生する。アカルボースの服用が心血管事故を抑制する可能性があり、この原因として高血糖の抑制に加えて、呼気中に水素ガスの増加が認められ、この増加した水素の抗酸化作用で心血管事故を抑制するメカニズムが想定されている[72]。
水素と水素が水に溶存した水素水の研究は、2007年から2015年6月までで321の水素の論文があり、臨床試験も年々増加してきた[51]。
上述のように水素は従来の医薬品とは異なり、病気の根源である酸化ストレスを抑制し広範囲の疾病に対する改善効果を有することから、病気に対する「ワイドスペクトラム分子」と呼ばれる可能性がある[73]。
2019年12月10日現在、水素の医療利用に関係する学術論文は600報を超える[74][75]。
宇宙における水素の反応
宇宙空間は、私たちが日頃暮らしを営む環境とは大きく異なるため、全く異なる現象が起こる。水素の場合も例外ではない。例えば惑星大気の上層部分では、水素に高エネルギー電子が衝突することによって、三水素イオンが生成する。
 この節の加筆が望まれています。
この節の加筆が望まれています。水素原子は非常に簡単な構造をしているため、水素の陽子または電子を別の粒子に置き換えた粒子は不特定多数存在する。なお、水素と似たような化学反応を起こす粒子もある。
- K中間子水素:電子を負電荷のK中間子に置き換えた粒子。
- 反水素:陽子を反陽子に、電子を陽電子に置き換えた粒子。
- プロトニウム:電子を反陽子に置き換えた粒子。
- ポジトロニウム:陽子を陽電子に置き換えた粒子。
- ミューオニウム:陽子を反ミュー粒子に置き換えた粒子。
- リュードベリ原子:n個の陽子を持つ核の付近にn−1個の電子があり、さらにそこから離れた軌道に1つの電子が飛び回っている粒子。
脚注
注釈
出典
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y 桜井 1997.
- ^ a b c d e f g h i j 化学工業日報 1996, pp. 233–234, 水素.
- ^ Magnetic susceptibility of the elements and inorganic compounds (PDF) (2004年3月24日時点のアーカイブ), in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ Palmer, D. (1997年9月13日). “What is the known percentage of hydrogen in the Universe and where is it?”. NASA. 2010年5月8日閲覧。
- ^ Anders & Grevesse 1989, p. 197.
- ^ クリエイティブ・スイート 2009, p. 22.
- ^ 西尾正則. “宇宙科学入門第7回資料” (PDF). 鹿児島大学理学部. 2010年5月9日閲覧。
- ^ a b 井田 2014, p. 9.
- ^ a b Asplund et al. 2009, pp. 24 & 46.
- ^ “The Element Hydrogen”. JLab. It’s Elemental. 2021年4月17日閲覧。
- ^ “「大気」概論”. 環境省. 2024年12月22日閲覧。
- ^ a b 日経サイエンス編集部 2009.
- ^ a b 化学工業日報 1996, pp. 234–235, 重水素.
- ^ a b c d e f g h i Lee 1982, pp. 119–123, 3. 元素の一般的性質: 水素.
- ^ Audia et al. 2003, p. 27.
- ^ a b c d e f g h 東北大学金属材料研究所 2009.
- ^ “〈研究例紹介〉液化水素用水素分子核スピン転換触媒の開発”. 北海道大学大学院工学研究院附属エネルギーマテリアル融合領域研究センター マルチスケール機能集積研究室. 2020年6月10日時点のオリジナルよりアーカイブ。2020年6月10日閲覧。
- ^ Weir, Mitchell & Nellis 1996.
- ^ W. J. ネリス (2000年8月). “水素の金属を作る”. 日経サイエンス. 2021年4月17日閲覧。
- ^ ビル・アーネット (1995年8月29日). “木星”. 金光研究室. ザ・ナイン・プラネッツ. 福岡教育大学. 2010年5月9日閲覧。
- ^ 長柄 2003.
- ^ a b Maccarone, Mattia; Takeshi Othoshi(訳) (2017年2月14日). “生み出された「金属水素」、さて何の役に立つのか?”. WIRED.jp. コンデナスト・ジャパン. 2021年5月12日閲覧。
- ^ Castelvecchi 2017.
- ^ 玉尾, 桜井 & 福山 2010, 付録. 112元素の周期表.
- ^ 井上 2016.
- ^ a b Kurokawa et al. 2019.
- ^ IUPAC Nomenclature of Organic Chemistry /Recommendations 1979 and Recommendations 1993 by ACD Lab. Inc.)
- ^ a b c d Lee 1982, pp. 123–126, 3. 元素の一般的性質: 水素化物.
- ^ “Hydride - PubChem Public Chemical Database”. The PubChem Project. USA: National Center for Biotechnology Information. 2016年5月19日閲覧。
- ^ METAL HYDRIDES, WATER-REACTIVE, N.O.S. (version 2.6 ed.), Alternate Chemical Names: Cameo Chemicals 2016年5月19日閲覧。
- ^ “Hydrogen anion”, NIST Standard Reference Database 69: NIST Chemistry WebBook (The National Institute of Standards and Technology (NIST)) 2016年5月19日閲覧。
- ^ “ヒドリドイオン”. LSDB. 学術用語の日本語と英語の対応. ライフサイエンス統合データベースセンター. 2019年6月13日時点のオリジナルよりアーカイブ。 Template:Cite webの呼び出しエラー:引数 accessdate は必須です。
- ^ 九州大学、科学技術振興機構、日本原子力研究開発機構 (2007年4月27日). “用語解説”. 水素活性化酵素のモデル化に成功. 注2: ヒドリドイオン: 科学技術振興機構. 2017年7月25日閲覧。
- ^ 「ヒドリドイオン」。コトバンクより2016年5月19日閲覧。
- ^ 玉尾, 桜井 & 福山 2007.
- ^ 経済産業省大臣官房調査統計グループ 2020, p. 9.
- ^ a b c d e f g h “水素の“色”について”. あいち産業科学技術総合センターニュース. (2021年9月)
- ^ a b c d FEDERAL MINISTRY FOR ECONOMIC AFFAIRS AND CLIMATE ACTION (June 2020). The National Hydrogen Strategy (Report). p. 28.
- ^ a b c d e f g 日本国際問題研究所 (May 2021). 第 6 章 欧州が進める脱炭素化の動き(水素戦略及び国境炭素税導入)と改訂された新エネルギー戦略に見るロシアの対応 (PDF) (Report). 「大国間競争時代のロシア」 (令和2年度 ロシア研究会).
- ^ “ホワイト水素とは?天然水素の可能性と脱炭素への貢献を分かりやすく解説”. 脱炭素とSDGsの知恵袋 (2025年5月4日). 2025年6月19日閲覧。
- ^ 玉尾, 桜井 & 福山 2010, pp. 86–87.
- ^ 「水素を生かす(上)初のセルフ式ステーション」『日本経済新聞』朝刊2019年1月6日(サイエンス面)2019年2月24日閲覧。
- ^ 既存添加物名簿収載品目リスト(日本食品化学研究振興財団、平成26年2月6日更新)2016年6月30日閲覧。
- ^ Agency Response Letter GRAS Notice No. 520 FDA, November 28, 2014.
- ^ ガッツリ学ぶ 電験二種 電力 2024, p. 93-95, 2-4. タービン発電機と電気設備.
- ^ 日本鍍金材料協同組合 2008.
- ^ 黒部 2008.
- ^ 「水素を発電燃料に 千代田化工など、東南アから輸入」『日本経済新聞』電子版(2017年7月27日)2018年5月11日閲覧
- ^ 古川一夫 (2015年3月2日). “水素社会構築に向け、新たな研究開発を開始”. 2015年7月11日閲覧。
- ^ a b 李 et al. 2015.
- ^ a b c d Ichihara et al. 2015.
- ^ Dole, Wilson & Fife 1975.
- ^ a b 大澤 2013.
- ^ Nicolson et al. 2016.
- ^ Cole. “Safety of inhaled hydrogen gas in healthy mice”. www.medgasres.com. 2020年2月14日閲覧。
- ^ “早産における分子状水素の予防効果と母獣長期投与の胎仔への影響”. KAKEN. 2020年2月14日閲覧。
- ^ “新生児低酸素性虚血性脳症に対する低体温と水素吸入ガス併用療法の効果に関する研究”. KAKEN. 2020年2月14日閲覧。
- ^ “世界唯一の爆発しない水素ガス吸入機の開発”. プレスリリース・ニュースリリース配信シェアNo.1|PR TIMES. 2020年2月14日閲覧。
- ^ 大学ジャーナルオンライン編集部 (2019年9月26日). “市販の水素ガス吸入機に爆発危険性 慶應義塾大学とMiZが共同研究 | 大学ジャーナルオンライン”. 大学ジャーナル. 2020年2月14日閲覧。
- ^ “事故情報データバンクシステム”. www.jikojoho.caa.go.jp. 2024年7月16日閲覧。
- ^ Ichikawa, Yusuke; Hirano, Shin-ichi; Sato, Bunpei; Yamamoto, Haru; Takefuji, Yoshiyasu; Satoh, Fumitake (2022-05-12). “Guidelines for the selection of hydrogen gas inhalers based on hydrogen explosion accidents”. Medical Gas Research 13 (2): 43–48. doi:10.4103/2045-9912.344972. ISSN 2045-9912. PMC 9555030. PMID 36204781.
- ^ “安全な水素ガス吸入機選択の世界基準 爆水素爆発事故に基づく安全な水素ガス吸入機の選択のガイドライン”. 2024年7月12日閲覧。 エラー: 閲覧日が正しく記入されていません。(説明)
- ^ “消費者庁 事故データバンク”. 2025年1月25日閲覧。
- ^ “A case of lung injury due to a hydrogen explosion caused by the simultaneous use of two home folk remedies devices”. 2025年1月21日閲覧。
- ^ “MiZ株式会社 水素を含有する薬理機能水およびその用途に関する特許公報 (特許第4783466号)”. J-PlatPat. 2020年2月14日閲覧。
- ^ Yanagihara et al. 2005.
- ^ Ohsawa et al. 2007.
- ^ a b 佐野 2016.
- ^ 先進医療 B 実施計画等評価表(番号 B066)2016年7月14日
- ^ Tamura et al. 2016.
- ^ “心停止の患者 水素で脳ダメージ軽減 臨床研究開始へ”. NHK科学文化部ブログ (2016年2月20日). 2017年4月1日閲覧。
- ^ 入江 & 伊藤 2012.
- ^ Hirano et al. 2020b.
- ^ “「水素分子の各種疾患又は疾患モデルに対する 効果を報告した文献一覧」MiZ株式会社”. 2020年2月18日閲覧。
- ^ Hirano et al. 2020a.
参考文献
- 書籍
-
- Lee, J. D. 著、浜口博、菅野等 訳「3. 元素の一般的性質 水素」『無機化学』東京化学同人、1982年4月、119-123頁。 ISBN 4-8079-0185-0。
- 桜井, 弘「水素」『元素111の新知識 — 引いて重宝、読んでおもしろい』講談社〈ブルーバックス〉、1997年10月、30-34頁。 ISBN 4-06-257192-7。
- 『完全図解周期表 — 自然界のしくみを理解する第1歩』玉尾皓平、桜井弘、福山秀敏(監修)、ニュートンプレス〈Newton別冊: サイエンステキストシリーズ〉、2007年1月。 ISBN 978-4315517897。
- 『12996の化学商品』化学工業日報、1996年1月。 ISBN 4-87326-204-6。
- 東北大学金属材料研究所「8. 燃料電池と水素貯蔵材料」『金属材料の最前線 — 近未来を拓くキー・テクノロジー』講談社〈ブルーバックス〉、2009年7月、241-259頁。 ISBN 978-4-06-257643-7。
- 日経サイエンス編集部 編「惑星の顔を決める大気流出」『見えてきた太陽系の起源と進化』日経サイエンス〈別冊 日経サイエンス〉、2009年10月、134-142頁。 ISBN 978-4-532-51167-8。
- 『完全図解周期表 — ありとあらゆる「物質」の基礎がわかる』玉尾皓平、桜井弘、福山秀敏(監修)(第2版)、ニュートンプレス〈ニュートン別冊: サイエンステキストシリーズ〉、2010年4月。 ISBN 978-4-315-51876-4。
- クリエイティブ・スイート『ビジュアルでよくわかる 宇宙の秘密 — 宇宙誕生の謎から地球外生命の真相まで』PHP研究所〈PHP文庫〉、2009年11月。 ISBN 978-4-569-67352-3。
- 井田, 喜明『地球の教科書』岩波書店、2014年11月27日。 ISBN 978-4-00-006251-0。
- 論文
-
- Ashcroft, N. W. (1968-12-23). “Metallic Hydrogen: A High-Temperature Superconductor?” (英語). Phys. Rev. Lett. (American Physical Society) 21 (26): 1748-1749. Bibcode: 1968PhRvL..21.1748A. doi:10.1103/PhysRevLett.21.1748. ISSN 0031-9007.
- Dole, M.; Wilson, F. R.; Fife, W. P. (1975-10-10). “Hyperbaric hydrogen therapy: a possible treatment for cancer” (英語). Science (AAAS) 190 (4250): 152-154. doi:10.1126/science.1166304. PMID 1166304.
- Anders, Edward; Grevesse, Nicolas (1989-01). “Abundances of the Elements-Meteoritic and Solar” (英語). Geochimica et Cosmochimica Acta (Elsevier) 53 (1): 197-214. doi:10.1016/0016-7037(89)90286-X.
- Weir, S. T.; Mitchell, A. C.; Nellis, W. J. (1996-03-11). “Metallization of Fluid Molecular Hydrogen at 140 GPa (1.4 Mbar)” (英語). Phys. Rev. Lett. (American Physical Society) 76 (11): 1860-1863. doi:10.1103/PhysRevLett.76.1860.
- 長柄, 一誠「高圧固体水素の第一原理計算」『高圧力の科学と技術』第13巻第3号、日本高圧力学会、2003年11月5日、204-211頁、doi:10.4131/jshpreview.13.204。
- Audia, G.; Bersillonb, O.; Blachotb, J.; Wapstrac, A.H. (2003-12). “The Nubase evaluation of nuclear and decay properties” (英語). Nuclear Physics A 729 (1): publisher=Elsevier. doi:10.1016/j.nuclphysa.2003.11.001.
- Yanagihara, Tomoyuki; Arai, Kazuyoshi; Miyamae, Kazuhiro; Sato, Bunpei; Shudo, Tatsuya; Yamada, Masaharu; Aoyama, Masahide (2005-01-01). “Electrolyzed Hydrogen-Saturated Water for Drinking Use Elicits an Antioxidative Effect: A Feeding Test with Rats” (英語). Bioscience, Biotechnology, and Biochemistry (Japan Society for Bioscience, Biotechnology and Agrochemistry) 69 (10): 1985–1987. doi:10.1271/bbb.69.1985. ISSN 0916-8451.
- Ohsawa, Ikuroh; Ishikawa, Masahiro; Takahashi, Kumiko; Watanabe, Megumi; Nishimaki, Kiyomi; Yamagata, Kumi; Katsura, Ken-ichiro; Katayama, Yasuo et al. (2007-05-07). “Hydrogen acts as a therapeutic antioxidant by selectively reducing cytotoxic oxygen radicals” (英語). Nature Medicine (Nature Publishing) 13: 688–694. doi:10.1038/nm1577. PMID 17486089.
- 黒部, 洋「機能水の製造方法および洗浄効果」『Material Stage』第7巻第10号、技術情報協会、2008年1月10日、40-43頁、 NAID 40015808393。
- Asplund, Martin; Grevesse, Nicolas; Sauval, A. Jacques; Scott, Pat (2009-09-04). “The chemical composition of the Sun” (英語). Annual Review of Astronomy and Astrophysics (Annual Reviews). doi:10.1146/annurev.astro.46.060407.145222. arXiv:0909.0948.
- 入江, 潤一郎、伊藤, 裕「腸管環境と心血管病」『心臓』第44巻第12号、日本心臓財団、2012年12月15日、1498-1503頁、doi:10.11281/shinzo.44.1498。
- 大澤, 郁朗「水素分子の疾患予防・治療効果」『日本透析医会雑誌』第28巻第2号、日本透析医会、2013年8月30日、261-267頁、 ISSN 0914-7136。
- 李, 強、田中, 良晴、田中, 博司、三羽, 信比古「水素医学研究概況及び関連文献のビブリオメトリックス解析」『大阪物療大学紀要』第3巻、大阪物療大学、2015年3月8日、31-40頁、doi:10.24588/bcokiyo.3.0_31。
- Ichihara, Masatoshi; Sobue, Sayaka; Ito, Mikako; Ito, Masafumi; Hirayama, Masaaki; Ohno, Kinji (2015-10-19). “Beneficial biological effects and the underlying mechanisms of molecular hydrogen – comprehensive review of 321 original articles” (英語). Medical Gas Research (BioMed Central) 5. doi:10.1186/s13618-015-0035-1. PMC 4610055. PMID 26483953.
- Nicolson, Garth L.; de Mattos, Gonzalo Ferreira; Settineri, Robert; Costa, Carlos; Ellithorpe, Rita; Rosenblatt, Steven; La Valle, James; Jimenez, Antonio et al. (2016-01-22). “Clinical Effects of Hydrogen Administration: From Animal and Human Diseases to Exercise Medicine” (英語). International Journal of Clinical Medicine (Scientific Research) 7 (1): 32–76. doi:10.4236/ijcm.2016.71005.
- 井上, 雅弘「水素の安全利用」『電気設備学会誌』第36巻第4号、電気設備学会、2016年4月10日、263-266頁、doi:10.14936/ieiej.36.263。
- Tamura, Tomoyoshi; Hayashida, Kei; Sano, Motoaki; Suzuki, Masaru; Shibusawa, Takayuki; Yoshizawa, Joe; Kobayashi, Yosuke; Suzuki, Takeshi et al. (2016-07-25). “Feasibility and Safety of Hydrogen Gas Inhalation for Post-Cardiac Arrest Syndrome – First-in-Human Pilot Study” (英語). Circulation Journal (The Japanese Circulation Society) 80 (8): 1870–1873. doi:10.1253/circj.CJ-16-0127. PMID 27334126.
- 佐野, 元昭「水素ガス吸入療法による心肺停止蘇生後臓器障害抑制」『Organ Biology』第23巻第2号、日本臓器保存生物医学会、2016年8月31日、117-120頁、doi:10.11378/organbio.23.117。
- Castelvecchi, Davide (2017-01-26). “Physicists doubt bold report of metallic hydrogen”. Nature (Nature Research) 17 (7639). doi:10.1038/nature.2017.21379.
- Dias, Ranga P.; Silvera, Isaac F. (2017-02-17). “Observation of the Wigner-Huntington transition to metallic hydrogen”. Science (AAAS) 355 (6326): 715-718. doi:10.1126/science.aal1579.
- Kurokawa, Ryosuke; Hirano, Shin-ichi; Ichikawa, Yusuke; Matsuo, Goh; Takefuji, Yoshiyasu (2019-09-23). “Preventing explosions of hydrogen gas inhalers” (英語). Medical Gas Reserach (BioMed Central) 9 (3): 160-162. doi:10.4103/2045-9912.266996.
- Hirano, Shin-ichi; Ichikawa, Yusuke; Kurokawa, Ryosuke; Takefuji, Yoshiyasu; Satoh, Fumitake (2020-03-13). “A ‘philosophical molecule,’ hydrogen may overcome senescence and intractable diseasess” (英語). Medical Gas Reserach (BioMed Central) 10 (1): 47-49. doi:10.4103/2045-9912.279983.
- Hirano, Shin-ichi; Ichikawa, Yusuke; Sato, Bunpei; Satoh, Fumitake; Takefuji, Yoshiyasu (2020-12-16). “Hydrogen Is Promising for Medical Applications” (英語). Clean Technologies (MDPI) 2 (4): 529–541. doi:10.3390/cleantechnol2040033.
- 雑誌
-
- 「水の活性化と機能水 — 表面処理における各種対策について」『鍍金の世界』第41巻第4号、日本鍍金材料協同組合、2008年4月、52-56頁、 NAID 40016050513。
- 行政資料
-
- 経済産業省大臣官房調査統計グループ 編『経済産業省生産動態統計年報 化学工業統計編』 2019年、経済産業調査会、2020年5月22日。 NCID AA12689558。
関連項目
- 文学
-
- 水素製造法(小説)
外部リンク
- Hydrogen - Encyclopedia of Earth「水素」の項目。
- 国際化学物質安全性カード 水素 (ICSC:0001) 日本語版(国立医薬品食品衛生研究所による), 英語版
- 『水素』 - コトバンク
水素
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2017/09/15 15:56 UTC 版)
炭化水素燃料に代わる次世代の燃料として水素が候補として挙げられるが、水素は自然界には産出しないため、水素細菌、天然ガスの改質、水の電気分解や高温ガス原子炉などで製造しなければならない。さらに、貯蔵には液体水素タンク、水素吸蔵合金、高圧タンクのいずれかを要する。それに対してメタノールであれば、常温、常圧で貯蔵が可能で貯蔵施設も含めた単位体積毎のエネルギー量は水素を凌駕する。
※この「水素」の解説は、「メタノール経済社会」の解説の一部です。
「水素」を含む「メタノール経済社会」の記事については、「メタノール経済社会」の概要を参照ください。
水素
出典:『Wiktionary』 (2021/11/06 13:26 UTC 版)
名詞
- 原子番号 1, 原子記号 Hの非金属元素の一つ。原子量が最も小さく、宇宙で最も豊富に存在する原子であり、水や有機化合物、生物内部にも多数存在する。単体は常温常圧では無色無臭の気体
- 2つの水素原子で構成される分子。化学式はH2。常温常圧では無色無臭の気体で、非常に燃えやすいなどの特徴がある。
発音(?)
- す↘いそ
語源
- オランダ語 waterstof ← water(水)+ stof(物質)。宇田川榕菴が『遠西医方名物考補遺』、1834、水素で翻訳。元は、ラヴォアジエの命名したhydrogène(Fr.)(<ギリシア語ὕδωρ(hydôr:水)+ γεννάν(gennan:発生))より 。
関連語
翻訳
- アイスランド語: vetni (is) 中性
- アイルランド語: hidrigin (ga)
- アストゥリアス語: hidróxenu (ast) 男性
- アゼルバイジャン語: hidrogen (az)
- アブハズ語: аӡри (ab)
- アフリカーンス語: waterstof (af)
- アムハラ語: ሃይድሮጅን (am)
- アラゴン語: hidrochén (an) 男性
- アラビア語: هِيدْرُوجِين (ar) (hidrožēn) 男性, هَيْدْرُوجِين (ar) (haydrojīn) 男性
- アルバニア語: hidrogjen (sq)
- アルメニア語: ջրածին (hy)
- イタリア語: idrogeno (it) 男性
- イディッシュ語: הידראָגען (yi), וואַסערשטאָף (yi)
- イド語: hidrogeno (io)
- イヌクティトゥット語: ᐳᓪᓚᕐᓂᐅᕿᓐᓂᖅᐹᖅ (iu)
- インターリングア: hydrogeno (ia)
- インドネシア語: hidrogen (id), zat air (id)
- ウイグル語: ھىدروگېن (ug)
- ウェールズ語: hydrogen (cy), ulai (cy)
- ヴェプス語: vezinik (vep)
- ヴォラピュク: hidrin (vo)
- ヴォロ語: vesinik (vro)
- ウクライナ語: во́день (uk)
- ウズベク語: vodorod (uz)
- ウルドゥー語: ہائیڈروجن (ur) (hāiḍrojan) 女性
- 英語: hydrogen (en)
- エストニア語: vesinik (et)
- エスペラント: hidrogeno (eo)
- エルジャ語: ведь чачтый (myv)
- オセット語: донгуыр (os)
- オック語: idrogèn (oc) 男性
- オランダ語: waterstof (nl) 中性
- オリヤー語: ଉଦ୍ଜାନ (or) (udjān)
- カザフ語: сутегі (kk), сутек (kk)
- カシューブ語: wòdzyk m
- カタルーニャ語: hidrogen (ca) 男性
- ガリシア語: hidróxeno (gl) 男性
- カルムイク語: үстөр (xal)
- カンナダ語: ಜಲಜನಕ (kn)
- 北フリジア語: wååderstuf (frr)
- ギリシア語: υδρογόνο (el) 中性
- ギリシア語ポントス方言: υδρογόνον (pnt)
- キルギス語: суутек (ky)
- グアラニ語: tatavevýi (gn)
- グジャラート語: ઉદજન (gu)
- クメール語: អ៊ីដ្រូសែន (km) (idrusaen)
- グリーンランド語: brinti (kl)
- グルジア語: წყალბადი (ka)
- クルド語: hîdrojen (ku)
- ケチュア語: yakuchaq (qu), idruhinu (qu)
- コーンウォール語: hidrojen (kw) 男性
- コサ語: umngxengamoya (xh)
- コミ・ジリエーン語: вачужысь (kpv)
- コミ・ペルミャク語: ваувтыр (koi)
- コルシカ語: idrogenu (co) 男性
- ザーターフリジア語: Woaterstof (stq)
- サモギティア語: ondėnilis (sgs)
- サンスクリット: उदजन (sa)
- シチリア語: idrògginu (scn) 男性
- ジャワ語: hidrogen (jv)
- シンド語: उदजन (sd) (udjan)
- シンハラ語: ජලකර (si)
- スウェーデン語: väte (sv) 中性
- スコットランド・ゲール語: haidreagain (gd)
- スペイン語: hidrógeno (es) 男性
- スラナン語: watraskotriki (srn)
- スロヴァキア語: vodík (sk) 男性
- スロヴェニア語: vodik (sl) 男性
- スワヒリ語: hidrojeni (sw)
- スンダ語: hidrogén (su)
- セブアノ語: idroheno (ceb), hidroheno (ceb)
- セルビア・クロアチア語:
- ソト語: sehlolametsi (st)
- ソルブ語:
- タイ語: ไฮโดรเจน (th)
- タガログ語: idroheno (tl)
- タジク語: гидроген (tg), ҳидроген (tg)
- タミル語: நீரகம் (ta), ஹைட்ரஜன் (ta)
- チェコ語: vodík (cs) 男性
- チェロキー語: ᏭᏓᏌᎧᎯᏴ ᎤᏃᎴ (chr)
- チベット語: ཡང་རླུང་། (bo)
- チュヴァシュ語: водород (cv)
- 中国語:
- 朝鮮語: 수소 (ko) (水素 (ko))
- 低地ドイツ語:
- オランダ低ザクセン語: waeterstof (nds-nl)
- テルグ語: ఉదజని (te), హైడ్రోజన్ (te)
- デンマーク語: brint (da), hydrogen (da)
- ドイツ語: Wasserstoff (de) 男性, Hydrogen (de) 中性, Hydrogenium (de) 中性
- ドーグリー語: उदजन (doi) (udjan)
- トルクメン語: wodorod (tk)
- トルコ語: hidrojen (tr), müvellidülmâ (tr)
- トンガ語: ʻeavai (to)
- ナヴァホ語: háájiʼjin (nv)
- ナワトル語: āyōcoxqui (nah)
- 西フリジア語: wetterstof (fy) 中性
- ネパール語: उदजन (ne)
- ノヴィアル: hidrogene (nov)
- ノルウェー語:
- バイエルン語: Wassastoff (bar) 男性
- ハイチ語: idwojèn (ht)
- パシュトー語: هايډروجن (ps) (hayḍroǰán) 男性
- バスク語: hidrogeno (eu)
- パピアメント語: hidrogeno (pap)
- ハワイ語: haikokene (haw)
- ハンガリー語: hidrogén (hu), köneny (hu), gyulany (hu)
- パンジャブ語: ਉਦਜਨ (pa)
- ルシン語: гідроґе́н (rue) 男性, во́день (rue) 男性
- ピトケアン・ノーフォーク語: hiidrojen (pih)
- ビルマ語: ဟိုက်ဒရိုဂျင် (my)
- ヒンディー語: उदजन (hi) 女性, हाइड्रोजन (hi) 女性
- フィンランド語: vety (fi)
- フェロー語: vetni (fo) 中性, loftevni (fo) 中性, vatnevni (fo) 中性, brint (fo) 中性, hydrogen (fo) 中性
- フラマン語: woaterstof (vls)
- フランス語: hydrogène (fr) 男性
- フリウリ語: idrogjen (fur) 男性
- ブリヤート語: уһантүрэгшэ (bua)
- ブルガリア語: водоро́д (bg) 男性
- ブルトン語: hidrogen (br) 男性
- ベトナム語: hiđrô (vi), hyđrô (vi), hi-đrô (vi), hy-đrô (vi), khinh khí (vi) (obsolete; usually refers to the gas), hiđrô (vi)
- ヘブライ語: מֵימָן (he) (meiman) 男性
- ベラルーシ語: вадаро́д (be) 男性
- ペルシア語: هیدروژن (fa) (hidrožen)
- ベンガル語: উদজান (bn)
- ボージュプリー語: उदजन (bho) (udjan)
- ポーランド語: wodór (pl) 男性
- ポルトガル語: hidrogénio (pt) 男性 (ポルトガル), hidrogênio (pt) 男性 (ブラジル)
- マオリ語: hauwai (mi)
- マケドニア語: водород (mk) 男性
- マラーティー語: उदजन (mr)
- マラヤーラム語: ഹൈഡ്രജന് (ml), ജലവായു (ml)
- マルタ語: idroġenu (mt) 男性
- マレー語: hidrogen (ms), zat air (ms)
- マン島語: hiddragien (gv)
- メグレル語: წყარბადიშ (xmf)
- モクシャ語: ведьшачфты (mdf)
- モンゴル語: устөрөгч (mn)
- ラーオ語: ອິດໂລເຊນ (lo), ອິດໂຣເຊນ (lo)
- ラテン語: hydrogenium (la) 中性
- ラトヴィア語: ūdeņradis (lv) 男性
- ラトガリア語: iudineklis (ltg)
- リトアニア語: vandenilis (lt)
- リンガラ語: idrojɛ́ní (ln)
- リンブルフ語: waterstof (li)
- ルーマニア語: hidrogen (ro) 中性
- ルクセンブルク語: Waasserstoff (lb)
- ロシア語: водоро́д (ru) 男性
- ロンバルド語: idrògen (lmo) 男性
- ワロン語: idrodjinne (wa)
- テンプレート:gbm: उदजन (gbm)
- テンプレート:jml: उदजन (jml) (udjan)
- テンプレート:kfr: ઉદજન (kfr) (udjan)
- テンプレート:kfy: उदजन (kfy) (udjan)
「水素」の例文・使い方・用例・文例
- 水素原子
- 水は酸素と水素に分解される
- 水素と酸素が化合すると水になる
- 水は水素と酸素の化合物です
- 水は酸素と水素の化合物です
- 彼が水素ガスの可視化技術の開発に成功しました
- デヒドロゲナーゼはある種の物質から水素を奪う。
- 水素を加えて原料油から不純物を除去する。
- 水素駆動の自動車が開発されている。
- 酸素と水素で水は構成される。
- 炭酸水素ナトリウムは酸溶液を中和するだ。
- 水は酸素と水素から成る。
- 過酸化水素の化学式はH2O2です。
- 水素脆性を除去するためベーキング処理すること。
- 水素脆性を除去するためベーキング処理を行うこと。
- 水分子は、2個の水素原子と1個の酸素原子からなる。
- 水素はそれ自体としては自然界に存在しない。
- 水素の原子番号は1である。
- 水素と酸素が結合して水になる。
- 水は水素と酸素を含む。
水素と同じ種類の言葉
- >> 「水素」を含む用語の索引
- 水素のページへのリンク