芳香族化合物
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2023/10/22 01:29 UTC 版)
分類
ベンゼン環を有する化合物は芳香族化合物の代表であるが、ベンゼン環を有することだけが芳香族である条件ではない。環の大きさ、縮合状態、複素元素や電荷の存在などベンゼンとは異なる構造を有する芳香族化合物が多数存在する。以下に芳香族化合物の分類と例を示す。
- ベンゼン系芳香族化合物 (benzenoid aromatic compound)
- 縮合環芳香族化合物 (condensed ring aromatic compound)
- ベンゾ縮合環化合物
- 縮合環芳香族化合物 (condensed ring aromatic compound)
- 複素芳香族化合物 (heteroaromatic compound)
- 非ベンゼン系芳香族化合物 (non-benzenoid aromatic compound)
- アヌレン
- アズレン
- シクロペンタジエニルアニオン
- シクロヘプタトリエニルカチオン(トロピリウムイオン)
- トロポン
- メタロセン
- アセプレイアジレン
芳香族性
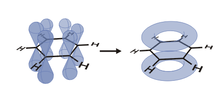
芳香族性は、π電子を持つ原子が環状に並んだ構造を持つ不飽和環状化合物に現れる。その中でも、電子基底状態で芳香族性を示す化合物は環上のπ電子系に含まれる電子の数が 4n + 2 (n = 0, 1, 2, 3, ...) 個であるもののみである。このような4n + 2個のπ電子を有する共役不飽和環構造を芳香環と呼び、またこの電子数の法則をヒュッケル則という。芳香環上のπ電子は非局在化し、環上にわたって分布している。また、共役の効率を高めるため環は平面構造をとる。このとき、π電子系とは二重結合由来のπ電子だけに限定されず、6員環である必要もなく、5員環の芳香族化合物も数多く知られている。例えばシクロペンタジエニルアニオンはアニオンの電子がπ電子系に関与し、あるいはチオフェンでは硫黄の孤立電子対がπ電子系に関与して芳香族性を現わす。このためチオフェンの硫黄原子を酸化し SO とすると硫黄の孤立電子対は酸素との結合に用いられるため芳香族性を失い、ジエンとしての反応性を示すようになる。
非局在電子に由来する磁気の遮蔽効果(核磁気共鳴などを参照)はあたかも環状の電流が存在するように作用するため環電流と呼ぶことがあるが、実際に電子が周回しているわけではない。前述の非局在化という言葉の示す通り、π電子は特定の場所にすら存在しておらず、全体として雲のように拡がっている(量子力学を参照)。ただ、実際に有機化学反応を考える場合、複数の共鳴寄与構造の間でπ電子が往来している、と考えた方が理解が容易になり、また、それで十分な場合も少なくない。
芳香族性は厳密な定義が存在しない概念であるが、上記の通り、構造的な特徴(結合長の同一化)、磁気的な特徴(環電流の発生)、エネルギー的な特徴(芳香族安定化)の3要素が芳香族性分子の条件とされている[1]。
芳香族固有の反応
芳香環は、他の不飽和環構造に比べ安定であると同時に反応性も異なる。
たとえば、ベンゼンに対して臭素 (Br2) は置換反応を起こし[注釈 1]、アルケンなどの非芳香族不飽和化合物のように付加反応は起こらない。
求核置換反応についても、反応点への背面攻撃が困難であったり、sp2炭素のカチオンが不安定であったりするため、SN1 や SN2 機構は難しい。
注釈
- ^ 通常は臭化鉄などの適切な触媒が必要。
出典
- ^ Slayden, Suzanne W.; Liebman, Joel F. (2001-05). “The Energetics of Aromatic Hydrocarbons: An Experimental Thermochemical Perspective”. Chemical Reviews (American Chemical Society) 101 (5): 1541-1566. doi:10.1021/cr990324+. ISSN 0009-2665.
芳香族化合物と同じ種類の言葉
- 芳香族化合物のページへのリンク