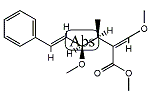
オウデマンシンA
オウデマンシンA
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2025/04/13 09:52 UTC 版)
| オウデマンシンA | |
|---|---|
 |
|
|
Methyl (2E,3S,4R,5E)-4-methoxy-2-(methoxymethylidene)-3-methyl-6-phenylhex-5-enoate
|
|
|
別称
(−)-Oudemansin A
|
|
| 識別情報 | |
| CAS登録番号 | 73341-71-6 |
| PubChem | 6438712 |
| ChemSpider | 4943167 |
| UNII | AF4T7P745Y  |
|
|
|
|
| 特性 | |
| 化学式 | C17H22O4 |
| モル質量 | 290.35 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
オウデマンシンA(英:Oudemansin A)は、担子菌門のOudemansiella mucidaから初めて分離された天然物である。その化学構造は1979年にX線結晶構造解析により、絶対立体化学は全合成により決定された。オウデマンシンBとXという2つの近縁の誘導体も他の担子菌から分離されている。これらはすべて、多くの糸状菌や酵母に対して生理活性を示すが、有用な製品にするには効力や安定性が不十分である。しかし、この発見はストロビルリン系とともに、同じ作用機序を持つアゾキシストロビンなどの農業用殺菌剤につながった[1]。
分離と特性


R1 = R2 = HのオウデマンシンA(当初は単にオウデマンシンとして知られていた)は、担子菌門のOudemansiella mucidaの菌糸体発酵物から分離された後、1979年に初めて記載された。メトキシ基と隣接するメチル基の相対配置を含むその構造は、分光学的方法と単結晶X線分析の両方によって確立されたが、絶対立体化学は当時不明であった[2]。その後、担子菌門のMycena polygrammaとXerula melanotrichaの培養物から発見された。後者の菌は、R1 = MeO、R2 = ClのオウデマンシンBも生産する。R1 = H、R2 = MeOのオウデマンシンXはOudemansiella radicataから分離された[3]。
化学合成
オウデマンシンは全合成のターゲットであり、1983年に(-)-オウデマンシンAの合成により、3つの化合物すべてが(9S,10S)-configurationを持つことが確定した[4]。オウデマンシンBとXへの経路も報告されている[1]。
殺菌剤としての作用機序
殺菌効果は、当時としては新しい作用機序であるQoI阻害に由来することが示された[5]。これはβ-メトキシアクリル酸の部分構造に関連しており、この部分構造と関連天然物であるストロビルリン系は共通している。いくつかの農薬会社による集中的な研究により、同じ作用機序に基づく有用な農業用殺菌剤が開発されたが、アゾキシストロビンはその典型例である[1]。
脚注
- ^ a b c Clough, J. M. (1993). “The strobilurins, oudemansins, and myxothiazols, fungicidal derivatives of β-methoxyacrylic acid”. Natural Product Reports 10 (6): 565–574. doi:10.1039/NP9931000565. PMID 8121648.
- ^ Anke, Timm; Hecht, Hans Jürgen; Chramm, Georgs; Steglich, Wolfgang (1979). “Antibiotics from basidiomycetes. IX. Oudemansin, an antifungal antibiotic from Oudemansiella mucida (Schrader ex Fr.) hoehnel (Agaricales)”. The Journal of Antibiotics 32 (11): 1112–1117. doi:10.7164/antibiotics.32.1112. PMID 528381.
- ^ Lorenzen, K.; Anke, T. (1998). “Basidiomycetes as a Source for New Bioactive Natural Products”. Current Organic Chemistry (Bentham Science Publishers) 2 (4): 329–364. doi:10.2174/1385272802666220128213627. ISSN 1385-2728.
- ^ Akita, Hiroyuki; Koshiji, Hiroko; Furuichi, Akiya; Horikoshi, Koki; Oishi, Takeshi (1983). “The absolute configuration of oudemansin total synthesis of (−)-oudemansin”. Tetrahedron Letters 24 (19): 2009–2010. doi:10.1016/S0040-4039(00)81829-8.
- ^ Becker, W.F.; von Jagow, G.; Anke, T.; Steglich, W. (1981). “Oudemansin, strobilurin A, strobilurin B and myxothiazol: New inhibitors of the bc 1 segment of the respiratory chain with an E-β-methoxyacrylate system as common structural element”. FEBS Letters 132 (2): 329–333. doi:10.1016/0014-5793(81)81190-8. PMID 6271595.
参考文献
- Anke, Timm; Steglich, Wolfgang (1999). “Strobilurins and Oudemansins”. Drug Discovery from Nature. Springer. pp. 320–334. ISBN 3540648445
- Morton, V.; Staub, T. (2008). “A Short History of Fungicides”. Apsnet Feature Articles. doi:10.1094/APSnetFeature-2008-0308.
- Reddy, P.Parvatha (2013). “Chapter 12: Strobilurin fungicides”. Recent advances in crop protection. Springer. pp. 185–200. doi:10.1007/978-81-322-0723-8. ISBN 978-81-322-0722-1
- オウデマンシンAのページへのリンク