ハロゲン化アルカリ金属
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/11/04 18:05 UTC 版)
構造
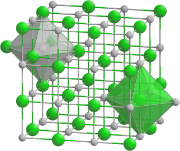
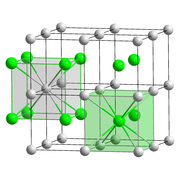
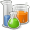
大部分のハロゲン化アルカリ金属は、面心立方格子状に結晶化する。この構造では、金属もハロゲンも八面体の配置となり、各々のイオンの配位数は6となる。塩化セシウム、臭化セシウム、ヨウ化セシウムは体心立方格子状に結晶化し、より大きな金属カチオン(アニオンも同様)に関して、配位数は8となる[2]。
性質
ハロゲン化アルカリ金属は、無色の結晶質固体であるが、細かいものは白色を呈する。高温で溶融し、通常数百℃で無色の液体になる。その高い融点は、格子エネルギーの高さを反映している。静かで高い温度では、これらの液体は二原子分子の気体を作る。
これらの化合物は極性溶媒に溶解し、溶媒和しやすいアニオン及びカチオンを含むイオン溶液となる。アルカリ金属は、対応するアルカリ金属をかなりの量、溶かす。セシウムは融点以上の全ての温度で、完全に混和性である[3]。
下の表は、各々の化合物の記事へのリンクを与えている。化合物名の横の数字は、ポーリングのスケールに基づく元素間の電気陰性度の差を示している。数字が大きいほど、固体がよりイオン性であることを表す。
| アルカリ金属 | |||||||
|---|---|---|---|---|---|---|---|
| リチウム | ナトリウム | カリウム | ルビジウム | セシウム | |||
| ハロゲン | フッ素 | LiF (3.0) | NaF (3.1) | KF (3.2) | RbF (3.2) | CsF (3.3) | |
| 塩素 | LiCl (2.0) | NaCl (2.1) | KCl (2.2) | RbCl (2.2) | CsCl (2.3) | ||
| 臭素 | LiBr (1.8) | NaBr (1.9) | KBr (2.0) | RbBr (2.0) | CsBr (2.1) | ||
| ヨウ素 | LiI (1.5) | NaI (1.6) | KI (1.7) | RbI (1.7) | CsI (1.8) | ||
出典
外部リンク
- ^ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ^ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ Huheey, James E.; Keiter, Ellen A.; Kieter, Richard L. (1993). Inorganic chemistry : principles of structure and reactivity (4. ed.). Cambridge, Mass. [u.a.]: Harper. pp. 377. ISBN 006042995X
- 1 ハロゲン化アルカリ金属とは
- 2 ハロゲン化アルカリ金属の概要
- ハロゲン化アルカリ金属のページへのリンク