トリクロロシラン
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/02/16 17:51 UTC 版)
| トリクロロシラン | |
|---|---|
| |

|

|
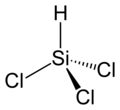
トリクロロシラン | |
| 識別情報 | |
| CAS登録番号 | 10025-78-2 
|
| EC番号 | 233-042-5 |
| 国連/北米番号 | 1295 |
| RTECS番号 | VV5950000 |
| |
| 特性 | |
| 化学式 | HCl3Si |
| モル質量 | 135.45 g/mol |
| 外観 | 無色液体 |
| 密度 | 1.342 kg/m3 |
| 融点 |
-126.6 ℃ |
| 沸点 |
31.8 ℃ |
| 水への溶解度 | 水と反応 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0591 |
| NFPA 704 | |
| Rフレーズ | R12, R14, R17, R20/22, R29, R35 |
| Sフレーズ | (S2), S7/9, S16, S26, S36/37/39, S43, S45 |
| 引火点 | -27 ℃ |
| 発火点 | 185 ℃ |
| 爆発限界 | 1.2–90.5% |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
トリクロロシラン(英: trichlorosilane)は、ケイ素、塩素、水素から成る無機化合物で、分子式は HSiCl3 と表される。高温で熱分解を起こして単体ケイ素に変わる性質から、半導体工業において高純度ケイ素の主原料として利用される[1]。水と触れると速やかに分解してシリコーンのポリマーおよび塩化水素となる[1]。反応性が高く入手が容易であることから、有機ケイ素化合物の原料ともされる[1]。
製造
工業的には、トリクロロシランは塩化水素のガスを 300 ℃ でケイ素の粉末に吹き付けて製造する[1]。下式のように、トリクロロシランとともに水素が生じる[1]。
適切に設計された反応装置では、80-90% の収率でトリクロロシランが得られる。主な副生物は四塩化ケイ素 (SiCl4)、六塩化二ケイ素 (Si2Cl6)、ジクロロシラン (H2SiCl2) であり、トリクロロシランは蒸留により取り出される。この逆反応により高純度の単体ケイ素が得られる。
用途
上記のように、トリクロロシランは高純度の多結晶ケイ素の原料とされる[1]。
出典
- “An Introductory Guide to the Safe Handling of Chlorosilanes” (PDF). Dow Corning. 2017年7月22日閲覧。
- Semiconductors: Silicon: Substrate Manufacture: Polycrystalline Silicon Production(2010年5月29日時点のアーカイブ)
- トリクロロシランのページへのリンク

