イオン半径
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2017/05/16 07:34 UTC 版)
イオン半径はオングストローム(Å)あるいはピコメートル(pm)という単位で表示されるが、後者がSI単位である。
概要
イオンの電子雲が球対称であると見做せる場合、イオン結晶中の陽イオンおよび陰イオンの原子間距離は、両者の半径の和であると仮定することができる。 X線回折により得られる原子間距離は陽イオンと陰イオンの半径の合計であり、単独イオンの半径を直接求めることはできない。そこで、1927年にライナス・ポーリング(Linus Carl Pauling)は1価イオンについて半径が有効核電荷に反比例するものと仮定して半径を求め、これを基に結晶構造のデータがあるものについて各種原子のイオン半径を決定した。
例えばフッ化ナトリウム結晶格子の格子定数は462 pmであり、ナトリウムイオン Na+ およびフッ化物イオン F− の半径の合計は231 pmとなるが単独のイオン半径はこの方法から知ることができない。
これらのイオンは共にネオンの電子配置 1s22s22p6 をとりスレーター軌道に基いて遮蔽定数を求めると 4.15 となる。ナトリウムイオンの有効核電荷は 11−4.15=6.85 、フッ化物イオンは 9−4.15=4.85 となり、イオン半径比は以下のようになる。これから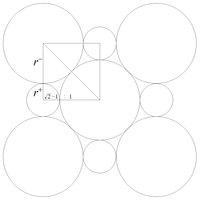
結晶格子中において陽イオンは陰イオンに、陰イオンは陽イオンにそれぞれ取り囲まれた配位構造であるが、同じ電荷のイオン同士では反発力が働き、それらが互いに接触した状態は不安定である。そのため各結晶格子について同種電荷のイオン同士が接触しない限界半径比(critical radius ratio)がある。
塩化セシウム型構造(8配位)をとるためには限界半径比は すなわち r− / r+ < 1.366 となる。
塩化ナトリウム型構造(6配位)では すなわち 1.366 < r− / r+ < 2.414 となる。
閃亜鉛鉱型構造(4配位)では すなわち 2.414 < r− / r+ < 4.449 となる。
また正三角形3配位では すなわち 4.449 < r− / r+ < 6.464 となる。
ただし、これらの r− / r+ は r+ / r− と置き換えても良い。
- ^ L. Pauling, The Nature of the Chemical Bond, 3rd Edn., Cornell University Press, Ithaca, N. Y. (1960).
- ^ FA コットン, G. ウィルキンソン著, 中原 勝儼訳 『コットン・ウィルキンソン無機化学』 培風館、1987年
- ^ 長島弘三、佐野博敏、富田 功 『無機化学』 実教出版
- ^ 松井義人、一国雅巳 訳 『メイスン 一般地球化学』 岩波書店、1970年
- ^ 日本化学会編 『改訂4版 化学便覧 基礎編』 丸善
- ^ 新村陽一 『無機化学』 朝倉書店、1984年
- ^ 田中元治 『基礎化学選書8 酸と塩基』 裳華房、1971年
- 1 イオン半径とは
- 2 イオン半径の概要
- 3 水和イオンの性質