タンパク質合成
まず、遺伝子の情報が、細胞核内でコピーされ、mRNAという分子になる過程を転写といい、このmRNAが細胞核外の細胞質へ移動する。次に転写により写し取ったmRNAの遺伝情報(アミノ酸の配列情報)をもとに、リボソームという細胞小器官でアミノ酸が結合され、タンパク質が合成される。この過程を翻訳という。このようにしてDNA上にある遺伝子の塩基配列からタンパク質が作られる。
生物の体を形成しているタンパク質は細胞核内のDNAの一部である遺伝子の情報をもとに作られている。遺伝子情報は、タンパク質を形成しているアミノ酸の配列情報のもとととなる。タンパク質は細胞核の外で合成され、タンパク質の合成には転写と翻訳、2つの過程が必要になる。この過程をタンパク質合成という。 まず、遺伝子の情報が、細胞核内でコピーされ、mRNAという分子になる過程を転写といい、このmRNAが細胞核外の細胞質へ移動する。次に転写により写し取ったmRNAの遺伝情報(アミノ酸の配列情報)をもとに、リボソームという細胞小器官でアミノ酸が結合され、タンパク質が合成される。この過程を翻訳という。このようにしてDNA上にある遺伝子の塩基配列からタンパク質が作られる。 | 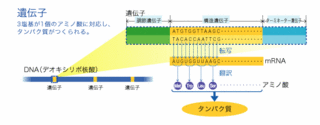 拡大表示 |
・ タンパク質
・ 細胞核
・ デオキシリボ核酸
・ 遺伝子
・ アミノ酸
・ メッセンジャーRNA
・ 遺伝
・ 塩基配列
タンパク質生合成
(タンパク質合成 から転送)
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/04/07 09:46 UTC 版)
タンパク質生合成(たんぱくしつせいごうせい、英: protein biosynthesis)は、タンパク質合成(英: protein synthesis)とも呼ばれ、細胞内で行われる中心的な生物学的プロセスであり、新しいタンパク質の生成を通じて細胞内タンパク質の消失(分解や輸送)とのバランスを維持する。タンパク質は、酵素、構造タンパク質、またはホルモンとして、多くの重要な機能を果たしている。原核生物と真核生物の両方で、タンパク質生合成は非常によく似たプロセスであるが、いくつかの明確な違いがある[1]。
- ^ a b c d e f g h i j Alberts B (2015). Molecular biology of the cell (Sixth ed.). Abingdon, UK: Garland Science, Taylor and Francis Group. ISBN 978-0815344643
- ^ O'Connor C (2010). Essentials of Cell Biology. NPG Education: Cambridge, MA 2020年3月3日閲覧。
- ^ a b Wang YC, Peterson SE, Loring JF (February 2014). “Protein post-translational modifications and regulation of pluripotency in human stem cells”. Cell Research 24 (2): 143–160. doi:10.1038/cr.2013.151. PMC 3915910. PMID 24217768.
- ^ Scheper GC, van der Knaap MS, Proud CG (September 2007). “Translation matters: protein synthesis defects in inherited disease”. Nature Reviews. Genetics 8 (9): 711–723. doi:10.1038/nrg2142. PMID 17680008.
- ^ Berg JM, Tymoczko JL, Gatto Jr GJ, Stryer L (2015). Biochemistry (Eighth ed.). US: W. H. Freeman and Company. ISBN 9781464126109
- ^ a b c d e f Toole G, Toole S (2015). AQA biology A level. Student book (Second ed.). Great Clarendon Street, Oxford, OX2 6DP, UK: Oxford University Press. ISBN 9780198351771
- ^ Berk A, Lodish H, Darnell JE (2000). Molecular cell biology (4th ed.). New York: W.H. Freeman. ISBN 9780716737063
- ^ a b “Eukaryotic pre-mRNA processing”. Khan Academy. 2020年3月9日閲覧。
- ^ Jo BS, Choi SS (December 2015). “Introns: The Functional Benefits of Introns in Genomes”. Genomics & Informatics 13 (4): 112–118. doi:10.5808/GI.2015.13.4.112. PMC 4742320. PMID 26865841.
- ^ “Stages of translation (article)” (英語). Khan Academy. 2020年3月10日閲覧。
- ^ “Nucleus and ribosomes (article)” (英語). Khan Academy. 2020年3月10日閲覧。
- ^ a b Cooper GM (2000). The cell : a molecular approach (2nd ed.). Sunderland (MA): Sinauer Associates. ISBN 9780878931064
- ^ “Protein structure: Primary, secondary, tertiary & quatrenary (article)” (英語). Khan Academy. 2020年3月11日閲覧。
- ^ Duan G, Walther D (February 2015). “The roles of post-translational modifications in the context of protein interaction networks”. PLoS Computational Biology 11 (2): e1004049. Bibcode: 2015PLSCB..11E4049D. doi:10.1371/journal.pcbi.1004049. PMC 4333291. PMID 25692714.
- ^ a b Schubert M, Walczak MJ, Aebi M, Wider G (June 2015). “Posttranslational modifications of intact proteins detected by NMR spectroscopy: application to glycosylation”. Angewandte Chemie 54 (24): 7096–7100. doi:10.1002/anie.201502093. PMID 25924827.
- ^ Ciechanover A (January 2005). “Proteolysis: from the lysosome to ubiquitin and the proteasome”. Nature Reviews. Molecular Cell Biology 6 (1): 79–87. doi:10.1038/nrm1552. PMID 15688069.
- ^ Brenner S, Miller JH (2001). Encyclopedia of genetics. Elsevier Science Inc. pp. 2800. ISBN 978-0-12-227080-2
- ^ Murn J, Shi Y (August 2017). “The winding path of protein methylation research: milestones and new frontiers”. Nature Reviews. Molecular Cell Biology 18 (8): 517–527. doi:10.1038/nrm.2017.35. PMID 28512349.
- ^ Drazic A, Myklebust LM, Ree R, Arnesen T (October 2016). “The world of protein acetylation”. Biochimica et Biophysica Acta 1864 (10): 1372–1401. doi:10.1016/j.bbapap.2016.06.007. PMID 27296530.
- ^ Bannister AJ, Kouzarides T (March 2011). “Regulation of chromatin by histone modifications”. Cell Research 21 (3): 381–395. doi:10.1038/cr.2011.22. PMC 3193420. PMID 21321607.
- ^ a b Habara A, Steinberg MH (April 2016). “Minireview: Genetic basis of heterogeneity and severity in sickle cell disease”. Experimental Biology and Medicine 241 (7): 689–696. doi:10.1177/1535370216636726. PMC 4950383. PMID 26936084.
- ^ Sickle Cell Anemia. StatPearls Publishing. (2020). PMID 29489205 2020年3月12日閲覧。.
- ^ Ilesanmi OO (January 2010). “Pathological basis of symptoms and crises in sickle cell disorder: implications for counseling and psychotherapy”. Hematology Reports 2 (1): e2. doi:10.4081/hr.2010.e2. PMC 3222266. PMID 22184515.
- ^ a b “Cell Division, Cancer | Learn Science at Scitable” (英語). www.nature.com. 2021年11月30日閲覧。
- ^ “p53, Cancer | Learn Science at Scitable” (英語). www.nature.com. 2021年11月30日閲覧。
タンパク質合成
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2020/04/23 16:10 UTC 版)
EF-Tu はタンパク質合成のポリペプチドの伸長過程に関与する。細菌では、EF-Tu の主要な機能は正しい aa-tRNA をリボソームのA部位に運搬することである。EF-Tu はGタンパク質であり、その機能には GTP が利用される。リボソーム外で、GTP を結合した EF-Tu (EF-Tu•GTP) が aa-tRNA と安定な EF-Tu•GTP•aa-tRNA 三者複合体を形成する。EF-Tu•GTP は、開始tRNAとセレノシステイン-tRNA を除く、全ての正しくアミノ酸が付加された aa-tRNA とほぼ同じ親和性で結合する。アミノ酸残基の性質はそれぞれ異なるが、側鎖の結合親和性の差を補償するさまざまな構造を tRNA は持っている。 三者複合体はリボソームのA部位に移動し、tRNA のアンチコドンが mRNA のコドンと対合する。正しいアンチコドンが mRNA のコドンに対合している場合には、リボソームはその構成を変化させて EF-Tu の GTPアーゼドメインの形状を変化させる。その結果、EF-Tu に結合した GTP は GDP とリン酸に加水分解される。このように、リボソームは EF-Tu に対して GTPアーゼ活性化タンパク質 (GAP) のような機能を果たす。GTP の加水分解に伴って EF-Tu のコンフォメーションは劇的に変化し、aa-tRNA を解離してリボソームから出てゆく。その後 aa-tRNA はA部位に深く入り込み、そのアミノ酸部分はP部位のポリペプチドに近接する。そしてリボソームはP部位のポリペプチドからA部位のアミノ酸への共有結合の転移を触媒する。 細胞質では、細菌の翻訳伸長因子 EF-Ts(英語版) によって、不活性化された EF-Tu•GDP から GDP が取り除かれる。EF-Ts が EF-Tu から解離すると、EF-Tu は GTP と複合体を形成する。これは細胞質の GTP の濃度が GDP の濃度よりも5-10倍高いためである。このようにして再活性化された EF-Tu•GTP は、再び別の aa-tRNA と三者複合体を形成する。
※この「タンパク質合成」の解説は、「EF-Tu」の解説の一部です。
「タンパク質合成」を含む「EF-Tu」の記事については、「EF-Tu」の概要を参照ください。
タンパク質合成
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/02/11 00:28 UTC 版)
タンパク質は生命に欠かせないものである。細胞は、DNAにコード化された情報をもとに、アミノ酸の構成要素から新しいタンパク質分子を作り出している。それぞれの種類のタンパク質は、通常は一つの機能しか果たさない専門家であるため、細胞が何か新しいことをする必要があれば、新しいタンパク質を作らなければならない。ウイルスは細胞に、細胞が必要としないがウイルスが繁殖するために必要な新しいタンパク質を作るように強制する。タンパク質生合成は、転写と翻訳という2つの主要なステップで構成されている。 転写とは、遺伝情報と呼ばれるDNAの情報を使用して、メッセンジャーRNA (mRNA) と呼ばれるRNAコピーを生成するプロセスである。mRNAは細胞内を移動して、タンパク質を作るために使用されるリボソームに遺伝情報を伝える。タンパク質のアミノ酸構造はmRNAの遺伝情報によって決定されるため、これは翻訳と呼ばれる。情報はゆえに核酸の言語からアミノ酸の言語に翻訳される。 RNAウイルスの一部の核酸は、それ以上修飾することなくmRNAとして直接機能する。このため、これらのウイルスはポジティブセンスRNAウイルスと呼ばれている。他のRNAウイルスでは、RNAはmRNAの相補的なコピーであり、これらのウイルスはmRNAを作るために細胞の酵素や自身の酵素に依存している。これらはネガティブセンスRNAウイルスと呼ばれている。DNAから作られたウイルスでは、mRNAの作り方は細胞のそれと似ている。レトロウイルスと呼ばれるウイルスの種類は完全に異なったふるまいをする。それらはRNAを持っているが、宿主細胞の中では逆転写酵素の助けを借りてRNAのDNAコピーが作られる。次に、このDNAは宿主自身のDNAに組み込まれ、細胞の通常の経路によってmRNAにコピーされる。
※この「タンパク質合成」の解説は、「ウイルスの紹介」の解説の一部です。
「タンパク質合成」を含む「ウイルスの紹介」の記事については、「ウイルスの紹介」の概要を参照ください。
タンパク質合成
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2021/09/18 08:22 UTC 版)
肝細胞はアルブミン、血液凝固因子のフィブリノーゲン及びプロトロンビンを製造する。またリポタンパク質、セルロプラスミン、トランスフェリン、補体系タンパク質、および糖タンパク質の主な合成の場である。肝細胞はそれ自身の構造タンパク質、細胞内酵素も製造する。 タンパク質の合成は粗面小胞体(RER)で行われる。粗面、滑面(SER)両小胞体は生成されたタンパク質の分泌に関与する。
※この「タンパク質合成」の解説は、「肝細胞」の解説の一部です。
「タンパク質合成」を含む「肝細胞」の記事については、「肝細胞」の概要を参照ください。
「タンパク質合成」の例文・使い方・用例・文例
- タンパク質合成のページへのリンク



